Clear Sky Science · pl
Aktywowane limfocyty T wywołują apoptozę w komórkach gruczolakoraka płuca A549 poprzez TRPV4‑zależny napływ wapnia
Dlaczego to badanie ma znaczenie dla raka płuca
Rak płuca wciąż należy do najgroźniejszych nowotworów, częściowo dlatego, że guzy często uczą się opierać standardowym terapiom, takim jak chemioterapia czy radioterapia. W ostatnich latach nadzieję przyniosło wykorzystanie własnego układu odpornościowego. To badanie bada nowy aspekt tej koncepcji: pokazuje, jak specyficzny typ komórki odpornościowej, zwany aktywowanym limfocytem T, może skłaniać komórki raka płuca do samozniszczenia, wymuszając ich pobór jonów wapnia przez molekularną „bramkę” TRPV4. Zrozumienie tej ścieżki może pomóc naukowcom zaprojektować bardziej skuteczne i precyzyjne immunoterapie.
Żołnierze układu odpornościowego spotykają komórki guza płuca
Naukowcy skupili się na ludzkich komórkach gruczolakoraka płuca oznaczonych jako A549, szeroko stosowanym modelu niedrobnokomórkowego raka płuca. Połączyli te komórki nowotworowe z komórkami Jurkat, które zastępują w badaniu cytotoksyczne limfocyty T, normalnie wyszukujące i niszczące zakażone lub złośliwe komórki. Chemicznie aktywując komórki Jurkat, zespół odtworzył wysoce pobudzonego stanu limfocytów uczestniczących w rzeczywistej odpowiedzi odpornościowej. Następnie mieszali aktywowane lub nieaktywowane limfocyty T z komórkami raka płuca w różnych proporcjach i obserwowali przebieg przez jeden do trzech dni, zwracając szczególną uwagę na to, ile komórek nowotworowych przeżywało oraz ile ulegało zaprogramowanej śmierci, czyli apoptozie.
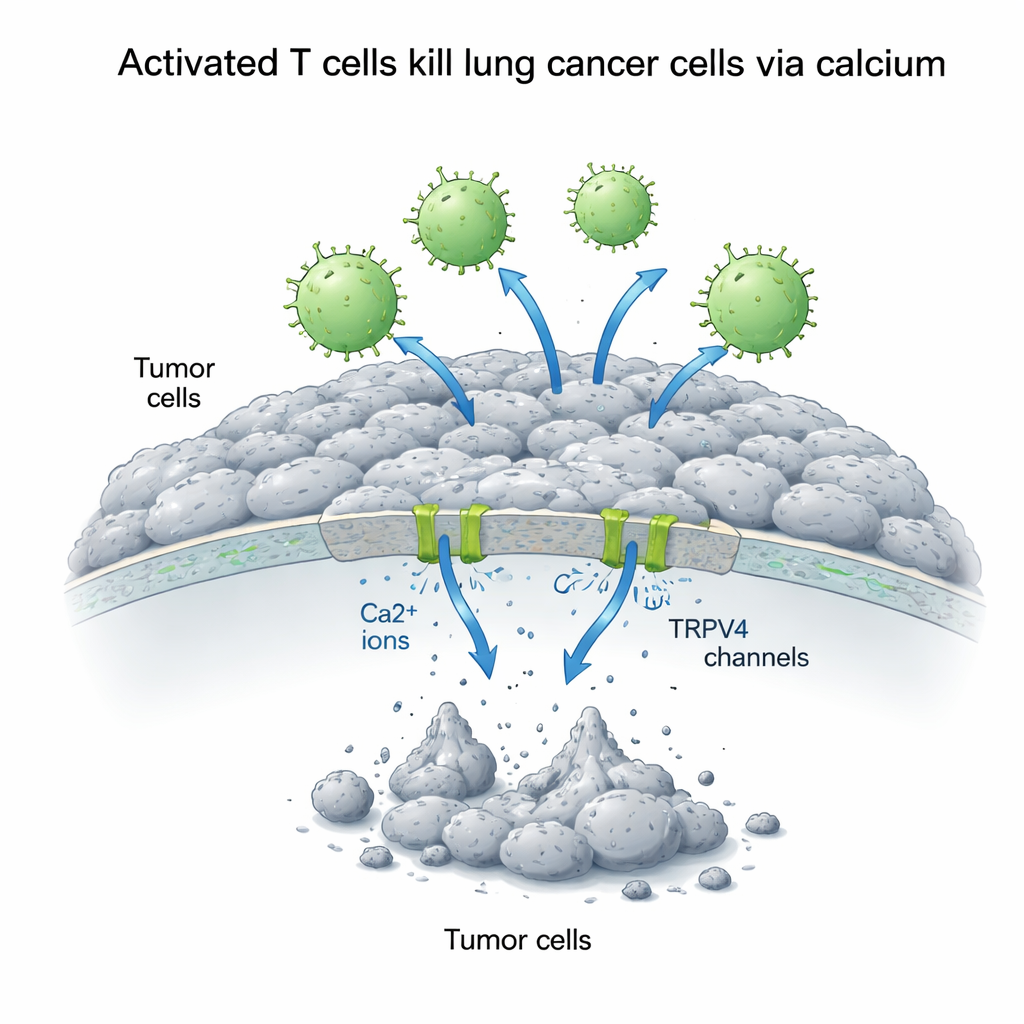
Wapń jako obosieczny sygnał dla komórek nowotworowych
Wapń wewnątrz komórek działa jak wszechstronny przełącznik sygnałowy, który może sprzyjać wzrostowi lub wywoływać śmierć, w zależności od sposobu jego regulacji. Naukowcy zwiększyli stężenie wapnia na zewnątrz komórek A549 i zmierzyli, jak to wpływa na rywalizację między limfocytami T a komórkami guza. Zaskakująco, sam dodatkowy wapń poprawiał wzrost komórek raka płuca, co sugeruje, że w spokojnych warunkach wapń zasila szlaki sprzyjające przetrwaniu. Jednak w obecności aktywowanych limfocytów T sytuacja się odwróciła: wyższe stężenie wapnia znacznie wzmocniło zabijanie przez limfocyty T. W ciągu 72 godzin przeżywalność komórek nowotworowych spadła do mniej niż jednej trzeciej wartości kontrolnej, gdy połączono aktywowane limfocyty T i dodatkowy wapń, podczas gdy nieaktywowane limfocyty T miały niewielki wpływ, a w niektórych przypadkach przy dodatku wapnia mogły nawet wspierać wzrost.
„Bramka” wapniowa związana ze stresem i śmiercią komórki
Aby zrozumieć, jak dochodzi do przełączenia od wzrostu do śmierci, zespół zbadał TRPV4 — białkowy kanał w błonie komórkowej, który pozwala na napływ jonów wapnia. Analiza białek wykazała, że poziomy TRPV4 wzrosły wyraźnie, gdy komórki A549 były wystawione na dodatkowy wapń, niezależnie od obecności limfocytów T, a najwyższe wartości obserwowano przy połączeniu wapnia i aktywowanych limfocytów T. Równocześnie komórki nowotworowe wykazywały wyraźne oznaki stresu oksydacyjnego: równowaga przesunęła się z ochronnych antyoksydantów (niższa całkowita zdolność antyoksydacyjna) na rzecz szkodliwych utleniaczy (wyższy całkowity status utleniający). Cytometria przepływowa, technika barwienia komórek barwnikami fluorescencyjnymi, potwierdziła, że aktywowane limfocyty T powodowały gwałtowny wzrost zarówno wczesnych, jak i późnych etapów apoptozy, zwłaszcza gdy wapnia było dużo. Razem te obserwacje wskazują na ciąg zdarzeń, w którym kanały TRPV4 dopuszczają więcej wapnia, co następnie napędza stres chemiczny wewnątrz komórki i popycha ją ku śmierci.
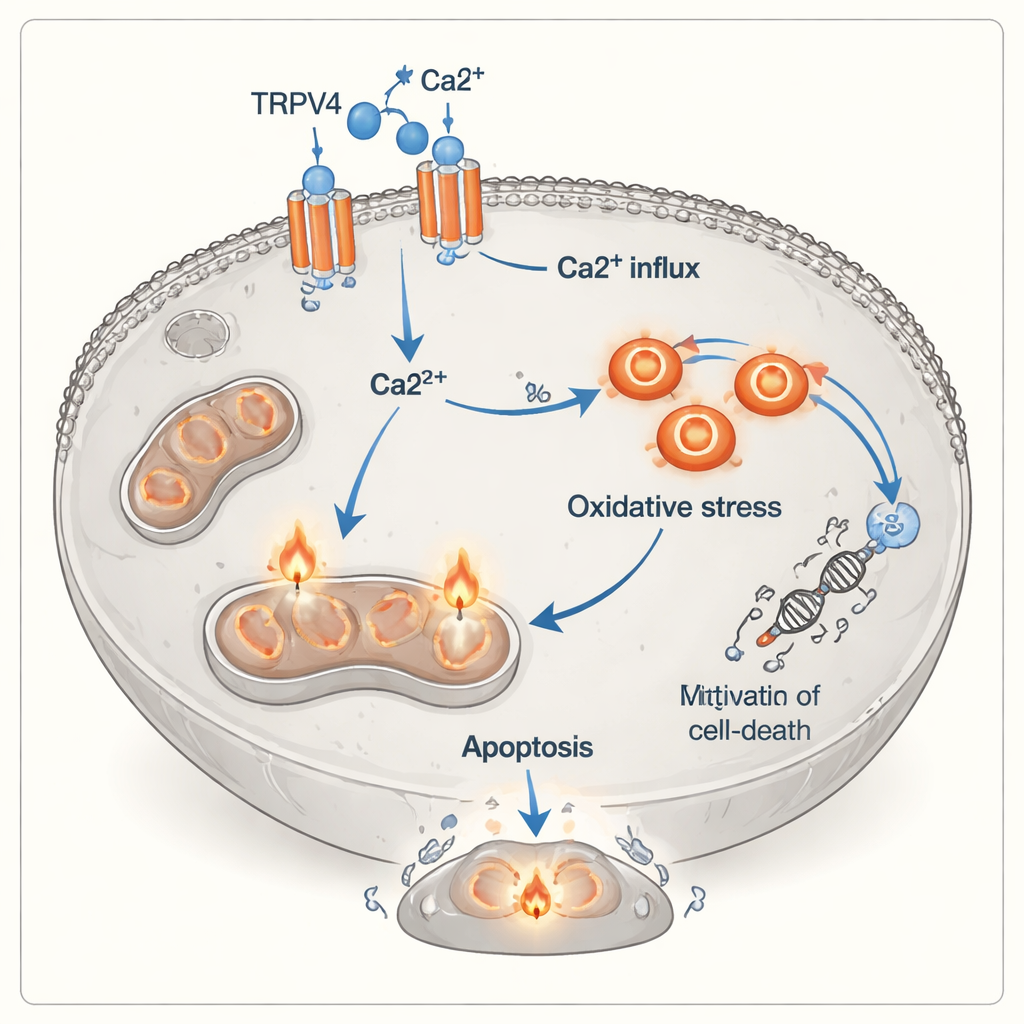
Nowy wymiar mechanizmu niszczenia guzów przez komórki odpornościowe
Klasycznie cytotoksyczne limfocyty T niszczą swoje cele przez uwalnianie toksycznych białek lub aktywowanie receptorów śmierci na powierzchni komórki nowotworowej. To badanie sugeruje istnienie dodatkowej, bardziej pośredniej drogi: sygnały pochodzące od aktywowanych limfocytów T — w tym molekuły zapalne i bliski kontakt komórka‑komórka — wydają się czynić komórki raka płuca bardziej zależnymi od TRPV4 i bardziej podatnymi na przeciążenie wapniowe oraz uszkodzenia oksydacyjne. W tym ujęciu TRPV4 działa jak przełącznik uwrażliwiający, który zamienia inaczej sprzyjający wzrostowi wapń w sygnał śmierci. Chociaż eksperymenty przeprowadzono w hodowlach in vitro i użyto jednej linii komórkowej nowotworu, wyniki ukazują potencjalnie istotne połączenie między atakiem immunologicznym, kanałami jonowymi a wewnętrznym mechanizmem stresu komórkowego w komórkach guza.
Co to może znaczyć dla przyszłych terapii
Dla czytelników nietechnicznych wniosek jest taki, że powodzenie immunoterapii może zależeć nie tylko od wzmacniania limfocytów T, lecz także od uczynienia komórek nowotworowych bardziej podatnymi na zabicie. Celowanie w TRPV4 lub pokrewne kanały wapniowe mogłoby w przyszłości zwiększyć zdolność limfocytów T do eliminacji guzów płuca lub pozwolić na dopracowanie terapii tak, by unikać uszkodzeń tkanek zdrowych. Prace są wciąż na wczesnym etapie, a autorzy podkreślają konieczność dalszych badań na modelach zwierzęcych i w bardziej złożonych układach. Mimo to odkrycie osi TRPV4–wapń–stres oksydacyjny dodaje obiecujący nowy cel do zestawu narzędzi mających poprawić terapie oparte na układzie odpornościowym przeciw rakowi płuca.
Cytowanie: Alavi, F., Kazemi-Lomedasht, F., Eftekhari, Z. et al. Activated T cells induce apoptosis in A549 lung adenocarcinoma cells via TRPV4-mediated calcium influx. Sci Rep 16, 7155 (2026). https://doi.org/10.1038/s41598-026-38589-2
Słowa kluczowe: immunoterapia raka płuca, limfocyty T, sygnalizacja wapniowa, kanał TRPV4, stres oksydacyjny