Clear Sky Science · pl
Optymalizacja czynników wiążących galektynę‑3 przez syntezę wieloskładnikową in situ i natywną spektrometrię mas
Dlaczego to ma znaczenie dla przyszłych leków
Wiele współczesnych leków działa przez przyłączanie się do białek w organizmie, jednak znalezienie małej cząsteczki, która mocno i selektywnie wiąże się we właściwym miejscu, jest powolne, kosztowne i często frustrujące. Badanie to przedstawia szybszy sposób dopracowania takich molekuł bezpośrednio w obecności białka‑celu, a następnie wybrania zwycięzców za pomocą bardzo czułej techniki ważenia. Autorzy pokazują swoją metodę na przykładzie galektyny‑3, białka powiązanego z rozwojem nowotworów, i otrzymują obiecujący kandydat o właściwościach podobnych do leków, który wiąże się tak mocno jak jedne z najlepszych znanych związków, lecz w nieoczekiwanym zagłębieniu na powierzchni białka.

Przemyślenie polowania na lepsze kandydata na leki
Tradycyjna optymalizacja leków przypomina kosztowną grę w zgadywanie. Chemicy modyfikują związek wyjściowy krok po kroku, testują każdą wersję i liczą na zwiększenie siły wiązania z białkiem‑celem. Jednak powierzchnie białek są elastyczne, cząsteczki wody wchodzą w interakcje, a samo wiązanie może przeformować białko, co czyni przewidywania komputerowe zawodnymi. Nawet gdy dostępna jest struktura w wysokiej rozdzielczości, nie ma gwarancji, że sugerowana zmiana pomoże. Istniejące metody „ukierunkowane przez cel” próbują pozwolić białku wybrać partnerów z puli cegiełek, lecz te podejścia nadal opierają się na złożonej analizie i pośrednich sygnałach, by wywnioskować, który związek naprawdę wiąże się najlepiej.
Pozwól białku wybrać, a potem zważyć zwycięzców
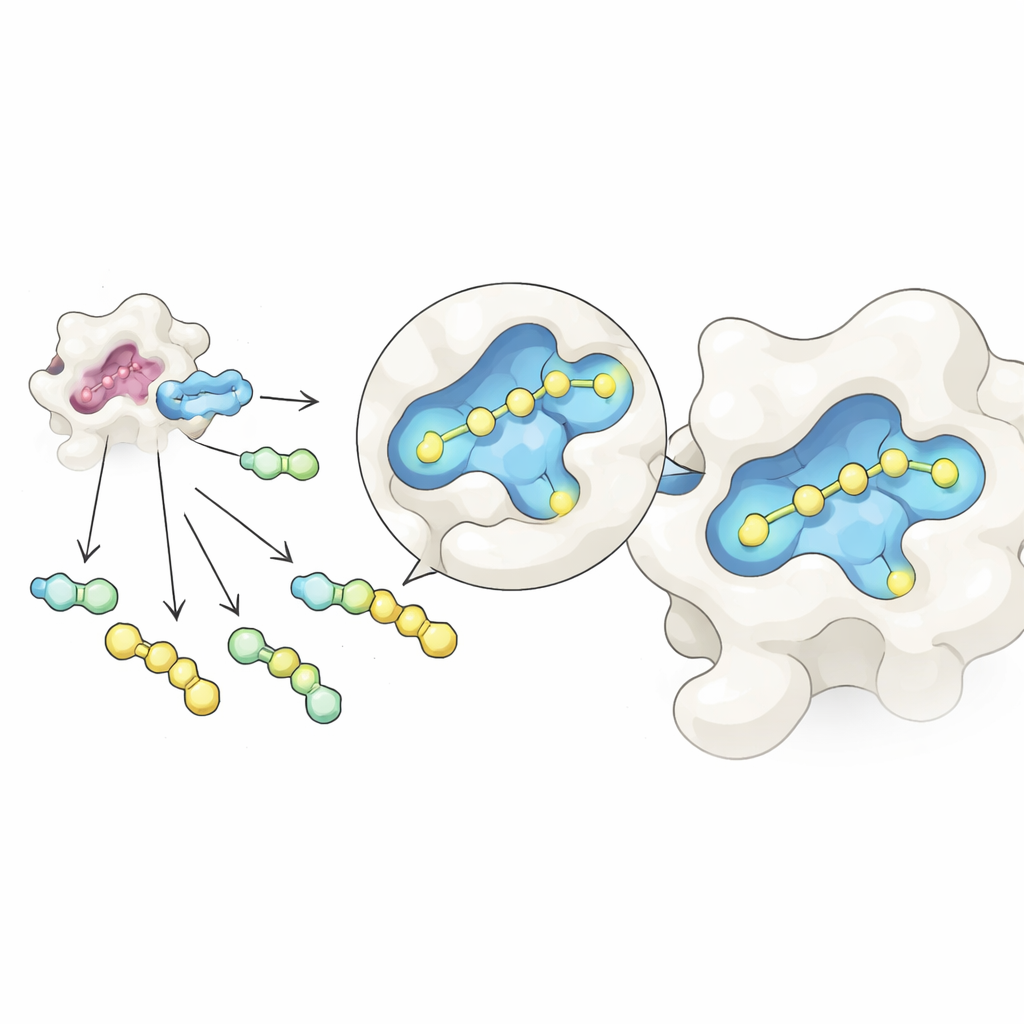
Badacze połączyli dwie koncepcje w jedną usprawnioną procedurę. Po pierwsze zastosowali odwracalną reakcję chemiczną, która łączy wspólne cukrowe rdzenie z wieloma różnymi bocznymi fragmentami w jednej probówce, tworząc mieszaninę powiązanych cząsteczek. Poprzez staranne dostosowanie stosunków wyjściowych, powstałe produkty osiągają stan równowagi regulowany prostymi zasadami stężenia, co pomaga wyrównać ich ilości mimo różnic w reaktywności. Po drugie, wystawili tę mieszaninę na działanie galektyny‑3 i zbadali ją za pomocą natywnej spektrometrii mas — odmiany spektrometrii mas, która utrzymuje pary białko–cząsteczka nienaruszone w łagodnym, wodnym środowisku. Ponieważ każdy kandydat ma unikalną masę, instrument może bezpośrednio wykryć, które molekuły rzeczywiście są związane z białkiem, bez użycia znaczników czy wzorców referencyjnych.
Z zatłoczonych mieszanin do wyróżniającego się liganda
Wykorzystując to ustawienie, zespół stworzył dziesiątki ligandów galektyny‑3 poprzez przyłączanie różnych grup bocznych do cukrowego rdzenia inspirowanego znanym inhibitorem GB1107. Podzielili 35 różnych hydrazydów na przystępne grupy, wytworzyli wszystkie kombinacje in situ, a następnie dodali galektynę‑3. Natywna spektrometria mas wyróżniła te związki, które najczęściej podróżowały razem z białkiem, wskazując je jako główne trafienia. Następnie test stabilności termicznej, który mierzy, jak związek stabilizuje białko podczas ogrzewania, odfiltrował fałszywe pozytywy spowodowane osobliwościami pomiaru w fazie gazowej. Pozostały trzy wiodące kandydatury, a szczegółowe pomiary wiązania oparte na cieple wykazały, że jeden z nich, nazwany GalAldBZ20, wiązał galektynę‑3 szczególnie silnie, w zakresie poniżej mikromolowego.
Odkrycie ukrytej kieszeni i jej wzmocnienie
Następne zaskoczenie pojawiło się, gdy zespół przyjrzał się, jak GalAldBZ20 osadza się na powierzchni galektyny‑3. Większość znanych ligandów korzysta z kieszeni „alfa” w pobliżu miejsca wiążącego cukier, ale metody strukturalne i symulacje komputerowe wskazały, że GalAldBZ20 zamiast tego preferuje sąsiednią kieszeń „beta”. Krystalografia rentgenowska zasugerowała to, spektroskopia magnetycznego rezonansu jądrowego w roztworze ujawniła wiele lokalnych konformacji w pobliżu tej kieszeni, a symulacje dynamiki molekularnej poparły model, w którym pierścień z grupą nitrową molekuły wcisnął się w miejsce beta. Zakładając, że można usztywnić to ustawienie, chemicy przeprojektowali łącznik chemiczny między cukrem a pierścieniem nitrowym, aby sprzyjać nowym kontaktom polarnym z białkiem i zmniejszyć elastyczność.
Przekształcenie sprytnego przesiewu w silnego kandydata
Z tą wiedzą zespół zsyntetyzował niewielką serię bardziej sztywnych cząsteczek następczych, które zachowały ten sam cukier i pierścień nitrowy, ale zmieniły łącznik między nimi. Jedna wersja, N‑galaktozyd (związek 5), wyróżniła się: wiązała galektynę‑3 około dziesięć razy silniej niż pierwotne trafienie, osiągając siłę wiązania porównywalną z GB1107, a mimo to nadal preferowała kieszeń beta. Krystalograficzna struktura o ultra‑wysokiej rozdzielczości pokazała wyraźną gęstość dla pierścienia nitrowego w tej kieszeni, wspieraną przez kilka wiązań wodorowych i oddziaływanie kation‑π z kluczowymi aminokwasami. Gdy grupa nitrowa została usunięta lub zastąpiona prostą grupą metylową, wiązanie istotnie osłabło, podkreślając jej znaczenie. Ponieważ galektyna‑1, białko spokrewnione, nie ma tej kieszeni beta, nowy związek może ostatecznie zapewnić lepszą selektywność — cenioną cechę w projektowaniu leków.
Co to oznacza dla przyszłego odkrywania leków
Mówiąc prosto, praca ta pokazuje, że można zmieszać wiele spokrewnionych molekuł, pozwolić białku powiązanemu z chorobą „wybrać” faworytów, a następnie bezpośrednio zważyć te pary białko–cząsteczka, by sprawdzić, które najlepiej się trzymają. Zastosowana do galektyny‑3 strategia niespodziewanie odkryła, a potem wzmocniła wiązanie w mniej zbadanej kieszeni, dając związek konkurujący z najlepszymi istniejącymi inhibitorami i mogący służyć jako kandydat do nowych leków przeciwnowotworowych. W szerszym ujęciu łączenie chemii in situ z natywną spektrometrią mas oferuje ogólny skrót do udoskonalania kandydatów na leki przeciwko białkom z wieloma możliwymi miejscami wiążącymi, potencjalnie oszczędzając czas, materiały i wysiłek na wczesnych etapach odkrywania leków.
Cytowanie: Hoshi, K., Konuma, T., Taguchi, R. et al. Optimization of galectin-3 binding agents by in situ multiple compound synthesis and native mass spectrometry. Sci Rep 16, 8453 (2026). https://doi.org/10.1038/s41598-026-38570-z
Słowa kluczowe: inhibitory galektyny‑3, natywna spektrometria mas, odkrywanie leków oparte na fragmentach, synteza ukierunkowana przez cel, kandydata na leki przeciwnowotworowe