Clear Sky Science · pl
Analiza integrująca transkryptom i sekwencjonowanie pojedynczych komórek wraz z walidacją eksperymentalną identyfikuje markery związane z komórkami T i starzeniem w sepsie
Dlaczego te badania mają znaczenie dla pacjentów z ciężkimi zakażeniami
Sepsa to zagrażająca życiu reakcja na zakażenie, która może przemienić rutynową chorobę lub uraz w stan nagły, często w ciągu kilku godzin. Lekarze wciąż nie dysponują prostym i niezawodnym sposobem na wykrycie, którzy pacjenci zmierzają w kierunku niewydolności narządów, a brak jest leków zaprojektowanych specjalnie do korekty chaosu immunologicznego wywołanego przez sepsę. W badaniu tym analizowano, w jaki sposób pewne komórki układu odpornościowego, zwane komórkami T, oraz ich przedwczesne starzenie mogą napędzać sepsę — oraz zidentyfikowano niewielki zestaw genów, które mogłyby pomóc lekarzom w wcześniejszej diagnozie i wskazać nowe możliwości terapii.
Sepsa: gdy mechanizmy obronne organizmu zawodzą
W sepsie układ odpornościowy najpierw wybucha gwałtowną reakcją zapalną, a następnie często przechodzi w niebezpieczne wyciszenie. Komórki T, które zwykle pomagają zwalczać zakażenia i pamiętają o wcześniejszych kontaktach z patogenami, stają się mniej liczne i mniej sprawne w działaniu. Równocześnie wiele komórek odpornościowych wykazuje cechy „senescencji” — rodzaju komórkowego starzenia, w którym komórki przestają się dzielić, ale nadal wydzielają sygnały zapalne. Autorzy założyli, że jeśli uda się im wskazać geny związane jednocześnie z komórkami T i z senescencją, mogą odkryć nowe markery ujawniające, kto rozwija sepsę i dlaczego niektórzy pacjenci pogarszają się szybciej niż inni.
Analiza krwi na poziomie pojedynczych komórek
Zespół połączył kilka warstw danych pochodzących z próbek krwi osób z sepsą i bez niej. Najpierw wykorzystano dane z transkryptomu zbiorczego (informacje o tym, które geny są aktywne), aby znaleźć prawie 10 000 genów o zmienionej aktywności w sepsie. Następnie, stosując sekwencjonowanie RNA pojedynczych komórek, przebadano dziesiątki tysięcy poszczególnych komórek krwi i zidentyfikowano ponad 1 300 genów zmienionych specyficznie w komórkach T. Przez przecięcie tych zestawów z wcześniej opracowaną listą 866 genów zaangażowanych w starzenie komórkowe, zawężono pole do 45 kandydatów znajdujących się na skrzyżowaniu sepsy, komórek T i senescencji. 
Odkrycie czterech kluczowych genetycznych drogowskazów
Aby dodatkowo przefiltrować tę listę, badacze zastosowali dwie techniki uczenia maszynowego poszukujące najbardziej informatywnych cech w złożonych danych. Podejścia te skupiły się na sześciu obiecujących genach, a po weryfikacji w dwóch niezależnych zbiorach danych cztery z nich konsekwentnie się wyróżniały: PATZ1, SIN3B, BLK i MTHFD2. W danych publicznych PATZ1, SIN3B i BLK były obniżone w sepsie, podczas gdy MTHFD2 był podwyższony. W małej grupie próbek klinicznych zbadanych metodą RT-qPCR pierwsze trzy geny ponownie wykazały wyraźne obniżenie w krwi pacjentów z sepsą, natomiast MTHFD2 nie pokazał jednoznacznej różnicy — co może sugerować, że jego rola dotyczy bardziej funkcji białka niż poziomu ekspresji genu.
Jak te geny wiążą się z równowagą immunologiczną i potencjalnymi lekami
Dalsze analizy powiązały każdy gen z szerszymi ścieżkami biologicznymi. PATZ1 był związany z replikacją DNA i sygnalizacją receptora komórek T — procesami niezbędnymi do mnożenia się komórek T i ich reakcji na zakażenie. SIN3B łączono z układem sygnalizacji lipidowej wpływającym na przeżywalność komórek i stany zapalne. BLK, lepiej znany z chorób autoimmunologicznych, był powiązany z rozwojem komórek krwi i obroną immunologiczną jelit, w tym produkcją przeciwciał IgA chroniących barierę jelitową. MTHFD2 wiązał się z maszynerią syntezy i degradacji białek, kluczową dla dostosowania metabolizmu komórek odpornościowych w warunkach stresu. Analiza wzorców „infiltracji” komórek odpornościowych w krwi wykazała, że wyższy poziom PATZ1 szedł w parze z większą liczbą limfocytów CD8 i mniejszą liczbą neutrofili — równowagą, która może sprzyjać lepszej kontroli zakażenia. Wykorzystując te cztery geny, badacze zbudowali sztuczną sieć neuronową — prosty model AI — który w dwóch zewnętrznych zbiorach danych odróżniał przypadki sepsy od braku sepsy z niemal doskonałą dokładnością. Korzystając także z bazy danych lek–gen i symulacji dokowania molekularnego, zaproponowali kilka istniejących związków, w tym antybiotyk latamoksef oraz molekuły emetynę i dihydroergotaminę, jako kandydatów silnie wiążących się z tymi celami. 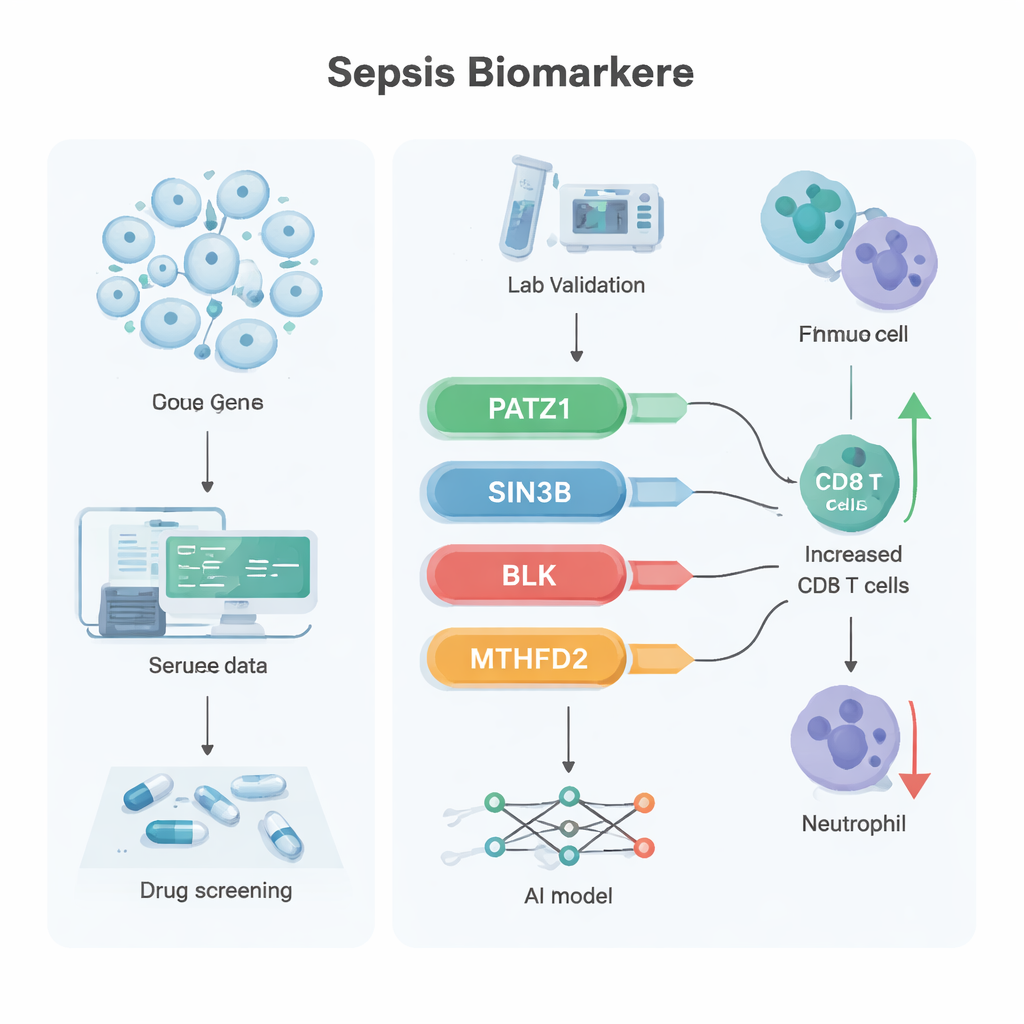
Co to może oznaczać dla przyszłej opieki
Dla czytelnika niebędącego specjalistą kluczowy wniosek jest taki, że badanie to identyfikuje cztery geny działające jak sygnały ostrzegawcze na komórkach T, które zawodzą i starzeją się przedwcześnie podczas sepsy. Razem te geny tworzą potencjalny panel badań krwi, który mógłby w przyszłości pomóc lekarzom w wcześniejszej i dokładniejszej diagnozie sepsy niż obecne narzędzia. Dają też wskazówki, jak zawodzi wykorzystanie energii i mechanizmy naprawcze układu odpornościowego, sugerując nowe podejścia do leków mających przywracać zdrową funkcję komórek T, zamiast jedynie tłumić stan zapalny. Choć przed wdrożeniem do praktyki potrzebne są większe badania i eksperymenty laboratoryjne, praca ta wytycza obiecującą drogę ku bardziej precyzyjnej, biologicznie ugruntowanej diagnostyce i terapii sepsy.
Cytowanie: Yang, K., Hu, Y., Ma, C. et al. Integrative analysis of transcriptome and single-cell sequencing combined with experimental validation identifies biomarkers associated with T cell and senescence in sepsis. Sci Rep 16, 7109 (2026). https://doi.org/10.1038/s41598-026-38559-8
Słowa kluczowe: markery sepsy, komórki T, immunosenescencja, sekwencjonowanie pojedynczych komórek, immunometabolizm