Clear Sky Science · pl
Badanie toksycznego mechanizmu wywołującego choroby neurodegeneracyjne przez cypermetryn za pomocą toksykologii sieciowej i dokowania molekularnego
Codzienne środki na insekty a starzejący się mózg
Od gospodarstw rolnych po domowe kuchnie insektycydy pomagają kontrolować szkodniki — jednak niektóre z tych substancji nie znikają natychmiast po użyciu. W tym badaniu analizowano cypermetryn, szeroko stosowany insektycyd, stawiając pytanie o realne znaczenie: czy długotrwała ekspozycja może cicho zwiększać ryzyko zaburzeń mózgu, takich jak choroba Alzheimera czy Parkinsona? Korzystając z zaawansowanych metod komputerowych, badacze mapują, jak ten związek może wchodzić w interakcje z organizmem i mózgiem, dostarczając wczesnego ostrzeżenia o zanieczyszczeniu, z którym wiele osób ma do czynienia nieświadomie.
Dlaczego komórek nerwowych trudno bronić
Choroby neurodegeneracyjne, w tym Alzheimer, Parkinson i inne postacie demencji, to schorzenia, w których komórki nerwowe w mózgu stopniowo obumierają i nie mogą zostać zastąpione. W miarę ich niewydolności ludzie tracą pamięć, zdolność myślenia i kontrolę ruchu. Równocześnie we współczesnym świecie rośnie stosowanie pestycydów, a kilka długoterminowych badań populacyjnych wykazało, że społeczności o intensywniejszym użyciu pestycydów mają wyższe wskaźniki tych chorób mózgu. Eksperymenty na zwierzętach i komórkach sugerują, że pyretroidy, takie jak cypermetryna, mogą uszkadzać komórki mózgu przez stres oksydacyjny (chemiczne „rdzewienie”) i długotrwałe zapalenie. Jednak do tej pory naukowcy nie mieli jasnego obrazu, jak konkretnie ten związek może łączyć się na poziomie molekularnym z ludzką neurodegeneracją.
Budowanie cyfrowej mapy szkodliwości chemicznej
Aby się tym zająć, zespół sięgnął po „toksykologię sieciową”, podejście big data łączące informacje z licznych baz biologicznych. Najpierw przewidzieli, które ludzkie białka cypermetryna mogłaby potencjalnie wiązać, porównując jej strukturę z tysiącami znanych związków. Następnie zgromadzili setki genów i białek już powiązanych z chorobami neurodegeneracyjnymi z głównych źródeł medycznych i genetycznych. Nakładając te dwie listy, odkryli 108 wspólnych celów — białek, które jednocześnie oddziałują z cypermetryną i są związane z degeneracją mózgu. Zbudowali następnie dużą mapę interakcji pokazującą, jak te białka komunikują się wewnątrz komórek, i użyli jej do wyróżnienia 19 „węzłowych” białek, które wydają się szczególnie centralne dla potencjalnych toksycznych efektów cypermetryny.
Kluczowe białka w centrum problemu
Kilka z najważniejszych węzłowych białek pełni dobrze znane funkcje dla zdrowia mózgu. Na przykład APOE pomaga zarządzać tłuszczami w mózgu i jest silnie związane z ryzykiem Alzheimera, podczas gdy A2M pomaga usuwać szkodliwe skupiska białkowe. Inne, takie jak AKT1 i SRC, znajdują się w istotnych szlakach sygnałowych kontrolujących przetrwanie lub śmierć komórkową. Badacze skupili się na trzech konkretnych białkach: CREBBP, które pomaga przełączać geny i wspiera tworzenie pamięci; GSK3B, enzym sygnałowy od dawna powiązany z nieprawidłowymi złogami białkowymi i zapaleniem; oraz ALB, główne białko krwi, które transportuje związki po organizmie i może przedostać się do mózgu, gdy bariera krew–mózg jest uszkodzona. W szczegółowych symulacjach „dokowania” komputerowego cypermetryna dopasowywała się ciasno w kieszeniach każdego z tych białek, co sugeruje, że realistycznie może się wiązać i modyfikować ich działanie.
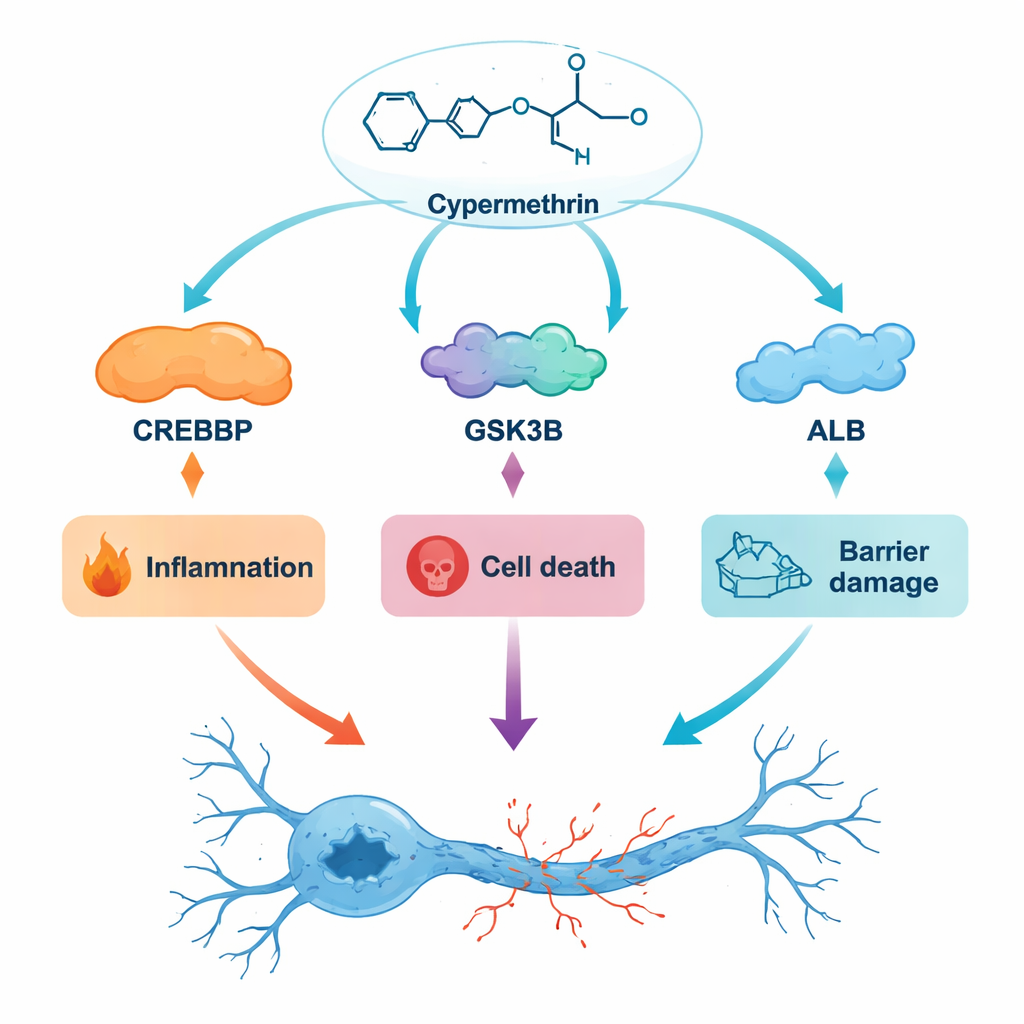
Symulowanie uszkodzeń na poziomie molekularnym
Aby sprawdzić, czy te dopasowania są stabilne czy tylko efemeryczne, zespół wykonał wirtualne „filmy” przedstawiające interakcję białek z cypermetryną przez 100 nanosekund, śledząc, jak bardzo struktury się chwiejają. We wszystkich trzech przypadkach kompleksy ustabilizowały się w trwałych kształtach, wspierając ideę, że cypermetryna może przylegać do tych białek wystarczająco długo, by mieć znaczenie biologiczne. Zaobserwowane wzorce zgadzają się z znanymi mechanizmami chorób: udział GSK3B wskazuje na zwiększone zapalenie i nieprawidłowe fałdowanie białek mózgowych; ingerencja w CREBBP mogłaby zaburzać programy genowe chroniące neurony; a silne wiązanie z ALB wspiera hipotezę, że cypermetryna może podróżować we krwi i wpływać na ilość związku docierającego do mózgu.
Co to oznacza dla ludzi i zdrowia publicznego
Mówiąc prosto, badanie sugeruje, że cypermetryna nie działa na jeden „wyłącznik” w mózgu, lecz raczej przesuwa całą sieć białek w stronę stresu, zapalenia i śmierci komórkowej — warunków sprzyjających rozwojowi chorób neurodegeneracyjnych. Praca nie dowodzi, że cypermetryna powoduje Alzheimera czy Parkinsona u ludzi, ponieważ opiera się na modelach komputerowych, a nie na badaniach klinicznych. Podkreśla jednak prawdopodobne biologiczne ścieżki, przez które codzienna ekspozycja na pestycydy mogłaby przyczyniać się do długotrwałego uszkodzenia mózgu, i identyfikuje konkretne białka, które przyszłe badania laboratoryjne i kliniczne mogą sprawdzić. Gdy regulatorzy i lekarze rozważają bezpieczeństwo powszechnie stosowanych insektycydów, ta sieciowa perspektywa dostarcza istotnych naukowych podstaw do ostrożniejszego użycia oraz opracowania wczesnych narzędzi diagnostycznych dla osób zagrożonych.
Cytowanie: Li, S., Ding, W., Yu, Y. et al. Exploring the toxic mechanism of cypermethrin-induced neurodegeneration diseases via network toxicology and molecular docking. Sci Rep 16, 7293 (2026). https://doi.org/10.1038/s41598-026-38547-y
Słowa kluczowe: cypermetryna, neurotoksyczność pestycydów, choroby neurodegeneracyjne, zapalenie mózgu, zanieczyszczenia środowiska