Clear Sky Science · pl
Adaptacje termoregulacyjne na zimno u myszy C3H/HeJ są niezależne od sygnalizacji ADRB3
Dlaczego myszy lubiące chłód mają znaczenie dla zdrowia ludzi
Utrzymanie ciepła może nie brzmieć jak nowatorski problem medyczny, ale to, jak organizm radzi sobie z zimnem, w dużej mierze determinuje sposób wykorzystania i spalania energii. W badaniu porównano dwa powszechne szczepy myszy laboratoryjnych i postawiono zaskakująco istotne pytanie: czy po wystawieniu na zimno włączają swoje wewnętrzne „piece” w taki sam sposób jak ludzie? Odpowiedź pomaga wyjaśnić, dlaczego niektóre leki przeciwotyłościowe skuteczne u myszy zawiodły u ludzi — i wskazuje na bardziej podobny do ludzkiego model myszy do badań nad metabolizmem.
Dwa rodzaje myszy, jedno chłodne wyzwanie
Naukowcy porównali standardowe myszy C57BL/6J, szeroko stosowane w badaniach metabolicznych, z rzadziej używanym szczepem C3H/HeJ. Obie grupy trzymano najpierw w temperaturze około 30 °C, przy której myszy praktycznie nie muszą wydatkować energii, aby pozostać ciepłe. Następnie zwierzęta stopniowo schładzano do 10 °C, a ich masę ciała, pobór pokarmu i zużycie energii dokładnie mierzono w zaawansowanych klatkach metabolicznych. Co ciekawe, oba szczepy miały niemal taki sam punkt „komfortu” dla minimalnego zużycia energii — około 29–30 °C — co oznacza, że zaczynały z podobnej bazy przed zetknięciem się z zimnem.
Gdy nadchodzi zimno, jeden szczep pracuje ciężej
Po spadku temperatury oba rodzaje myszy zwiększyły wydatkowanie energii, jak można było oczekiwać. Jednak myszy C3H spalały więcej energii niż C57, mimo podobnego spożycia pokarmu. Wyższe spalanie nie było tylko krótkotrwałą reakcją — utrzymywało się zarówno w pierwszych godzinach, jak i w kolejnych dniach ekspozycji na zimno. Mimo to myszy C3H ważyły mniej i miały ogólnie mniej brązowej tkanki tłuszczowej, co sugeruje, że ich istniejąca tkanka tłuszczowa pracowała intensywniej, zamiast znacznie się powiększać. Badania krwi również sugerowały, że myszy C3H mobilizowały więcej paliwa, takiego jak glicerol, aby zasilić zwiększoną produkcję ciepła.
Brązowa i biała tkanka tłuszczowa dołączają do zespołu grzewczego
Aby zobaczyć, co działo się wewnątrz organizmu, zespół zbadał brązową tkankę tłuszczową — klasyczną tkankę produkującą ciepło — oraz dwa rodzaje białej tkanki tłuszczowej. U myszy C3H zimno silnie zwiększyło aktywność genów związanych z termogenezą w brązowej tkance, a kluczowe białka wspierające spalanie paliwa i aktywność mitochondrialną były silniej aktywowane. Mikroskopia ujawniła zmiany strukturalne zgodne z bardziej aktywną tkanką. Biała tkanka tłuszczowa opowiadała podobną historię: w szczególności depozyt wokół jąder, zwykle oporny na przekształcenie w komórki produkujące ciepło, wykazał u myszy C3H wyraźną aktywację. To sugeruje, że u tych zwierząt nie tylko brązowa tkanka, lecz także tradycyjna „magazynująca” tkanka tłuszczowa może zostać zaangażowana do utrzymania ciepła.
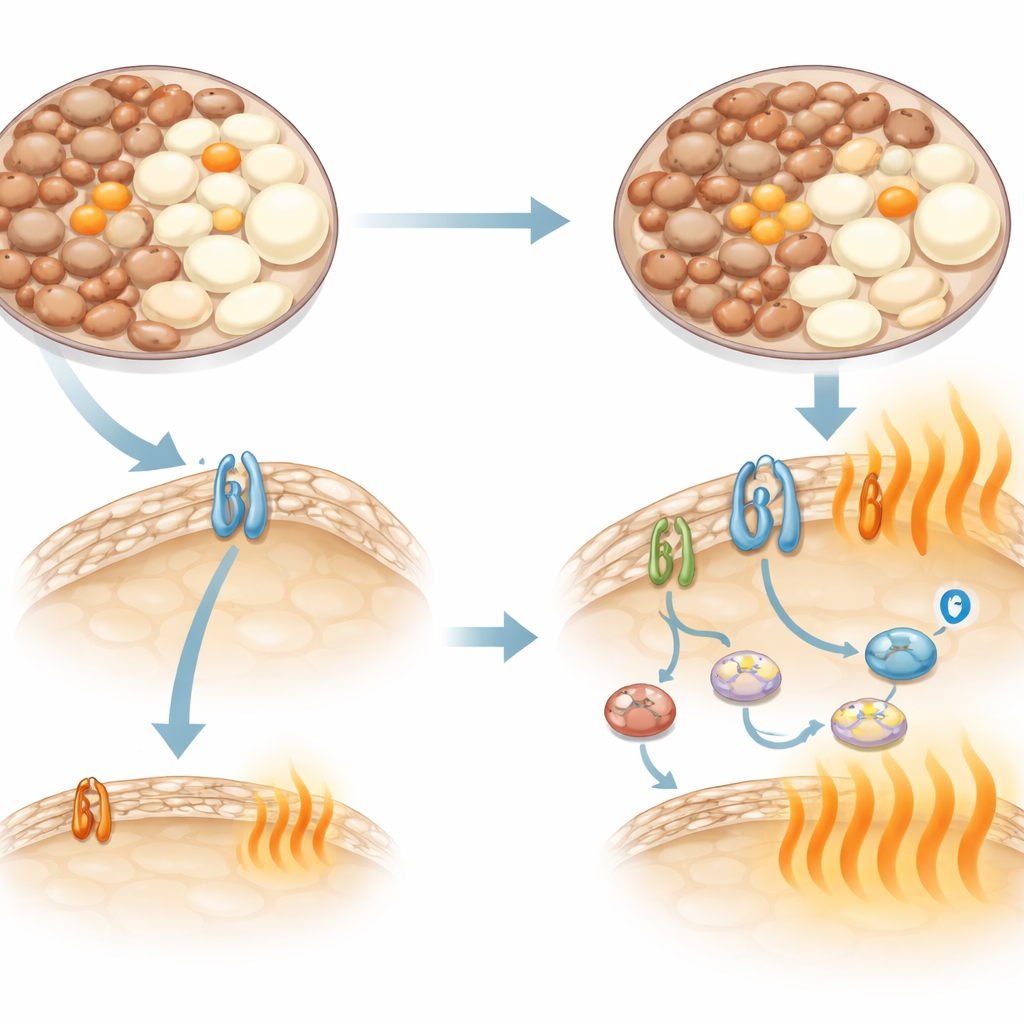
Inne okablowanie sygnałów nerwowych do tłuszczu
Produkcja ciepła w tkance tłuszczowej zwykle napędzana jest przez sygnały nerwowe działające przez receptor beta-adrenergiczny na komórkach tłuszczowych. U standardowych myszy C57 receptor beta-3 odgrywa ważną rolę, a leki go stymulujące mocno zwiększają wydatkowanie energii. Badacze to potwierdzili: selektywny związek celujący w beta-3 spowodował duży, utrzymujący się wzrost zużycia energii u myszy C57. Jednak u myszy C3H ten sam lek wywołał jedynie słaby, krótkotrwały efekt. Badania ekspresji genów wyjaśniły przyczynę — te myszy prawie nie eksprymowały receptora beta-3 w tkance tłuszczowej. Mimo to po podaniu noradrenaliny, naturalnego sygnału aktywującego kilka pokrewnych receptorów, myszy C3H nadal zwiększały wydatkowanie energii. Zablokowanie receptorów beta-1 i beta-2 w dużej mierze zlikwidowało różnice między szczepami, co wskazuje, że myszy C3H polegają na tych alternatywnych receptorach i innych nieklasycznych szlakach termogenezy zamiast na beta-3.
Co to oznacza dla badań nad metabolizmem człowieka
Ludzie, podobnie jak myszy C3H, w swojej brązowej tkance tłuszczowej opierają się w większym stopniu na receptorach beta-1 i beta-2, a nie na beta-3. To może tłumaczyć, dlaczego leki celujące w receptor beta-3 działały w typowych szczepach myszy, ale rozczarowały w badaniach klinicznych. Pokazując, że myszy C3H potrafią wywołać silną termogenezę po ekspozycji na zimno przy niemal braku sygnalizacji beta-3, badanie to uwydatnia je jako model bardziej zbliżony do ludzkiego do badania spalania energii przez tkankę tłuszczową. Wniosek dla czytelników jest taki, że nie wszystkie myszy są takie same: wybór odpowiedniego szczepu i właściwej temperatury hodowli może uczynić badania przedkliniczne znacznie bardziej relewantnymi dla zdrowia człowieka i przyszłych terapii otyłości oraz chorób metabolicznych.
Cytowanie: Beji, S., Mouchiroud, M., Gélinas, Y. et al. Thermoregulatory adaptations to cold in C3H/HeJ mice are independent of ADRB3 signaling. Sci Rep 16, 7859 (2026). https://doi.org/10.1038/s41598-026-38538-z
Słowa kluczowe: brązowa tkanka tłuszczowa, adaptacja do zimna, sygnalizacja adrenergiczna, modele mysie, wydatkowanie energii