Clear Sky Science · pl
Ukierunkowana inhibicja HDAC8 za pomocą nie‑hydroksamowych związków [1,2,4]triazolo[4,3-a]quinoliny
Nowa nadzieja dla dziecięcego nowotworu
Neuroblastoma to agresywny nowotwór wieku dziecięcego wywodzący się z komórek nerwowych, który bywa trudny do leczenia po rozsianiu. Badanie to analizuje nową strategię spowalniania lub zabijania komórek neuroblastomy poprzez wyłączenie kluczowego przełącznika komórkowego o nazwie HDAC8. Tworząc nową rodzinę związków o charakterze lekopodobnym, działających bardzo wybiórczo na ten przełącznik, badacze dążą do opracowania terapii bardziej skutecznych wobec guza i łagodniejszych dla reszty organizmu.
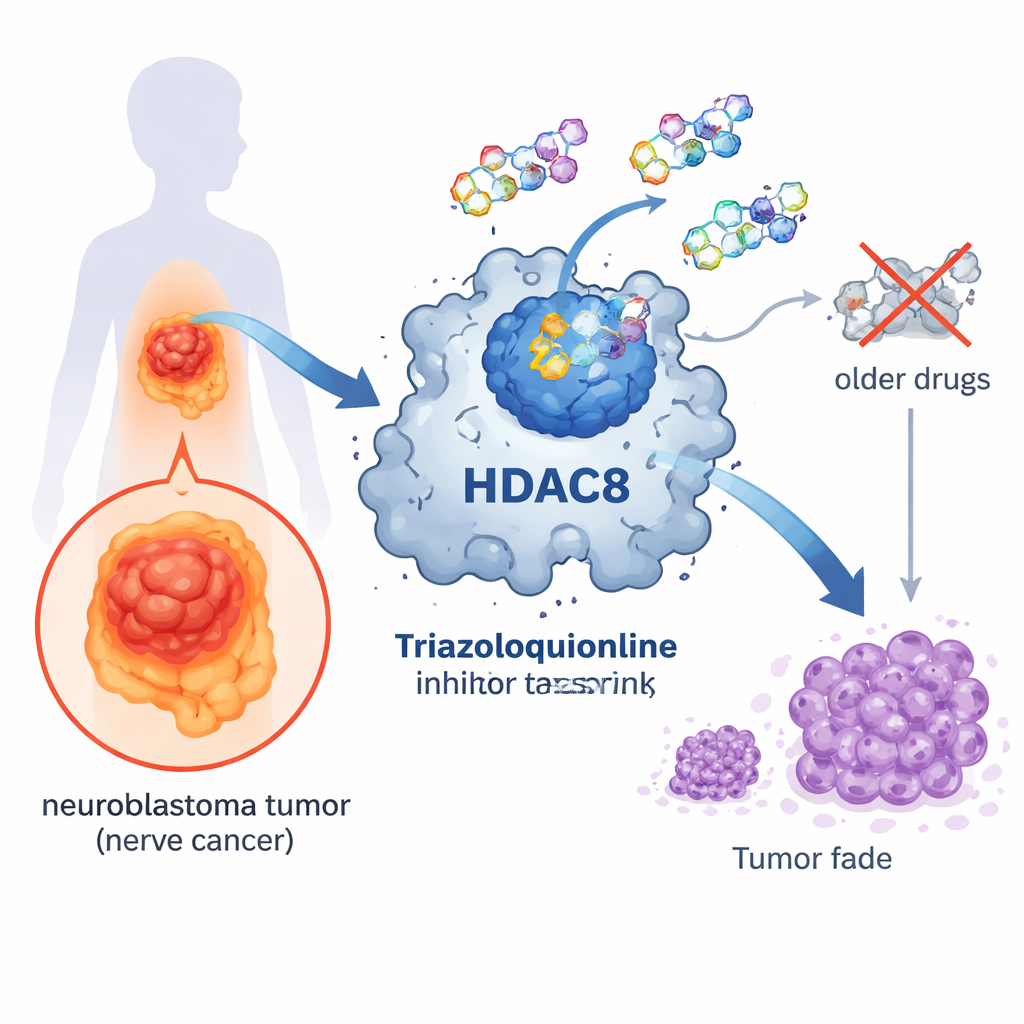
Molekularny przełącznik w centrum nowotworu
W naszych komórkach geny są nieustannie włączane i wyłączane. Jednym z ważnych mechanizmów kontroli są drobne chemiczne znaczniki zwane grupami acetylowymi, które przyłączają się do białek związanych z DNA. Enzymy zwane deacetylazami histonowymi (HDAC) usuwają te znaczniki, zagęszczając upakowanie DNA i zwykle zmniejszając aktywność genów. HDAC8 jest jednym z członków tej rodziny enzymów i powiązano go z kilkoma nowotworami, w tym z neuroblastomą. Gdy HDAC8 jest nadmiernie aktywny, komórki nowotworowe łatwiej się dzielą, przeżywają i rozsiewają, co czyni go atrakcyjnym celem dla nowych leków.
Ograniczenia starszych leków hamujących HDAC
Kilka leków blokujących HDAC jest już zatwierdzonych do leczenia niektórych nowotworów krwi, ale zwykle oddziałują na wiele typów HDAC jednocześnie. Większość tych leków wykorzystuje grupę hydroksamatu, która mocno wiąże jon metalu w centrum aktywnym enzymu. Choć skuteczna, grupa ta wiąże metale tak mocno, że może powodować skutki uboczne i utrudniać precyzyjne rozróżnianie między różnymi HDAC. W efekcie pacjenci mogą doświadczać toksyczności, a komórki zdrowe są uszkadzane razem z nowotworowymi. Badacze poszukują zatem alternatywnych rozwiązań chemicznych, które zachowają korzyści przeciwnowotworowe przy jednoczesnym ograniczeniu niepożądanych szkód.
Projektowanie nowej klasy ukierunkowanych inhibitorów
W tej pracy zespół zaprojektował i zsyntetyzował 21 nowych związków opartych na szkielecie triazoloquinoliny, połączonych za pomocą elastycznego łącznika z regionem „α‑aminowego amidu”, który może wiązać atom cynku w centrum aktywnym HDAC8. Wykorzystując projektowanie wspomagane komputerowo, wybrali tę architekturę, aby dopasować ją do wąskiego „kanału uwalniania octanu” unikalnego dla HDAC8 — cechy strukturalnej sprzyjającej wysokiej swoistości. Szczegółowe badania dokowania i symulacje dynamiki molekularnej wykazały, że kilka nowych cząsteczek — w szczególności oznaczonych jako 9m i 9r — tworzy stabilne, długotrwałe interakcje w kieszeni HDAC8 i wiąże się równie silnie, a nawet silniej niż dobrze znany inhibitor referencyjny. Co ważne, testy biochemiczne potwierdziły, że najlepsze związki silnie blokują HDAC8, pozostawiając inne członki rodziny HDAC w dużej mierze nietknięte.
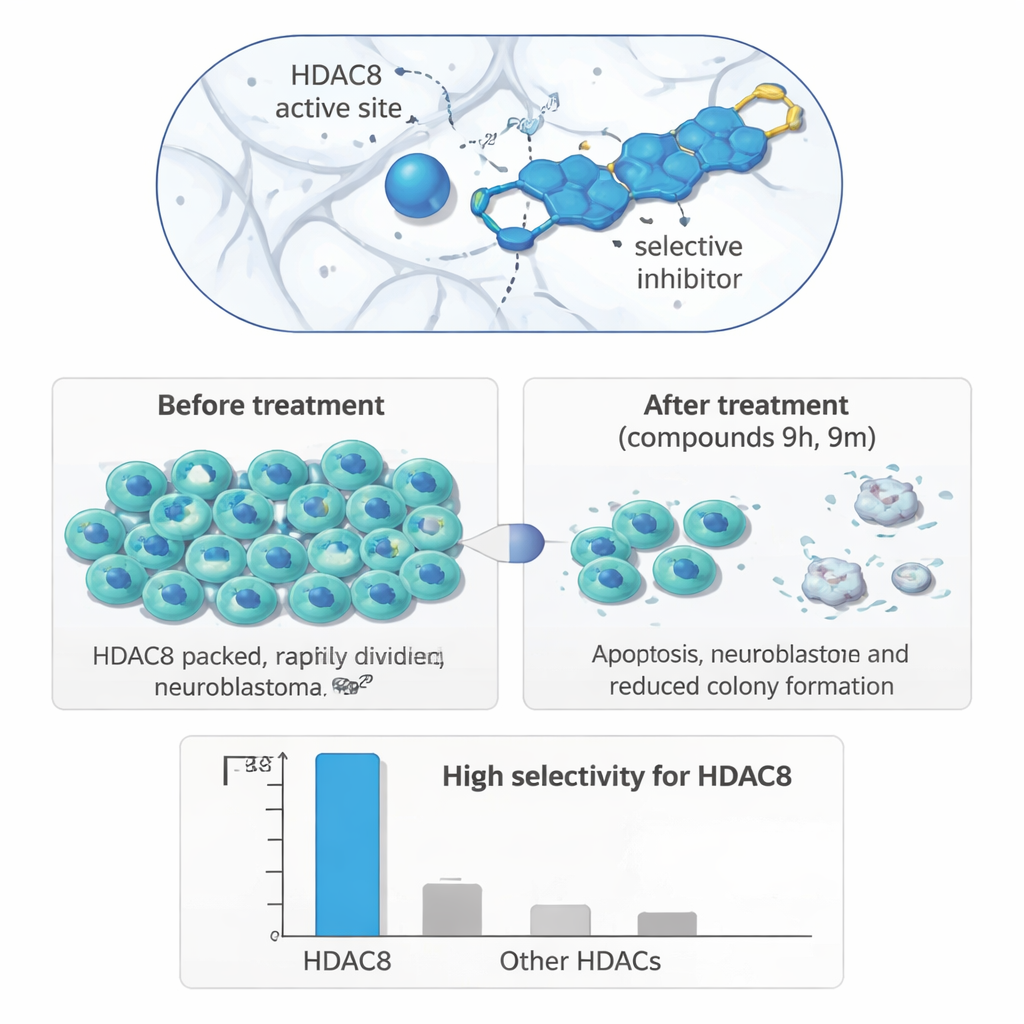
Od probówki do komórek nowotworowych
Aby sprawdzić, czy to precyzyjne celowanie enzymu przekłada się na użyteczne efekty biologiczne, badacze przetestowali swoje związki na panelu ludzkich linii komórkowych. W komórkach neuroblastomy (IMR‑32) wyróżniły się dwie cząsteczki, 9h i 9m: ograniczały wzrost komórek w stężeniach mikromolowych i działały silniej w neuroblastomie niż w komórkach raka piersi czy jelita grubego, a także niż w nie‑nowotworowych komórkach nerkowych. Długoterminowe eksperymenty formowania kolonii wykazały, że leczone komórki neuroblastomy utraciły dużą część zdolności do ponownego wzrostu po ekspozycji na związek. W teście gojenia się rany, śledzącym, jak szybko komórki przemieszczają się, aby zamknąć zadrapanie w warstwie komórkowej, oba związki spowolniły ruch komórek neuroblastomy, co sugeruje zmniejszone możliwości przerzutowania.
Zgłębianie mechanizmu zabijania komórek nowotworowych
Eksperymenty cytometrii przepływowej ujawniły, że 9h i 9m wywołują zaprogramowaną śmierć komórki (apoptozę) w komórkach neuroblastomy i powodują nagromadzenie komórek w fazie cyklu komórkowego związanej z uszkodzeniem DNA lub śmiercią (Sub‑G1). Aby potwierdzić, że efekty te rzeczywiście wynikają z blokady HDAC8, zespół zmierzył stopień acetylacji białka SMC3, znanego celu HDAC8 zaangażowanego w utrzymanie siostrzanych chromatyd razem podczas podziału komórki. Gdy HDAC8 jest zahamowany, acetylowane SMC3 się kumuluje. Po leczeniu 9h lub 9m poziomy acetylowanego SMC3 znacząco wzrosły, podczas gdy całkowita ilość białka SMC3 pozostała niezmieniona — mocny dowód, że związki te bezpośrednio oddziałują na HDAC8 w żywych komórkach i zakłócają jego normalną funkcję w kontroli chromosomów.
Co to może oznaczać dla przyszłych terapii
Podsumowując, chemia, modelowanie komputerowe, testy enzymatyczne i eksperymenty na komórkach tworzą spójny obraz: nowo opracowane związki triazoloquinolinowe są silnymi, wysoce selektywnymi blokerami HDAC8, które mogą zahamować wzrost i rozprzestrzenianie się komórek neuroblastomy przy jednoczesnym oszczędzaniu innych enzymów HDAC. Dzięki unikaniu konwencjonalnej grupy hydroksamatu mogą oferować bezpieczniejszą drogę wykorzystania HDAC8 jako celu terapeutycznego. Choć pozostało wiele pracy — zwłaszcza badania na zwierzętach i ostateczne próby kliniczne — badania te stanowią solidną podstawę do opracowania bardziej precyzyjnych leków przeciwko dziecięcej neuroblastomie i być może innym chorobom napędzanym przez HDAC8.
Cytowanie: Bandaru, N.V.M.R., Fathima, A., Sengar, S. et al. Targeted HDAC8 inhibition with non-hydroxamate [1,2,4]triazolo[4,3-a] quinoline compounds. Sci Rep 16, 7472 (2026). https://doi.org/10.1038/s41598-026-38490-y
Słowa kluczowe: inhibitory HDAC8, neuroblastoma, terapia epigenetyczna, triazoloquinolina, ukierunkowane leki przeciwnowotworowe