Clear Sky Science · pl
Prądy zależne od GluN2A i sygnał wapniowy w neuronach pochodzących z ludzkich komórek iPSC
Dlaczego drobne, hodowane w laboratorium komórki mózgowe mają znaczenie
Naukowcy coraz częściej wykorzystują hodowane w laboratorium ludzkie komórki mózgowe, by badać rozwój mózgu i sprawdzać, co idzie nie tak w zaburzeniach takich jak autyzm, padaczka czy choroba Alzheimera. To badanie stawia proste, ale kluczowe pytanie: czy te sztucznie wytworzone neurony dojrzewają i łączą się w sposób rzeczywiście przypominający ludzki mózg, zwłaszcza jeśli chodzi o obsługę ważnego sygnału chemicznego — glutaminianu? Odpowiedź wskazuje, jak tworzyć bardziej realistyczne modele „mini-mózgów” oraz sugeruje nowe drogi badania zdrowia i chorób mózgu.
Budowanie neuronów z przeprogramowanych komórek
Badacze zaczęli od ludzkich indukowanych pluripotencjalnych komórek macierzystych — zwykłych komórek przeprogramowanych z powrotem do stanu komórek macierzystych. Następnie ukierunkowali je do postaci prekursorów neuronów, a ostatecznie do sieci neuronów i wspierających astrocytów, naśladując rozwijającą się korę mózgową człowieka. Porównali dwa powszechnie stosowane protokoły hodowli, czyli warunki kultury. Pierwszy, zwany medium BrainPhys, został zaprojektowany tak, by sprzyjać aktywnym, elektrycznie reagującym neuronom i zwykle generuje więcej astrocytów. Drugi, bardziej tradycyjne medium do utrzymania neuronów, promuje neurony przy mniejszej liczbie astrocytów. W ciągu sześćdziesięciu dni zespół śledził zmiany w wyglądzie, aktywności genów i składzie komórkowym kultur, stwierdzając, że hodowle w BrainPhys rozwijały bardziej rozbudowaną morfologię neuronów i stosunek neuronów do astrocytów bliższy temu w rzeczywistym ludzkim mózgu.
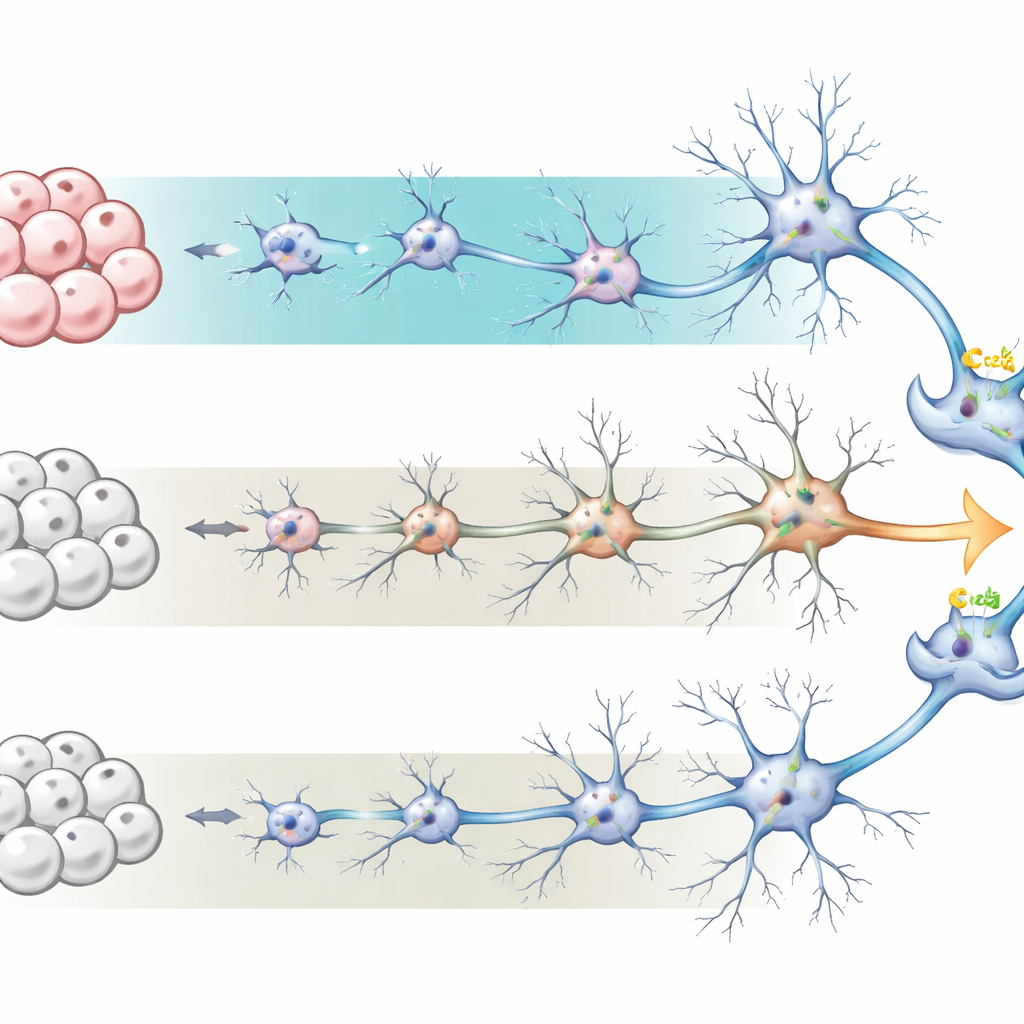
Znaki, że komórki dojrzewają
Aby ocenić, jak „dojrzałe” są neurony, zespół zmierzył globalną aktywność genów za pomocą sekwencjonowania RNA w 60. dniu. Komórki hodowane w BrainPhys wykazywały prawie dwa tysiące genów o zmienionym poziomie ekspresji w porównaniu z medium standardowym, z wieloma powiązanymi z różnicowaniem neuronów, tworzeniem synaps i aktywnością elektryczną. Geny związane z funkcją astrocytów i zapaleniem także były podwyższone, co odzwierciedla większą populację astrocytów. Razem te wzorce sugerują, że kultury w BrainPhys lepiej odtwarzają późniejsze etapy rozwoju mózgu, z bardziej wyspecjalizowanymi punktami komunikacji między neuronami i środowiskiem wspierającym bardziej przypominającym tkankę żywą.
Kluczowe przełączniki w komunikacji chemicznej
Znak dojrzewania mózgu to zmiana składu receptorów NMDA — molekularnych bramek na neuronach, które otwierają się w odpowiedzi na glutaminian i pomagają ustawić połączenia związane z uczeniem się. We wczesnym rozwoju dominuje podjednostka o nazwie GluN2B; później pojawia się GluN2A, co zmienia czas trwania i siłę otwarcia receptorów. Za pomocą mikroskopii zespół pokazał, że z upływem czasu coraz więcej receptorów NMDA przesuwa się do synaps, punktów kontaktu między neuronami, szczególnie w kulturach BrainPhys. Ukierunkowane pomiary genów ujawniły spadek „wczesnej” podjednostki GluN2B i wzrost „późniejszej” GluN2A, co wskazuje, że neurony przechodzą ten klasyczny przełącznik rozwojowy.
Śledzenie prądów i wapnia wewnątrz komórek
Testy funkcjonalne potwierdziły, że te zmiany molekularne mają znaczenie. Przy użyciu elektrody o cienkim końcu badacze rejestrowali prądy elektryczne wywołane NMDA, substancją selektywnie aktywującą receptory NMDA. Neurony z obu metod hodowli wykazywały silne prądy, ale zablokowanie podjednostki GluN2A zmniejszało te prądy około o połowę, demonstrując, że GluN2A stała się teraz głównym uczestnikiem przepływu sygnału. Zespół następnie śledził wapń, kluczowy wewnętrzny przekaźnik, używając fluorescencyjnego barwnika. Po ekspozycji na NMDA znacznie większy odsetek neuronów hodowanych w BrainPhys wykazywał silne skoki wapniowe, a amplituda sygnału była większa. Analiza genów sugerowała powód: kultury BrainPhys zwiększały ekspresję wielu składników kanałów wapniowych i dróg uwalniania, wyposażając komórki do przekształcania aktywacji receptorów NMDA w szerokie, skoordynowane sygnały wapniowe.
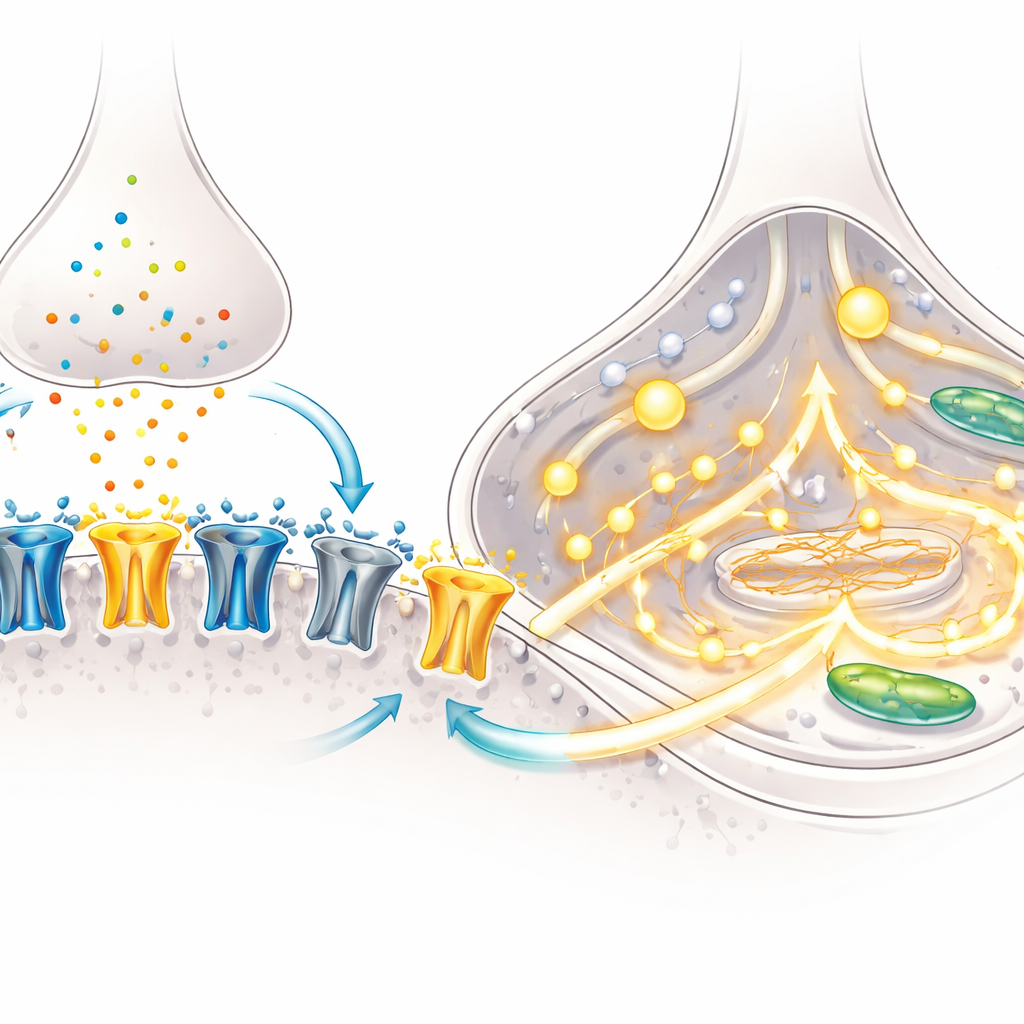
Co to oznacza dla badań nad zaburzeniami mózgu
Razem wyniki pokazują, że neurony pochodzące z ludzkich komórek macierzystych mogą osiągnąć funkcjonalnie dojrzały stan w zaledwie dwa miesiące, szczególnie jeśli są hodowane w warunkach sprzyjających aktywnym sieciom i realistycznemu stosunkowi neuronów do astrocytów. W tym stanie „dorosłopodobna” podjednostka GluN2A dominuje w prądach receptorów NMDA i silnie przyczynia się do sygnalizacji wapniowej, podobnie jak w rozwijającym się mózgu człowieka. Dla osób spoza specjalności wniosek jest taki, że badacze dysponują teraz wierniejszym modelem laboratoryjnym tego, jak ludzkie neurony pobudzeniowe dojrzewają, łączą się i reagują na glutaminian. Umożliwia to badanie, jak subtelne zmiany genetyczne lub procesy chorobowe zakłócają te precyzyjnie wyregulowane przełączniki, otwierając okno na schorzenia od padaczki po chorobę Alzheimera i wspierając projektowanie oraz testowanie przyszłych terapii.
Cytowanie: Escamilla, S., Avilés-Granados, C., Peralta, F.A. et al. GluN2A-mediated currents and calcium signal in human iPSC-derived neurons. Sci Rep 16, 9736 (2026). https://doi.org/10.1038/s41598-026-38482-y
Słowa kluczowe: receptory NMDA, neurony z komórek macierzystych, rozwój mózgu, sygnalizacja wapniowa, dojrzewanie synaptyczne