Clear Sky Science · pl
Podwójny inhibitor G9a i antagonistyczny receptor histaminowy H3 A-366 poprawia zachowania repetetywne i społeczne oraz łagodzi neurozapaleniem u myszy BTBR T + tf/J
Dlaczego to badanie na myszach ma znaczenie dla autyzmu
Rodziny żyjące z zaburzeniami ze spektrum autyzmu (ASD) często zmagają się z mozaiką terapii, które łagodzą jedynie pojedyncze objawy. W tym badaniu zbadano nowy eksperymentalny związek, zwany A-366, zaprojektowany tak, by działać jednocześnie na dwa bardzo różne układy biologiczne. W powszechnie używanym modelu myszy wykazującym zachowania przypominające autyzm, A-366 zmniejszał zachowania repetetywne, poprawiał interakcje społeczne i uspokajał zapalenie mózgu, sugerując możliwość przyszłości, w której jeden lek mógłby jednocześnie przeciwdziałać kilku podstawowym cechom ASD.
Stan o wielu składowych
ASD nie jest jedną chorobą o jednej przyczynie. Obejmuje trudności w komunikacji społecznej, zachowania repetetywne i często inne problemy, takie jak lęk czy zaburzenia uwagi. Za tymi zewnętrznymi objawami kryje się splot zmian w chemii mózgu i regulacji genów. Obecne leki, jak przeciwpsychotyczny aripiprazol, głównie oddziałują na układy przekaźników mózgowych, takie jak dopamina i serotonina, i są zatwierdzone jedynie dla objawów towarzyszących, np. drażliwości. Równocześnie badania ujawniły, że sposób, w jaki DNA jest pakowane i chemicznie znakowane wewnątrz komórek mózgu — epigenetyka — również zmienia się w ASD, podobnie jak aktywność własnych odpowiedzi immunologicznych i zapalnych mózgu. Te wielowarstwowe zmiany sugerują, że podejście „jeden cel na raz” może być zbyt wąskie.
Uderzając jednocześnie w przełączniki genowe i przekaźniki mózgowe
A-366 został pierwotnie opracowany, by blokować białko zwane G9a, enzym dodający chemiczne znaczniki do białek histonowych, co zwykle prowadzi do wyciszania genów. W kilku zaburzeniach mózgowych aktywność G9a i jego znaczniki są zwiększone, potencjalnie wyciszając geny istotne dla uczenia się, pamięci i prawidłowego okablowania mózgu. Co ciekawe, kształt chemiczny A-366 przypomina także leki blokujące receptor histaminowy H3, przełącznik kontrolujący uwalnianie histaminy i innych przekaźników, powiązany z uwagą, pobudzeniem i zachowaniami społecznymi. Z powodu tego nakładania się autorzy przypuszczali, że A-366 może działać jako „podwójny środek”: rozluźniając szkodliwe wyciszanie genów przez hamowanie G9a, a jednocześnie wzmacniając sygnalizację histaminową przez blokadę receptorów H3.
Testowanie A-366 na myszach o cechach autystycznych
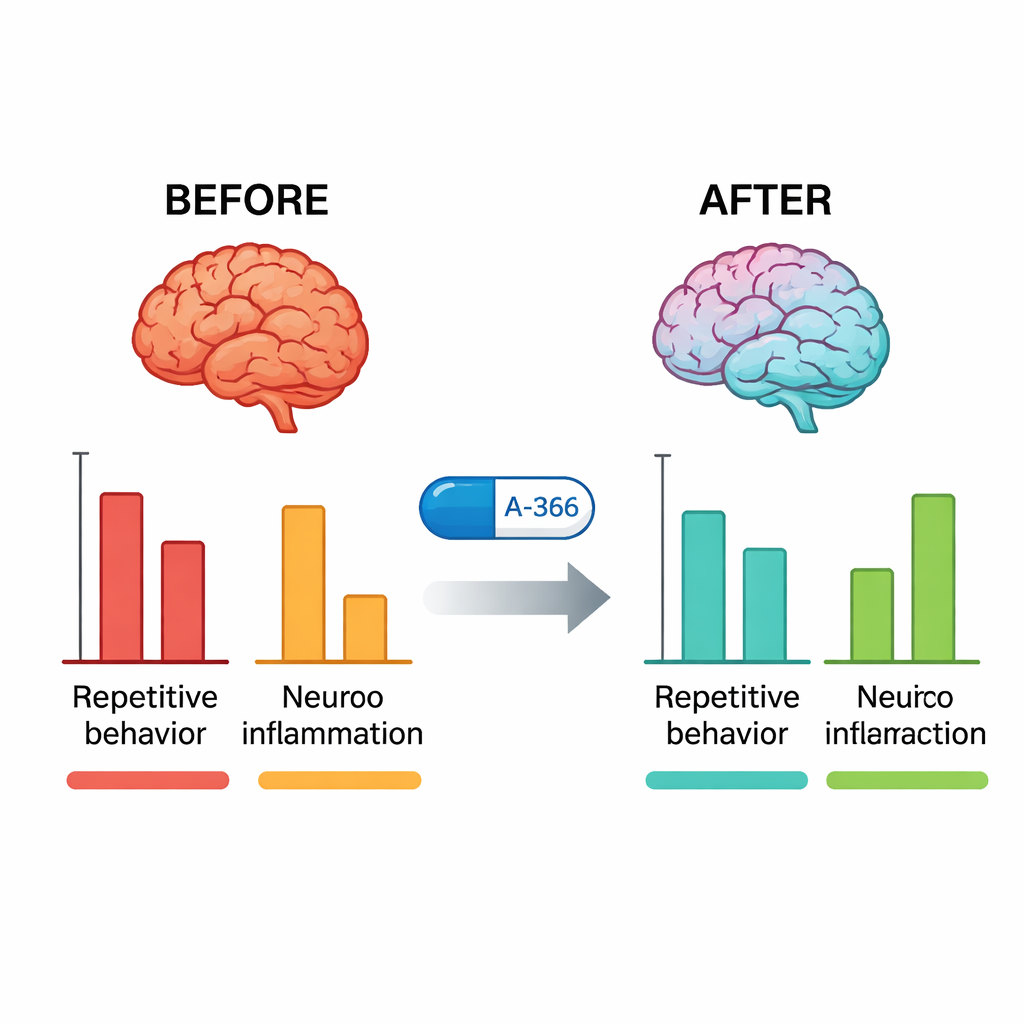
Zespół pracował na myszach BTBR T+tf/J, szczepie, który naturalnie wykazuje niską towarzyskość, silne repetetywne czyszczenie i kopanie oraz podwyższone zapalenie mózgu — cechy przypominające kluczowe aspekty ASD. Samce BTBR otrzymywały codzienne zastrzyki A-366 przez trzy tygodnie w trzech różnych dawkach, a ich zachowanie porównywano z typowymi myszami C57 oraz z myszami BTBR leczonymi pitolisantem (standardowy bloker receptora H3) lub aripiprazolem. W kilku zadaniach A-366 zmniejszał kopanie, drapanie i samoczynne czyszczenie w sposób zależny od dawki oraz poprawiał wyniki w teście labiryntu Y oceniającym pamięć roboczą przestrzenną. W teście społecznym w trzech komorach A-366 nie tylko przywrócił preferencję mysz za spędzaniem czasu z inną myszą zamiast pustej klatki, ale przy najwyższej dawce podniósł wyniki społeczne do poziomu myszy typowych i przewyższył efekty pitolisantu i aripiprazolu.
Tłumienie zapalenia i potwierdzenie celów
Po testach behawioralnych badacze przebadali mózgi myszy. U nieleczonych myszy BTBR aktywność G9a w hipokampie i móżdżku była wyraźnie wyższa niż u myszy typowych. Leczenie A-366 ostro zmniejszyło tę aktywność z powrotem w kierunku normy, podczas gdy sam pitolisant tego nie zrobił, potwierdzając, że A-366 rzeczywiście angażuje swój epigenetyczny cel. Równocześnie kluczowe molekuły zapalne — TNF-α, IL-6 i IL-1β — były znacznie podwyższone u myszy BTBR i znacząco obniżone przez A-366, bardziej niż przez aripiprazol. Gdy naukowcy dodali lek aktywujący receptory H3 (RAMH) do terapii A-366, korzyści behawioralne i przeciwzapalne zostały tylko częściowo odwrócone, a spadek aktywności G9a pozostał. Ten wzorzec wspiera mechanizm złożony: trwałe złagodzenie epigenetyczne poprzez hamowanie G9a oraz wkład pośredni związany z histaminą przez blokadę receptorów H3.
Co to może oznaczać dla przyszłych terapii
Dla osoby niezajmującej się specjalistycznie te wyniki sugerują, że możliwe jest zaprojektowanie leków działających jednocześnie na „oprogramowanie” i „system przekazu” mózgu. W tym modelu myszy o zachowaniach przypominających autyzm A-366 złagodził zachowania repetetywne, poprawił zaangażowanie społeczne i zmniejszył oznaki przewlekłego zapalenia mózgu poprzez jednoczesne rozluźnienie szkodliwego wyciszania genów i dostrojenie sygnalizacji histaminowej. Sam A-366 został opracowany z myślą o innych chorobach i wymagałby optymalizacji oraz rozległych badań bezpieczeństwa przed ewentualnym zastosowaniem u ludzi. Mimo to dostarcza planu działania dla nowej klasy leków wielocelowych ukierunkowanych na złożoną biologię ASD, gdzie adresowanie tylko jednej ścieżki na raz jak dotąd dawało ograniczoną ulgę.
Cytowanie: Hajar, M., Jayaprakash, P., Stark, H. et al. The dual G9a inhibitor and histamine H3 receptor antagonist A-366 improves repetitive and social behaviors and attenuates neuroinflammation in BTBR T + tf/J mice. Sci Rep 16, 7105 (2026). https://doi.org/10.1038/s41598-026-38481-z
Słowa kluczowe: zaburzenia ze spektrum autyzmu, terapia epigenetyczna, receptor histaminowy H3, neurozapalenie, model myszy