Clear Sky Science · pl
aFGF ratuje fibroblasty postarzałe przez wysoki poziom glukozy i poprawia gojenie ran cukrzycowych poprzez regulację szlaku SIRT1/STAT3
Dlaczego rany gojące się powoli mają znaczenie
Dla wielu osób z cukrzycą drobne skaleczenie na stopie lub nodze może przekształcić się w uporczywą ranę utrzymującą się miesiącami, czasem prowadzącą do zakażenia lub nawet amputacji. Te przewlekłe owrzodzenia to nie tylko problem powierzchniowy: komórki skóry, które powinny odbudować uszkodzony tkankę, często starzeją się przedwcześnie i przestają prawidłowo funkcjonować. Badanie to opisuje obiecujący sposób „odmłodzenia” części tych komórek przy użyciu naturalnego sygnału naprawczego, z nadzieją na szybsze i bardziej pełne zamykanie ran cukrzycowych.
Komórki, które starzeją się zbyt wcześnie
Zdrowa skóra opiera się na fibroblastach — komórkach podporowych znajdujących się w głębszych warstwach skóry — które mnożą się, przemieszczają do rany i tworzą nową „rusztowanie” dla regenerującej się tkanki. W cukrzycy długotrwały wysoki poziom glukozy i produkty glikacji uszkadzające białka skłaniają fibroblasty do wejścia w stan zwany starzeniem komórkowym lub senescencją. Fibroblasty senescentne słabiej się dzielą, wytwarzają mniej białek strukturalnych potrzebnych do naprawy i zamiast tego uwalniają koktajl czynników sprzyjających stanowi zapalnemu. Autorzy wykazali, że u szczurów cukrzycowych skóra wokół rany zawiera więcej takich postarzałych fibroblastów i mniej korzystnych białek macierzy, co koreluje ze znacznie wolniejszym gojeniem.
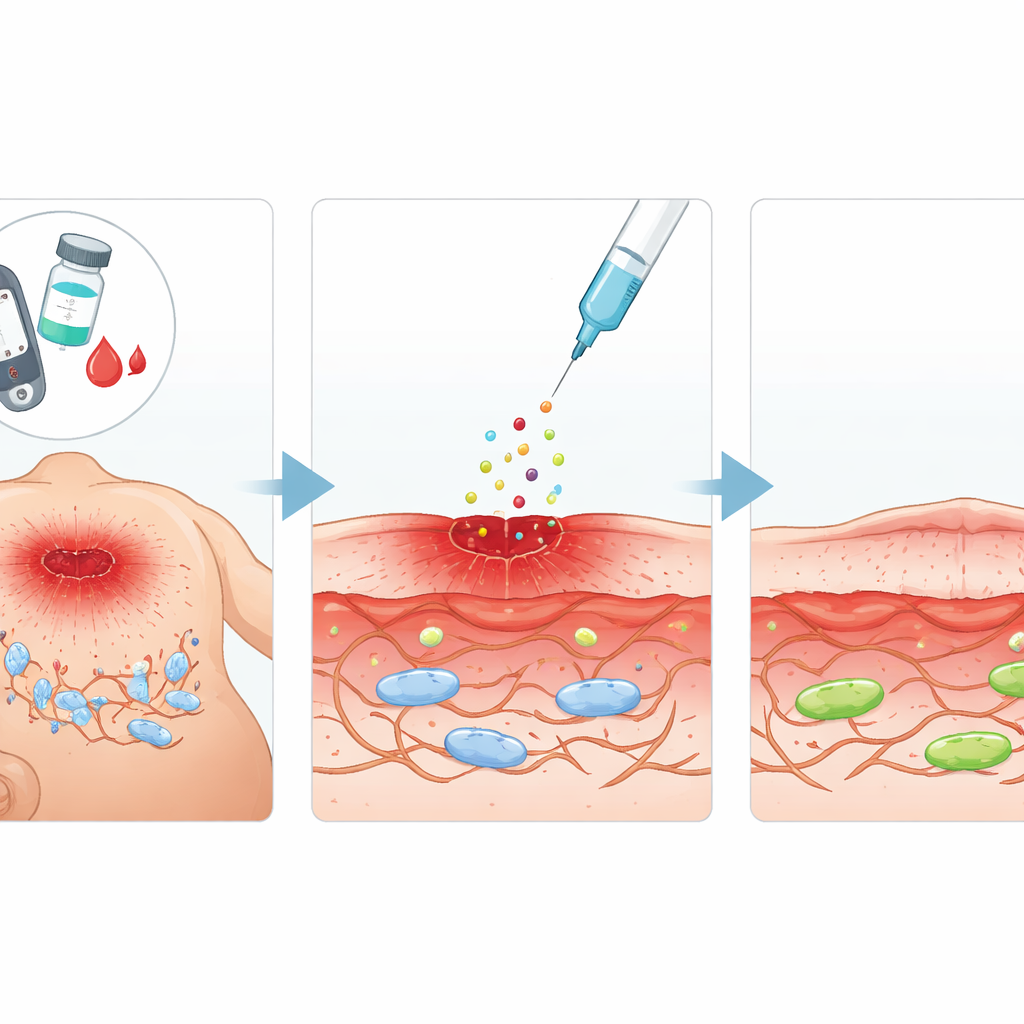
Sygnal naprawczy z potencjałem
Zespół skupił się na kwaśnym czynniku wzrostu fibroblastów (aFGF), naturalnie występującym białku znanym z pobudzania wzrostu komórek i naprawy tkanek. Zastanawiali się, czy aFGF może nie tylko zwiększyć aktywność fibroblastów, ale też odwrócić zmiany przypominające starzenie wywołane przez wysoką glukozę. U szczurów cukrzycowych wykonali standardowe rany skórne i wstrzykiwali aFGF wokół uszkodzonego obszaru co kilka dni. W porównaniu ze zwierzętami cukrzycowymi bez leczenia, szczury leczone aFGF wykazywały szybsze kurczenie się powierzchni rany, lepszą odbudowę tkanki podstawowej i niższe poziomy markerów sygnalizujących starzenie komórkowe. W równoległych eksperymentach na linii fibroblastów mysich wystawionych na bardzo wysoką glukozę, aFGF przywracał komórkom zdolność do dzielenia się i migracji — dwa zachowania niezbędne do zamknięcia rany.
Łagodzenie stresu oksydacyjnego wewnątrz komórek
Wysoki poziom cukru we krwi robi więcej niż tylko dostarcza komórkom dodatkowego paliwa: prowadzi też do nadprodukcji reaktywnych form tlenu, niestabilnych cząsteczek uszkadzających białka, tłuszcze i DNA. Ten stres oksydacyjny jest ważnym czynnikiem wywołującym senescencję fibroblastów. Badacze zmierzyli w modelu komórkowym kilka standardowych wskaźników tego stresu, w tym produkty uszkodzeń i aktywność przeciwutleniających enzymów komórkowych. Przy wysokiej glukozie fibroblasty wykazywały więcej uszkodzeń i słabsze mechanizmy obronne. Po dodaniu aFGF równowaga uległa przesunięciu: wskaźniki szkodliwych procesów spadły, a aktywność enzymów ochronnych wzrosła. To sugeruje, że aFGF pomaga przywrócić zdrowsze środowisko wewnątrzkomórkowe, przez co fibroblasty są mniej podatne na przejście w trwały stan postarzenia.
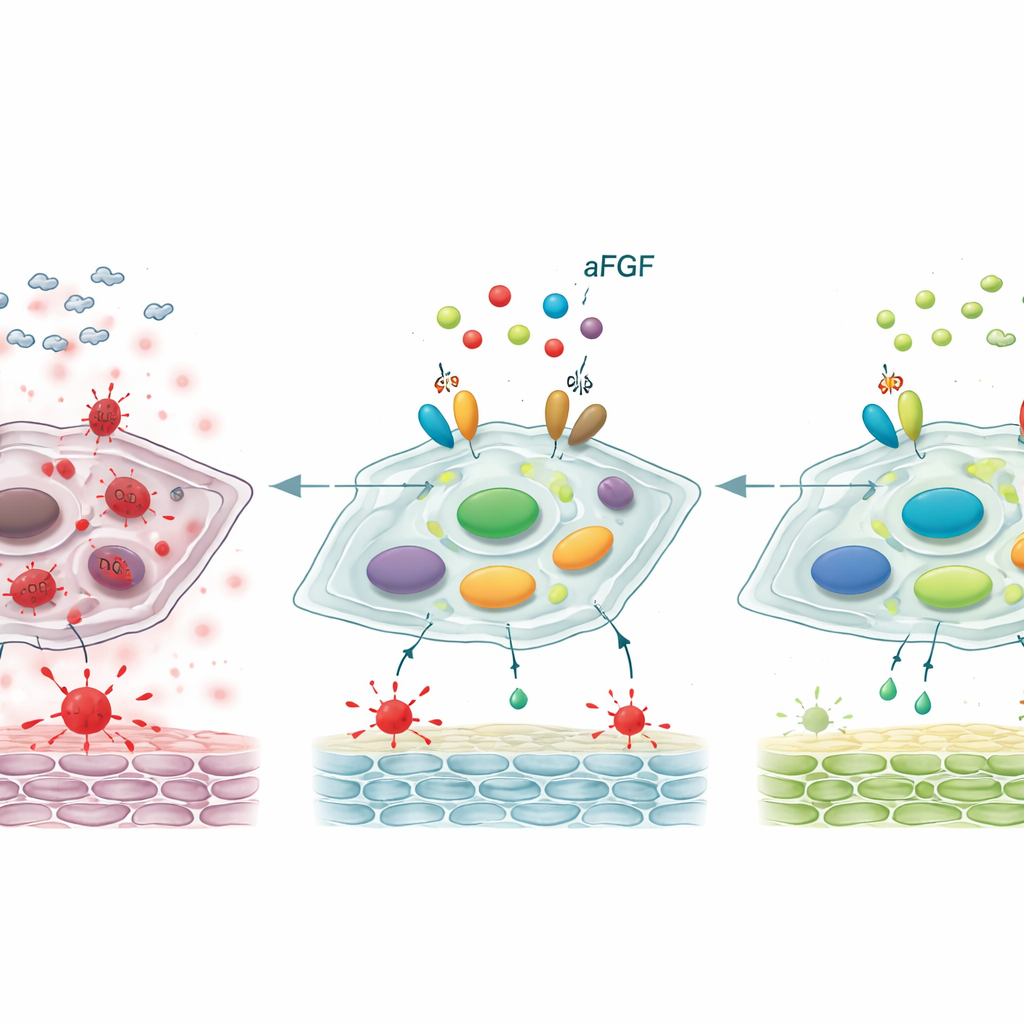
Resetowanie kluczowego przełącznika kontrolnego
Badając mechanizmy głębiej, naukowcy przeanalizowali molekularną oś kontrolną obejmującą dwa białka, SIRT1 i STAT3, które razem wpływają na to, czy fibroblasty pozostaną młode, czy przejdą w senescencję. W ranach cukrzycowych i w komórkach traktowanych wysoką glukozą poziomy SIRT1 — strażnika związanego z odpornością na stres — były obniżone, podczas gdy aktywna forma STAT3 — czynnik sprzyjający starzeniu i zachowaniom zapalnym — była podwyższona. Leczenie aFGF odwróciło ten wzorzec: SIRT1 wzrósł, a aktywowany STAT3 spadł. Gdy zespół zablokował SIRT1 specyficznym inhibitorem, aFGF w dużej mierze stracił zdolność do zmniejszania stresu oksydacyjnego, tłumienia markerów starzenia i przyspieszania zamykania ran u szczurów. Wskazuje to, że korzystne efekty aFGF zależą w dużej mierze od „przebudzenia” SIRT1, który z kolei hamuje STAT3 i szkodliwy program starzenia przez niego kontrolowany.
Co to może znaczyć dla pacjentów
Podsumowując, wyniki sugerują, że aFGF robi więcej niż tylko pobudza komórki do wzrostu. Wygląda na to, że ratuje przeciążone fibroblasty w ranach cukrzycowych z destrukcyjnego cyklu starzenia, łagodząc stres oksydacyjny i resetując kluczowy przełącznik molekularny, dzięki czemu te komórki mogą ponownie uczestniczyć w odbudowie tkanki. Chociaż prace przeprowadzono na szczurach i komórkach hodowlanych, a rzeczywiste rany cukrzycowe są jeszcze bardziej złożone niż zastosowane modele, wyniki wskazują na aFGF jako obiecującego kandydata do przyszłych terapii. Jeśli podobne korzyści potwierdzą się u ludzi, celowana terapia aFGF mogłaby pewnego dnia pomóc przewlekłym owrzodzeniom cukrzycowym szybciej się goić, zmniejszając ból, ryzyko infekcji i szansę na poważne powikłania.
Cytowanie: Wang, X., Lu, M., Jia, S. et al. aFGF rescues high glucose-induced senescent fibroblasts and improves diabetic wound healing by regulating SIRT1/STAT3 pathway. Sci Rep 16, 7856 (2026). https://doi.org/10.1038/s41598-026-38480-0
Słowa kluczowe: gojenie ran cukrzycowych, starzenie się fibroblastów, stres oksydacyjny, terapia czynnikami wzrostu, szlak SIRT1 STAT3