Clear Sky Science · pl
Odkrycie in silico wielofunkcyjnego inhibitora pochodzenia naturalnego do terapii choroby Huntingtona
Nowe spojrzenie na wyniszczającą chorobę mózgu
Choroba Huntingtona to rzadka, lecz wyniszczająca choroba mózgu, która stopniowo pozbawia ludzi sprawności ruchowej, zdolności myślenia i niezależności. Dostępne dziś leki mogą złagodzić niektóre objawy, ale nie zatrzymują ani nie odwracają przebiegu choroby. W tym badaniu zbadano nowe, komputerowe podejście do poszukiwania terapii, szukając pojedynczego związku naturalnego, który jednocześnie uderza w kilka newralgicznych miejsc procesu chorobowego — podejście, które może być skuteczniejsze niż leki ukierunkowane na pojedynczy cel.
Dlaczego choroba Huntingtona jest tak trudna do leczenia
Choroba Huntingtona jest wywołana wadliwym genem, który prowadzi do stopniowego rozpadu komórek nerwowych, zwykle rozpoczynającego się w średnim wieku. Na początku ludzie mogą zauważyć subtelne zmiany nastroju, drobne mimowolne ruchy lub niewielkie trudności w planowaniu i koncentracji. W ciągu 10–12 lat może to postępować do ciężkich zaburzeń ruchowych, utraty mowy, otępienia i całkowitej zależności od opiekunów. Naukowcy wiedzą, że w komórkach mózgowych w chorobie Huntingtona dochodzi do wielu nieprawidłowości — produkcja energii zawodzi, toksyczne białka tworzą skupiska, a sygnały chemiczne między komórkami stają się szkodliwe. Ponieważ jednocześnie zaburzonych jest tak wiele szlaków, strategia „jeden białko, jeden lek” miała trudności z przyniesieniem przełomów.
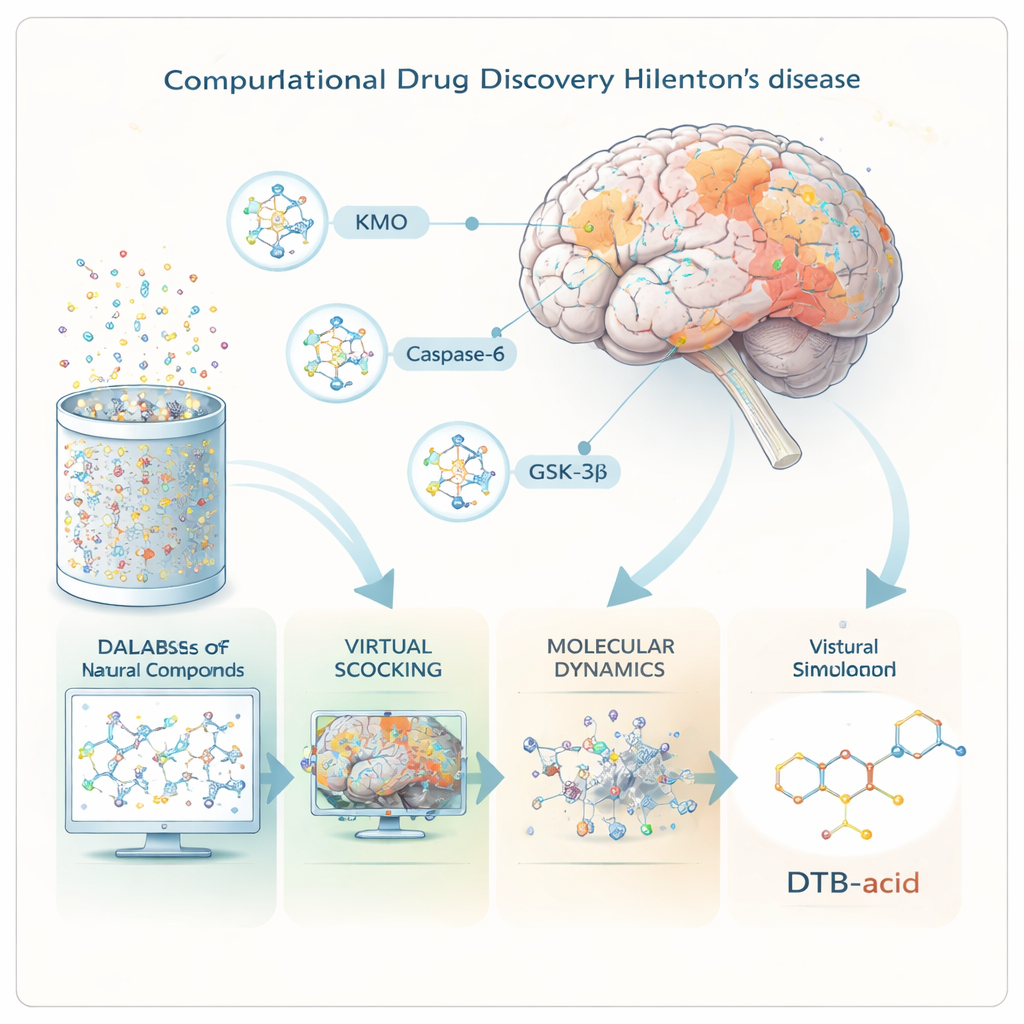
Trzy krytyczne punkty nacisku w mózgu
Naukowcy skupili się na trzech białkach, które zajmują kluczowe stanowiska kontrolne w chorobie Huntingtona. Pierwsze, KMO, kieruje rozkładem aminokwasu tryptofanu w stronę produktów toksycznych lub ochronnych; gdy równowaga przechyla się w stronę toksyn, komórki mózgowe cierpią. Drugie, kaspaza-6, tnie zmutowane białko huntingtynę na mniejsze, wysoce toksyczne fragmenty, które gromadzą się we wczesnym stadium choroby. Trzecie, GSK-3β, to enzym sygnałowy powiązany z nieprawidłowymi splątaniami białkowymi i śmiercią komórek w kilku chorobach mózgu. Znalezienie jednej cząsteczki, która mogłaby jednocześnie stłumić szkodliwą aktywność wszystkich trzech, dawało nadzieję na terapię lepiej dopasowaną do złożoności choroby.
Przesiewanie biblioteki natury za pomocą superkomputerów
Zamiast mieszać chemikalia w probówkach, naukowcy pracowali wyłącznie „in silico”, używając zaawansowanego oprogramowania do modelowania zachowania cząsteczek. Rozpoczęli od ponad 695 000 związków naturalnych pobranych z bazy publicznej, przygotowując każdy w formie trójwymiarowej. Potężne narzędzia do wirtualnego przesiewania przewidziały, które związki mają największe szanse przeniknąć barierę krew–mózg, zachowywać się jak prawdziwe leki w organizmie i unikać poważnych problemów bezpieczeństwa. Tylko około 60 000 przeszło przez te filtry i zostało przetestowanych — na komputerze — pod kątem tego, jak ściśle mogą pasować do kieszeni wiążących trzech białek docelowych.
Jedna wyróżniająca się cząsteczka: DTB-acid
Z tego ogromnego poszukiwania wyłoniła się jedna cząsteczka — nazwana DTB-acid, naturalny alkaloid związany z kwasem matrinowym. Szczegółowe badania dokowania wykazały, że DTB-acid może tworzyć silne, odpowiednio rozmieszczone kontakty wewnątrz wszystkich trzech białek. Następnie zespół przeprowadził długie symulacje dynamiki molekularnej, które naśladują ruch atomów w wodzie w czasie, aby sprawdzić, czy związek pozostanie na miejscu, zamiast odpłynąć. W symulowanych 100 miliardowych sekundy ruchu kompleksy białko–lek pozostały stabilne. Dodatkowe obliczenia energetyczne sugerowały, że wiązanie z KMO było szczególnie silne, podczas gdy oddzielna analiza cząsteczek wody w miejscach wiążących wskazała, że interakcje z GSK-3β również były termodynamicznie korzystne.
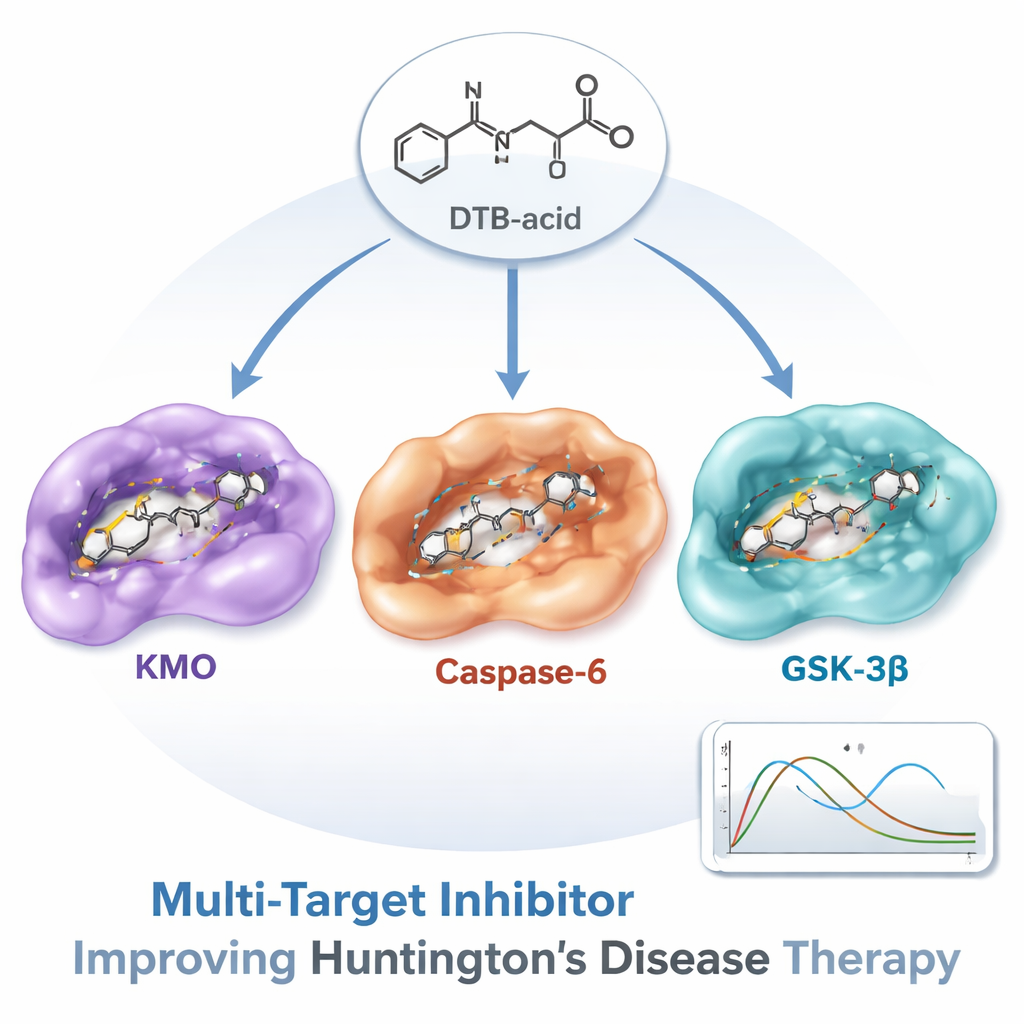
Od komputerowego trafienia do przyszłego leku
Oczywiście cząsteczka, która wydaje się obiecująca na ekranie, to tylko pierwszy krok. Autorzy podkreślają, że DTB-acid musi jeszcze zostać przetestowany w komórkach i modelach zwierzęcych, aby potwierdzić, że dociera do mózgu, trafia w zamierzone cele i rzeczywiście chroni neurony bez szkodliwych skutków ubocznych. Mimo to praca ta pokazuje potężną, efektywną ścieżkę odkrywania leków wielocelowych dla złożonych chorób mózgu. Dla odbiorcy niespecjalistycznego kluczowy wniosek jest taki, że zamiast leczyć chorobę Huntingtona szeregiem oddzielnych, wąsko ukierunkowanych leków, możliwe może być zaprojektowanie jednej starannie dobranej cząsteczki, takiej jak DTB-acid, która przeciwdziała kilku czynnikom uszkodzeń jednocześnie — dając nową nadzieję na spowolnienie lub zmianę przebiegu tej nieustępliwej choroby.
Cytowanie: Zheng, B., Banday, M., Gangwar, S. et al. In silico discovery of natural compound-derived multi-target inhibitor for Huntington’s disease therapy. Sci Rep 16, 7716 (2026). https://doi.org/10.1038/s41598-026-38430-w
Słowa kluczowe: Choroba Huntingtona, lek wielocelowy, komputerowe odkrywanie leków, związki naturalne, neurodegeneracja