Clear Sky Science · pl
Szlak sygnalizacyjny CNOT2 /c-Myc/STAT3 odgrywa kluczową rolę w apoptozie zależnej od glikolizy indukowanej przez benzyl izotiocyjanian w raku wątrobowokomórkowym
Składnik przeciwnowotworowy na twoim talerzu
Benzyl izotiocyjanian, w skrócie BITC, to naturalny związek występujący w powszechnie znanych warzywach, takich jak brokuły, kapusta i jarmuż. Choć lekarze od dawna obserwują, że osoby spożywające więcej tych produktów mają niższe wskaźniki zachorowań na nowotwory, mechanizmy, dzięki którym konkretne składniki roślinne spowalniają lub zabijają komórki nowotworowe, wciąż są badane. W tym badaniu przyjrzano się wpływowi BITC na komórki raka wątroby w laboratorium i odkryto zaskakujące powiązanie między sposobem, w jaki komórki nowotworowe metabolizują cukier, a mechanizmami prowadzącymi je do autodestrukcji.
Dlaczego rak wątroby potrzebuje lepszych opcji leczenia
Rak wątroby należy do najbardziej śmiertelnych nowotworów na świecie, a rak wątrobowokomórkowy jest jego najczęstszą postacią. Nawet przy zastosowaniu chirurgii, chemioterapii i leków celowanych wiele guzów nawraca lub przestaje odpowiadać na terapię. Jednym z powodów jest to, że komórki nowotworowe przestawiają swój sposób pozyskiwania energii: zamiast opierać się głównie na tlenie w mitochondriach, intensywnie spalają cukier w procesie często określanym jako efekt Warburga. Zniekształcony sposób wykorzystania cukru pomaga komórkom nowotworowym szybciej rosnąć i opierać się śmierci. Znalezienie bezpiecznych sposobów przerwania tego dopływu energii, zwłaszcza przy użyciu związków pochodzących z żywności, jest atrakcyjną strategią.
Testowanie związku roślinnego na komórkach raka wątroby
Naukowcy poddali dwie ludzkie linie komórkowe raka wątroby, SK-Hep1 i Huh7, działaniu rosnących dawek BITC. Wraz ze wzrostem dawki przeżywalność komórek malała, co wskazuje, że BITC jest toksyczny dla komórek raka wątroby w tych warunkach. Po bliższym zbadaniu wnętrza komórek zaobserwowali klasyczne cechy zaprogramowanej śmierci komórkowej, czyli apoptozy. Kluczowe białka, które normalnie występują w formie „nieaktywnej” przed przecięciem podczas apoptozy, takie jak PARP i kaspaza-3, występowały w zmniejszonych ilościach w postaci nienaruszonej, czyli „pro‑”. Testy cytometrii przepływowej wykazały także więcej komórek w frakcji sub‑G1 cyklu komórkowego oraz więcej komórek pozytywnych w teście Annexin V, oba te wskaźniki sugerują, że komórki nowotworowe przechodziły aktywną apoptozę, a nie jedynie ulegały uszkodzeniu.
Zamykanie apetytu nowotworu na cukier
Zespół następnie zbadał, czy BITC wpływa na efekt Warburga. Mierzono białka wspomagające intensywne pobieranie cukru i przekształcanie go w energię oraz laktat — w szczególności HK2, PKM2 i LDH. Leczenie BITC obniżało poziomy wszystkich trzech białek w obu liniach komórkowych raka wątroby oraz zmniejszało ilość laktatu uwalnianego przez komórki i ilość glukozy zużywanej z pożywki. Innymi słowy, BITC osłabiał zdolność komórek raka wątroby do obsługi ich szybkiego „spalania” cukru. Gdy naukowcy dodali pirogronian, produkt pośredni rozpadu cukrów, który nadal może zasilać metabolizm komórek, wiele efektów BITC zostało odwróconych: komórki odzyskały wyższe poziomy PARP, kaspazy-3 i enzymów glikolizy. Ten efekt „ratunkowy” sugeruje, że zakłócenie przetwarzania cukru jest kluczowym elementem mechanizmu, w którym BITC wywołuje śmierć komórek.
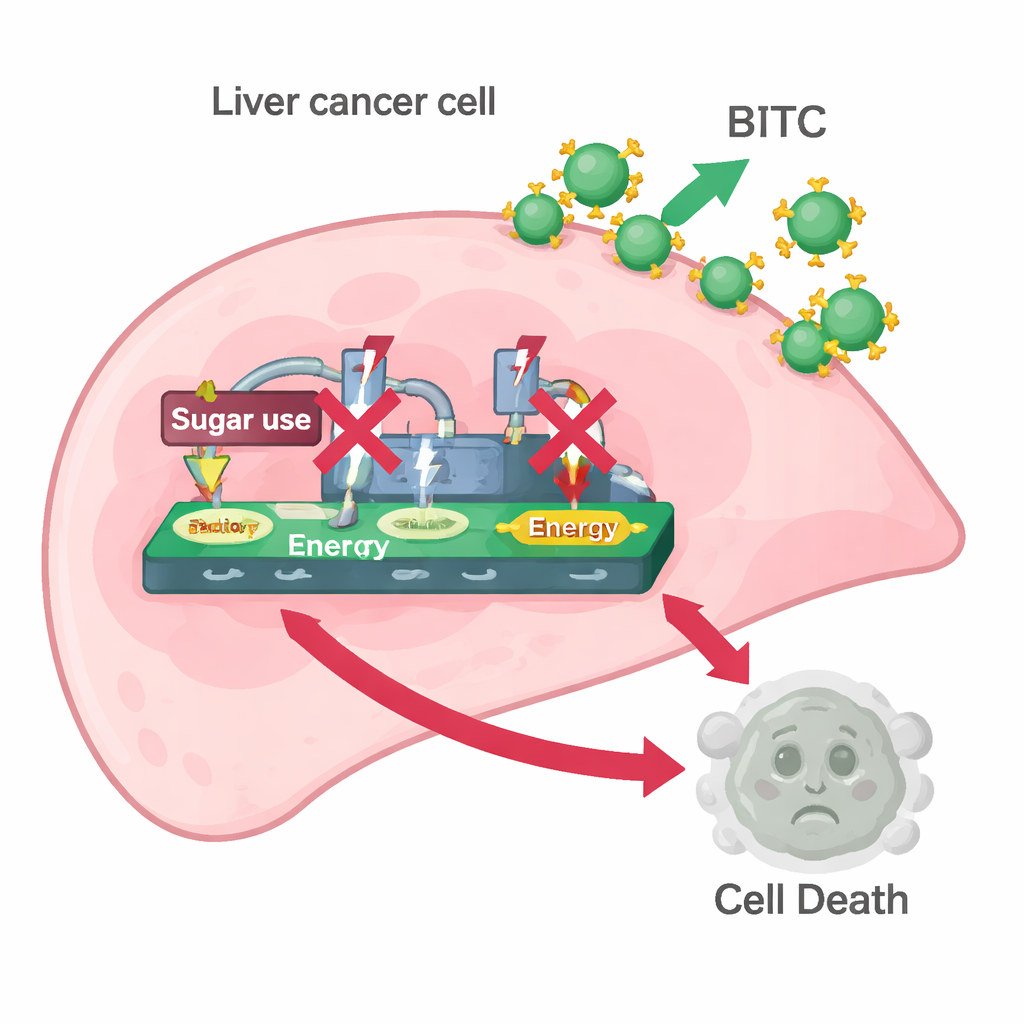
Rozplątywanie przełączników kontrolnych wewnątrz komórki
Aby zrozumieć głębsze warstwy kontroli, badacze skupili się na trójce białek sygnalizacyjnych: CNOT2, c-Myc i STAT3. Białka te wspierają wzrost, przetrwanie i metaboliczną przebudowę w wielu guzach. Dane od pacjentów z rakiem wątroby wykazały, że poziom CNOT2 zwykle jest wyższy u osób z gorszym rokowaniem. W badaniach laboratoryjnych leczenie BITC obniżało aktywną, sfosforylowaną formę STAT3, jego aktywator górnego rzędu JAK1, białko promujące wzrost c-Myc oraz sam CNOT2. Użycie narzędzi genetycznych do zmniejszenia poziomów CNOT2 lub STAT3 zwiększało efekt zabijający BITC, dodatkowo obniżając poziomy PARP i kaspazy-3. Eksperymenty badające wiązania białek ujawniły, że BITC także zaburzał fizyczne interakcje między CNOT2 a STAT3 oraz między CNOT2 a c-Myc. Gdy CNOT2 lub c-Myc zostały sztucznie zwiększone, BITC stracił dużą część swojej zdolności do tłumienia enzymów glikolizy i wywoływania apoptozy, co podkreśla, że ta oś sygnalizacyjna działa jak przełącznik główny łączący metabolizm cukrów z mechanizmami przeżycia.
Co to może znaczyć dla przyszłych terapii
W sumie wyniki tworzą spójny obraz: BITC atakuje komórki raka wątroby, odcinając ich preferowany liniowy dopływ paliwa opartego na cukrze i uruchamiając przełączniki śmierci komórkowej zależne od osi CNOT2/c-Myc/STAT3. Blokując jednocześnie sygnały wzrostu i wykorzystanie cukru, BITC przesuwa komórki nowotworowe za metaboliczny punkt krytyczny w kierunku apoptozy. Wyniki pochodzą z eksperymentów na hodowlach komórkowych, nie z badań klinicznych, i obejmowały tylko dwa typy komórek raka wątroby, więc konieczne są dalsze badania na zwierzętach i w badaniach z udziałem ludzi. Mimo to badanie wzmacnia pogląd, że niektóre związki pochodzące z codziennych warzyw mogłyby zostać udoskonalone lub skojarzone z innymi terapiami, by precyzyjniej głodzić guzy wątrobowe, jednocześnie pobudzając je do autodestrukcji.
Cytowanie: Koh, W., Park, SY., Kim, B. et al. CNOT2 /c-Myc/STAT3 signaling is critically involved in glycolysis mediated apoptosis of benzyl isothiocyanate in hepatocellular carcinoma. Sci Rep 16, 7000 (2026). https://doi.org/10.1038/s41598-026-38416-8
Słowa kluczowe: rak wątroby, benzyl izotiocyjanian, metabolizm nowotworowy, apoptoza, warzywa krzyżowe