Clear Sky Science · pl
Model prognostyczny oparty na uczeniu maszynowym łączący geny związane ze „stemness” i angiogenezą do przewidywania rokowania i infiltracji immunologicznej u pacjentów z HCC
Dlaczego to badanie ma znaczenie dla pacjentów z rakiem wątroby
Rak wątrobowokomórkowy, najczęstsza postać raka wątroby, często nawraca lub daje przerzuty nawet po leczeniu. W pracy tej badano przyczyny takiego przebiegu choroby oraz sposoby lepszego przewidywania, którzy pacjenci są najbardziej narażeni. Łącząc obszerne zbiory danych genetycznych z nowoczesnymi metodami uczenia maszynowego, badacze opracowali narzędzie łączące dwa istotne cechy nowotworu — „stemness” (komórki zachowujące się jak uporczywe nasiona) oraz neowaskularyzację — z przeżyciem pacjentów i ich prawdopodobną odpowiedzią na terapie immunologiczne.
Nowotworowe „komórki‑nasiona” i nowe naczynia
Wiele guzów zawiera małą populację komórek działających jak nasiona. Te nowotworowe komórki macierzyste potrafią odnawiać się, opierać leczeniu i ponownie zainicjować wzrost guza po operacji lub chemioterapii. Równocześnie nowotwory potrzebują tworzyć nowe naczynia krwionośne, by dostarczać tlen i substancje odżywcze niezbędne do wzrostu i rozprzestrzeniania się. Ostatnie badania pokazują, że te dwa procesy są powiązane: komórki o cechach „stemness” wydzielają sygnały stymulujące angiogenezę, a środowisko bogate w naczynia sprzyja przetrwaniu tych „nasiennych” komórek. Zrozumienie i jednoczesne ukierunkowanie tego partnerstwa jest szczególnie istotne w raku wątroby, który jest silnie unaczyniony i skłonny do nawrotów.
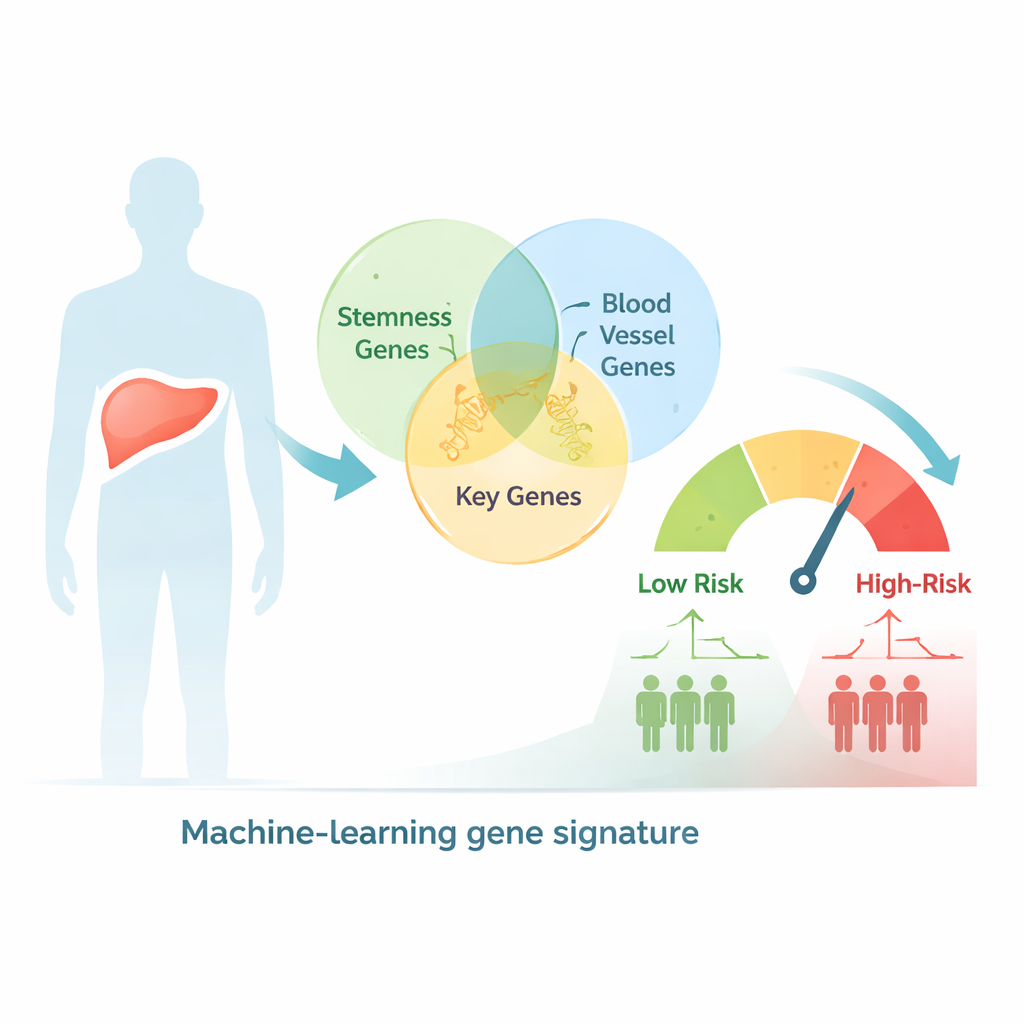
Wykorzystanie big data do podziału pacjentów według ryzyka
Badacze rozpoczęli od przeszukania obszernej bazy genów ludzkich w poszukiwaniu genów powiązanych zarówno z cechami „stemness”, jak i z tworzeniem naczyń, wychwytując ponad 2600 genów wspólnych. Następnie przeanalizowali próbki raka wątroby od setek pacjentów, których aktywność genów i wyniki kliniczne były udokumentowane w publicznych bazach onkologicznych. Za pomocą testów statystycznych i metod grupowania wyodrębnili dwa podtypy genetyczne pacjentów, które wykazywały wyraźne różnice w stadium choroby, wielkości guza i przeżyciu, co sugeruje, że łączone sygnały związane ze „stemness” i naczyniami odzwierciedlają istotną biologię tego schorzenia.
Opracowanie dziewięciogenowego wskaźnika ryzyka
Z tej obszernej puli genów zespół zastosował podejście uczenia maszynowego, aby zawęzić listę do zaledwie dziewięciu kluczowych genów, których skumulowana aktywność najlepiej przewidywała długość przeżycia pacjentów. Na podstawie tych dziewięciu genów obliczano dla każdej osoby wskaźnik ryzyka. Pacjenci z wysokim wynikiem mieli istotnie krótsze całkowite przeżycie, zarówno w zestawie danych treningowych, jak i w niezależnej grupie pacjentów użytej do walidacji. Dokładność modelu była konkurencyjna lub lepsza niż wielu istniejących narzędzi, a połączenie wyniku z prostymi informacjami klinicznymi, takimi jak stadium guza, w formie nomogramu poprawiło przewidywanie przeżyć 1-, 3- i 5‑letnich.
Powiązania z układem odpornościowym i odpowiedzią na leczenie
Zespół zbadał także, co dziewięciogenowy wskaźnik mówi o mikrośrodowisku immunologicznym guza. Guzy o niskim ryzyku miały tendencję do bycia bardziej „zapalenionymi”, z wyższymi poziomami różnych komórek odpornościowych i silniejszymi sygnałami ścieżek obronnych. Guzy o wysokim ryzyku wykazywały natomiast wzory zgodne z unikaniem odpowiedzi immunologicznej i większą liczbą mutacji w istotnych genach, takich jak TP53. Korzystając z ustalonych narzędzi komputerowych szacujących reakcję na nowoczesne terapie immunologiczne, badanie sugeruje, że pacjenci o niskim ryzyku mogą lepiej odpowiadać na inhibitory punktów kontrolnych układu odpornościowego niż pacjenci wysokiego ryzyka. Choć te przewidywania muszą zostać zweryfikowane w rzeczywistych warunkach leczenia, wskazują praktyczny sposób identyfikacji pacjentów, którzy mogą najbardziej skorzystać z takich leków.
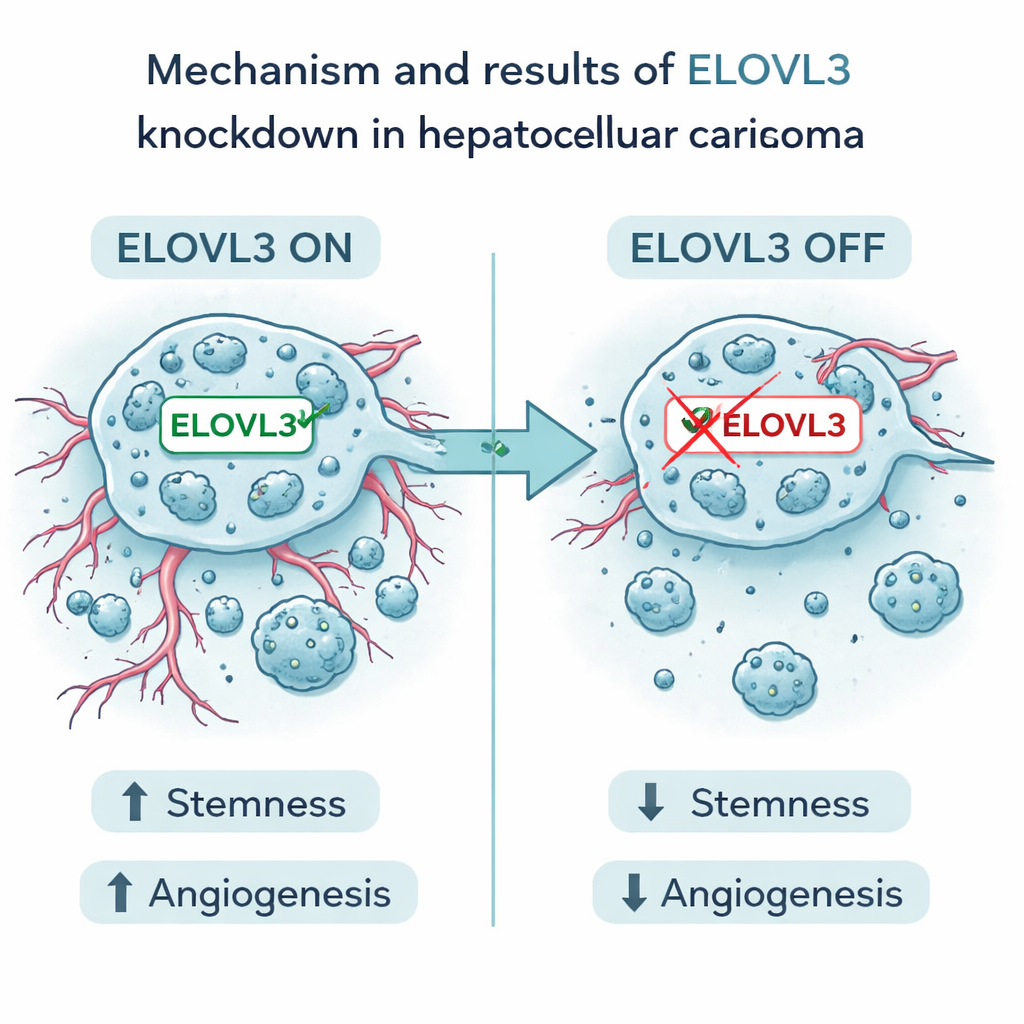
Skupienie uwagi na obiecującym celu
Wśród tych dziewięciu genów wyróżnił się jeden o nazwie ELOVL3. Wysoka ekspresja tego genu wiązała się z gorszym przeżyciem. W eksperymentach laboratoryjnych autorzy obniżyli poziom ELOVL3 w ludzkich komórkach raka wątroby. Spowodowało to zmniejszenie zdolności komórek do formowania klastrów o cechach „stemness” oraz obniżenie poziomów znanych markerów stemness. Redukcja ELOVL3 zmniejszyła także produkcję i uwalnianie dwóch głównych czynników promujących angiogenezę, VEGFA i FGF2. Komórki nowotworowe proliferowały, migrowały i inwadowały w mniejszym stopniu, a w modelach mysich guzy o obniżonym ELOVL3 były mniejsze i wykazywały mniej cech agresywnego przebiegu choroby. Wyniki te wspierają tezę, że ELOVL3 wspomaga zarówno „nasienne” zachowanie komórek raka wątroby, jak i ich zdolność do tworzenia wspierających naczyń.
Co to może oznaczać dla przyszłej opieki
Mówiąc prosto, praca ta niesie dwa główne wnioski. Po pierwsze, prosty dziewięciogenowy wskaźnik oparty na próbkach guza może podzielić pacjentów z rakiem wątroby na grupy o wyższym i niższym ryzyku oraz sugerować, jak mogą zareagować na terapie immunologiczne. Po drugie, jeden z genów tworzących ten wskaźnik, ELOVL3, wydaje się być na skrzyżowaniu zdolności nowotworu do regeneracji i tworzenia naczyń, co czyni go atrakcyjnym celem terapeutycznym w przyszłości. Chociaż model i cel wymagają potwierdzenia w prospektywnych badaniach klinicznych, otwierają drogę do bardziej spersonalizowanej opieki nad chorymi na raka wątroby oraz do strategii łączonych blokujących zarówno nowotworowe „komórki‑nasienne”, jak i ich ukrwienie.
Cytowanie: Cheng, F., Shi, Y., Gao, X. et al. Machine learning-based prognostic model of stemness and angiogenesis-related genes for predicting prognosis and immune infiltration in patients with HCC. Sci Rep 16, 7271 (2026). https://doi.org/10.1038/s41598-026-38379-w
Słowa kluczowe: rak wątrobowokomórkowy, komórki macierzyste nowotworu, angiogeneza, prognostyczny podpis genowy, ELOVL3