Clear Sky Science · pl
Zmienne odniesieniowe genów w zależności od wieku i płci u myszy 5XFAD uwidaczniają wyzwania normalizacji w modelach choroby Alzheimera
Dlaczego to badanie na myszach ma znaczenie dla badań nad Alzheimerem
Kiedy naukowcy szukają wczesnych sygnałów ostrzegawczych lub efektów leczenia w chorobie Alzheimera, często mierzą, jak mocno różne geny są włączone lub wyłączone w mózgu. Aby stwierdzić, czy gen rzeczywiście uległ zmianie, potrzebny jest najpierw stały „metrycznik” do porównań: geny referencyjne, które zakłada się, że pozostają niezmienne. Ten artykuł pokazuje, że w szybko postępującym modelu myszy choroby Alzheimera te rzekomo stałe geny nie są tak stabilne, jak wielu badaczy zakłada — zwłaszcza w zależności od wieku, regionu mózgu i płci.
Jak naukowcy odczytują aktywność genetyczną mózgu
Nowoczesne badania mózgu często opierają się na technice zwanej RT-qPCR, która mierzy, ile cząsteczek informacyjnego materiału genetycznego danego genu znajduje się w próbce tkanki. Ponieważ próbki nigdy nie zawierają dokładnie tej samej ilości całkowitej materii, naukowcy normalizują pomiary względem jednego lub więcej genów referencyjnych, często nazywanych „genami gospodarza”, które powinny być stałe w różnych warunkach. W praktyce jednak choroby takie jak Alzheimer radykalnie zmieniają skład komórkowy, metabolizm i stan zapalny w mózgu, co może po cichu przesuwać poziomy tych genów referencyjnych. Jeśli sam gen referencyjny się zmienia, każde pomiary na jego podstawie mogą wprowadzać w błąd, wyolbrzymiając lub ukrywając rzeczywiste zmiany biologiczne.
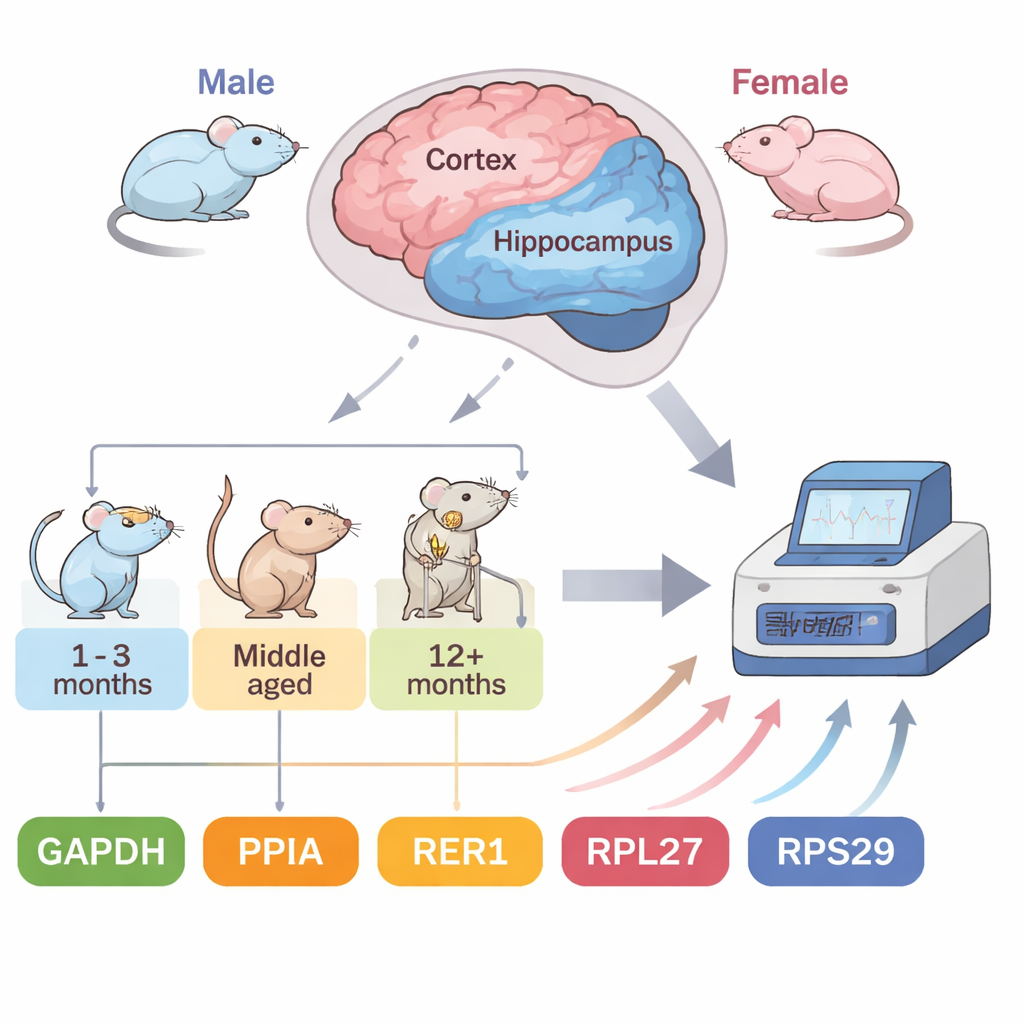
Przyspieszony model myszy choroby Alzheimera
Zespół skupił się na myszach 5XFAD, powszechnie stosowanym modelu niosącym pięć ludzkich mutacji związanych z rodzinną postacią choroby Alzheimera. Zwierzęta te rozwijają płytki amyloidowe — skupiska białkowe będące znakiem rozpoznawczym schorzenia — niezwykle wcześnie: około drugiego miesiąca życia, a intensywne odkładanie płytek występuje już w 4.–5. miesiącu. Przyspieszona oś czasu pozwala badaczom śledzić zmiany związane z chorobą w ciągu miesięcy zamiast lat. Autorzy przebadali dwie podatne na uszkodzenia struktury mózgu, korę i hipokamp, u myszy samców i samic w czterech stadiach: wczesnym (2 miesiące), rozwijającym się (4 miesiące) oraz bardziej zaawansowanym (7 i 10 miesięcy). Testowali pięć powszechnych genów referencyjnych i zastosowali cztery niezależne narzędzia statystyczne, by uszeregować stabilność każdego z nich w tych zmieniających się warunkach.
Geny referencyjne nie są uniwersalne
Wyniki pokazują, że żaden pojedynczy gen nie pozostał idealnie stały wszędzie. Stabilność zależała od miejsca pochodzenia próbki w mózgu, płci myszy i stopnia zaawansowania choroby. Niektóre geny, takie jak Gapdh — klasyczny „roboczy” gen w wielu badaniach — sprawdzały się relatywnie dobrze w kilku kontekstach, zwłaszcza w korze na wcześniejszych etapach, lecz wykazywały większą zmienność w późniejszych stadiach lub w niektórych próbkach hipokampa. Inne kandydatury, takie jak Rps29, Ppia, Rpl27 i Rer1, okazały się lepszymi partnerami w konkretnych kombinacjach, a te „najlepsze pary” zmieniały się wraz z wiekiem i płcią. Ogólnie kora wykazywała większą zmienność niż hipokamp, a późniejsze stadia choroby, szczególnie u samców, zaburzały rzekomą stabilność kilku genów referencyjnych.
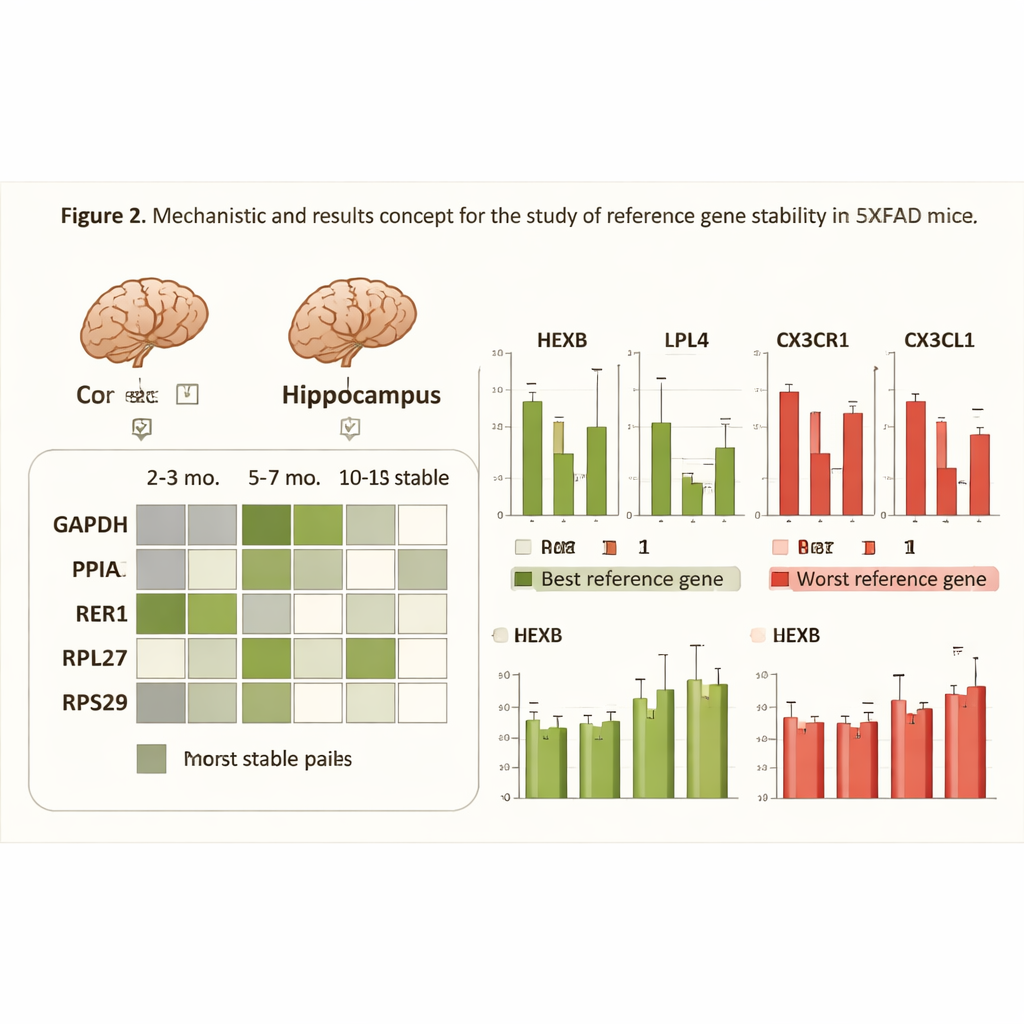
Co się dzieje, gdy miernik się wygina
Aby pokazać, dlaczego staranny wybór genów referencyjnych ma znaczenie, badacze przeanalizowali cztery geny mózgowe zaangażowane w procesy zapalne, metabolizm i sygnalizację układu odpornościowego — procesy mocno powiązane z chorobą Alzheimera. Porównali zmiany pozorne w tych genach docelowych, gdy normalizowano je względem najstabilniejszej pary referencyjnej, najmniej stabilnego pojedynczego genu lub wszystkich pięciu genów razem. Gdy używano słabych genów referencyjnych, dane stawały się bardziej hałaśliwe, a niektóre biologicznie istotne zmiany wydawały się słabsze lub nawet statystycznie nieistotne. Natomiast użycie najlepiej dopasowanej pary dla danego warunku zmniejszało rozrzut pomiarów i wzmacniało wykrywanie rzeczywistych różnic między myszami zdrowymi a chorymi, szczególnie w późniejszych stadiach patologii.
Czystsze sygnały dla złożonej choroby
Dla osób spoza specjalizacji wniosek jest prosty: nawet podstawowe miary stosowane w badaniach genów mogą się zniekształcać pod wpływem gwałtownie zmieniającej się choroby mózgu, jaką jest Alzheimer. Praca ta dostarcza praktycznego przewodnika do wyboru lepszych genów referencyjnych w ważnym modelu myszy i podkreśla, że badacze muszą weryfikować swoje „metryki” dla każdego regionu mózgu, wieku i płci, które analizują. Dzięki temu naukowcy mogą uzyskać jaśniejsze, bardziej wiarygodne pomiary tego, które geny rzeczywiście zmieniają się podczas degeneracji podobnej do alzheimerowskiej — co jest kluczowym krokiem do zrozumienia mechanizmów choroby i oceny potencjalnych terapii.
Cytowanie: Daini, E., Antonioni, K., Piemontese, M. et al. Reference gene variability across age and sex in 5XFAD mice highlights normalization challenges in Alzheimer’s models. Sci Rep 16, 7302 (2026). https://doi.org/10.1038/s41598-026-38346-5
Słowa kluczowe: choroba Alzheimera, ekspresja genów, myszy 5XFAD, geny referencyjne, RT-qPCR