Clear Sky Science · pl
Hamowanie receptora galaniny 3 spowalnia degenerację siatkówki w retinitis pigmentosa przez modulację odpowiedzi zapalnej i stresu oksydacyjnego
Dlaczego ochrona zanikania widzenia nocnego ma znaczenie
Retinitis pigmentosa to grupa chorób dziedzicznych, które stopniowo odbierają ludziom widzenie nocne i obwodowe, często prowadząc do poważnej utraty wzroku w średnim wieku. Nie istnieje uniwersalnie skuteczne leczenie, częściowo dlatego, że chorobę mogą powodować bardzo różne mutacje genów. To badanie bada inną strategię: zamiast naprawiać uszkodzony gen, pyta, czy stłumienie szkodliwego zapalenia i „rdzewienia” tkanki w siatkówce może spowolnić utratę komórek światłoczułych i pomóc zachować wzrok.
Przełącznik stresu ukryty w siatkówce
Komórki światłoczułe w tylnej części oka, zwane fotoreceptorami, muszą nieustannie równoważyć zużycie energii, tlen, składniki odżywcze i usuwanie odpadów. W jednej powszechnej postaci retinitis pigmentosa mutacja w białku rodopsynie (znana jako P23H) powoduje niepoprawne fałdowanie tego barwnika wzrokowego, zapychając wewnętrzne mechanizmy komórkowe i wywołując chroniczny stres. Ten stres z kolei uruchamia zapalenie i uszkodzenia oksydacyjne, które mogą prowadzić do śmierci fotoreceptorów. Autorzy skupili się na białku sygnałowym zwanym receptorem galaniny 3 (GALR3), obecnym w kilku typach komórek siatkówki. Stwierdzili, że u myszy niosących mutację P23H GALR3 i jego naturalne ligandy były aktywowane silniej niż w zdrowych oczach, co sugeruje, że GALR3 może działać jako wzmacniacz stresu w degenerującej siatkówce.
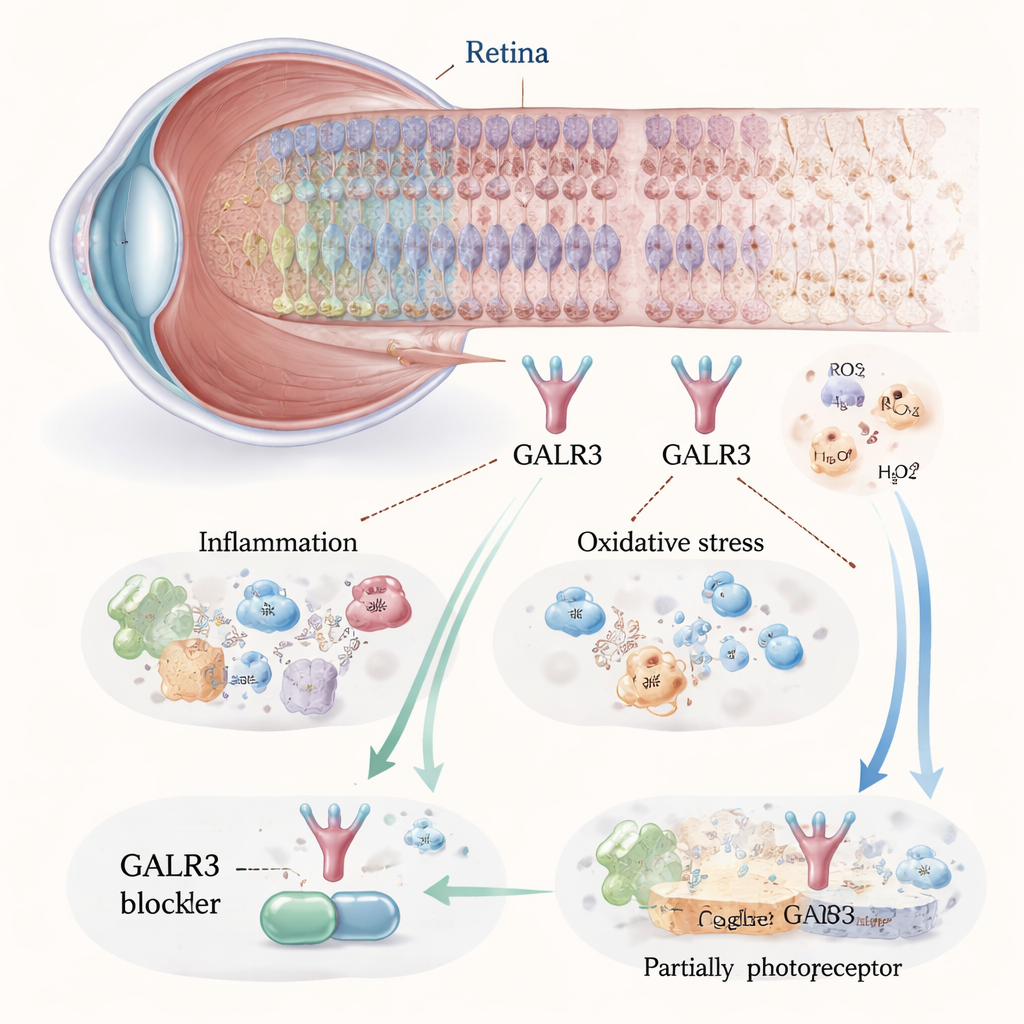
Spowolnienie utraty komórek przez zablokowanie szkodliwego sygnału
Aby sprawdzić, czy GALR3 napędza uszkodzenia czy ochronę, badacze zastosowali dwie strategie u myszy P23H: wyhodowali zwierzęta całkowicie pozbawione genu Galr3 oraz leczyli inne grupy lekiem, który specyficznie blokuje receptor, nazwanym SNAP-37,889. Przez kilka tygodni badali strukturę siatkówki za pomocą obrazowania o wysokiej rozdzielczości i mierzyli reakcje elektryczne na światło. U nieleczonych myszy P23H warstwa jąder zawierająca fotoreceptory przerzedziła się w przybliżeniu o połowę w porównaniu ze zdrowymi myszami już w wieku miesiąca i nadal zmniejszała się. Gdy GALR3 był zablokowany, to przerzedzenie było istotnie mniejsze, a kluczowe białka wzrokowe, takie jak rodopsyna i opsyna czopków, utrzymywały się na wyższych poziomach. Rejestracje elektryczne siatkówki również wykazały silniejsze odpowiedzi na światło u myszy leczonych lub pozbawionych GALR3, co oznacza, że przetrwałe komórki działały lepiej, a nie tylko istniały.
Przyciszanie zapalenia i wzmacnianie mechanizmów obronnych
Zespół następnie zapytał, dlaczego hamowanie GALR3 pomagało. W retinitis pigmentosa komórki wspierające w siatkówce — glej Müllerów i mikroglej — przechodzą z roli opiekunów w nadaktywne komórki odpowiadające, które napędzają chroniczne zapalenie. U myszy P23H markery tego „stanu alarmowego”, w tym GFAP w komórkach glejowych i IBA-1 w mikrogleju, były mocno zwiększone, a zestaw cząsteczek zapalnych i kompleksów czujników niebezpieczeństwa, takich jak NF-κB i inflamasom NLRP3, wykazywał podwyższone poziomy. Zablokowanie GALR3 uspokoiło tę reakcję: aktywacja gleju została zredukowana, cytokiny prozapalne spadły, a sygnały przeciwzapalne związane z regeneracją tkanki, takie jak IL‑10 i TGF‑β1, wzrosły wcześnie w przebiegu choroby. Równolegle hamowanie GALR3 wzmocniło mechanizmy antyoksydacyjne siatkówki. Zwiększyło aktywność NRF2, głównego regulatora genów antyoksydacyjnych, oraz podniosło poziomy enzymów neutralizujących reaktywne formy tlenu, pomagając ograniczyć dalsze uszkodzenia wynikające ze stresu metabolicznego.
Ochrona wewnętrznej bariery oka
Zdrowe widzenie zależy także od szczelnej „barierki krew–siatkówka”, która chroni przed przedostawaniem się niepożądanych cząsteczek i komórek odpornościowych do delikatnej tkanki nerwowej. U myszy P23H ta bariera zaczęła przeciekać: połączenia między komórkami barwnikowymi nabłonka siatkówki stały się nierówne, a białka krwi przedostawały się do siatkówki. Zarówno genetyczne usunięcie, jak i farmakologiczne zablokowanie GALR3 znacznie zmniejszyły te uszkodzenia, zachowując uporządkowany, kafelkowy układ bariery i ograniczając przecieki. W eksperymentach na hodowlach komórkowych komórki przypominające fotoreceptory wystawione na sygnały zapalne pochodzące od aktywowanego mikrogleju zwiększały ekspresję własnych genów zapalnych, ale efekt ten był osłabiony, gdy GALR3 w komórkach fotoreceptorowych został wyciszony. Razem te wyniki pokazują, że GALR3 znajduje się na skrzyżowaniu łączącym aktywację mikrogleju, stres oksydacyjny i rozpad bariery z obumieraniem fotoreceptorów.
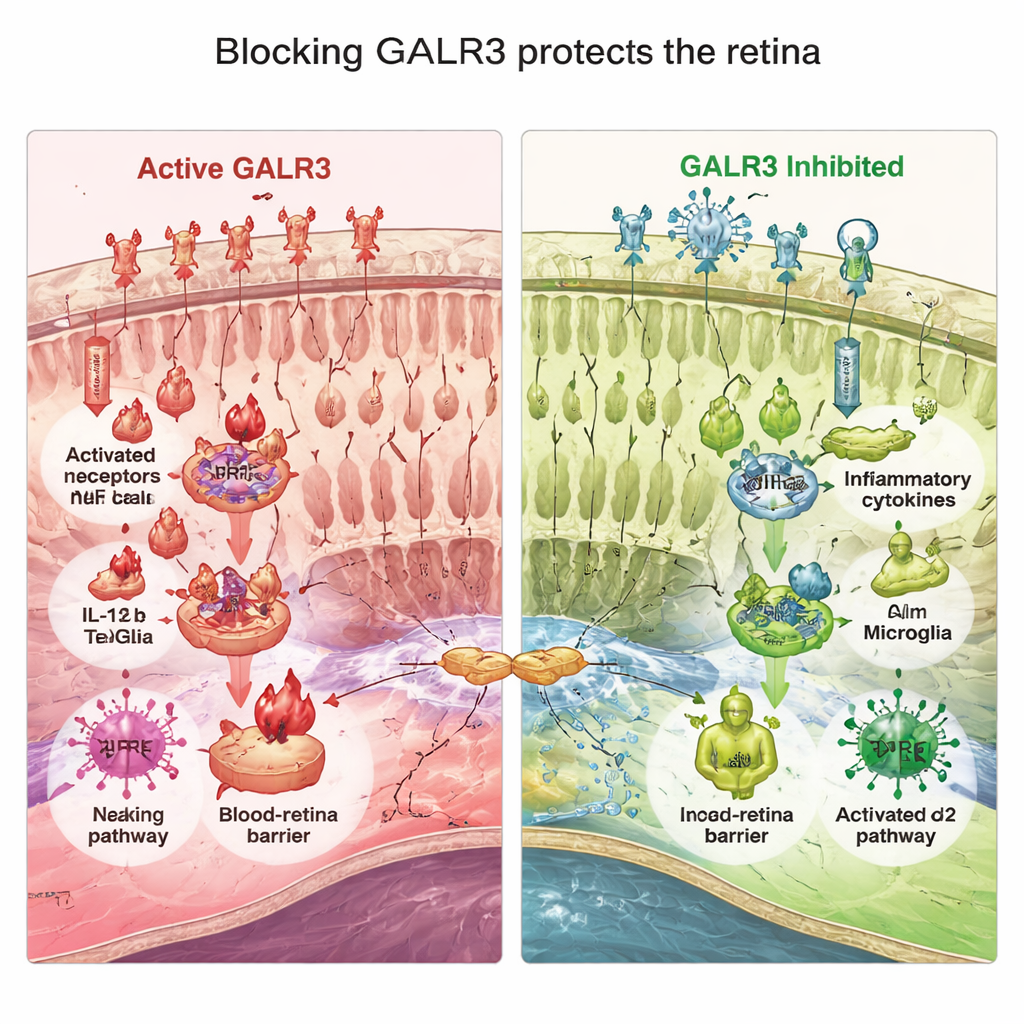
Ścieżka niezależna od mutacji prowadząca do ratowania wzroku
Dla osób z retinitis pigmentosa, zwłaszcza tych, które prawdopodobnie nigdy nie otrzymają terapii ukierunkowanych na konkretną mutację, strategie szeroko spowalniające uszkodzenia siatkówki są bardzo cenne. To badanie identyfikuje GALR3 jako kluczowy „regulator głośności” szkodliwego zapalenia i stresu oksydacyjnego w szeroko stosowanym modelu myszy tej choroby. Zablokowanie GALR3 nie wyleczyło retinitis pigmentosa, ale konsekwentnie spowalniało utratę fotoreceptorów, poprawiało odpowiedzi siatkówki na światło, redukowało toksyczne zapalenie, wzmacniało naturalne mechanizmy antyoksydacyjne i pomagało utrzymać wewnętrzną barierę oka. Ponieważ GALR3 działa na szlaki stresu i układu odpornościowego, a nie na pojedynczą mutację, leki celujące w ten receptor mogłyby teoretycznie pomagać pacjentom z wieloma różnymi genetycznymi przyczynami degeneracji siatkówki.
Cytowanie: Azam, M., Pashandi, Z., Liu, M. et al. Inhibition of galanin receptor 3 slows down retina degeneration in retinitis pigmentosa through modulation of inflammatory and oxidative stress response. Sci Rep 16, 7765 (2026). https://doi.org/10.1038/s41598-026-38345-6
Słowa kluczowe: retinitis pigmentosa, zapalanie siatkówki, przeżywalność fotoreceptorów, receptor galaniny 3, stres oksydacyjny