Clear Sky Science · pl
DGCR8 reguluje wiele procesów sprzężonej z transkrypcją nukleotydowej naprawy wycięciowej
Jak światło słoneczne rozmawia z naszymi genami
Za każdym razem, gdy wchodzimy na słońce, niewidoczne promienie ultrafioletowe (UV) uderzają w naszą skórę i uszkadzają DNA w komórkach. Najczęściej komórki naprawiają te uszkodzenia zanim wywołają problemy. To badanie ujawnia zaskakującego uczestnika tego systemu ochronnego: białko o nazwie DGCR8, wcześniej znane z udziału w tworzeniu mikroRNA. Naukowcy pokazują, że po ekspozycji na UV DGCR8 zmienia zadania i koordynuje kilka etapów kluczowej ścieżki naprawczej DNA, co pomaga zapobiegać nowotworom i innym chorobom.
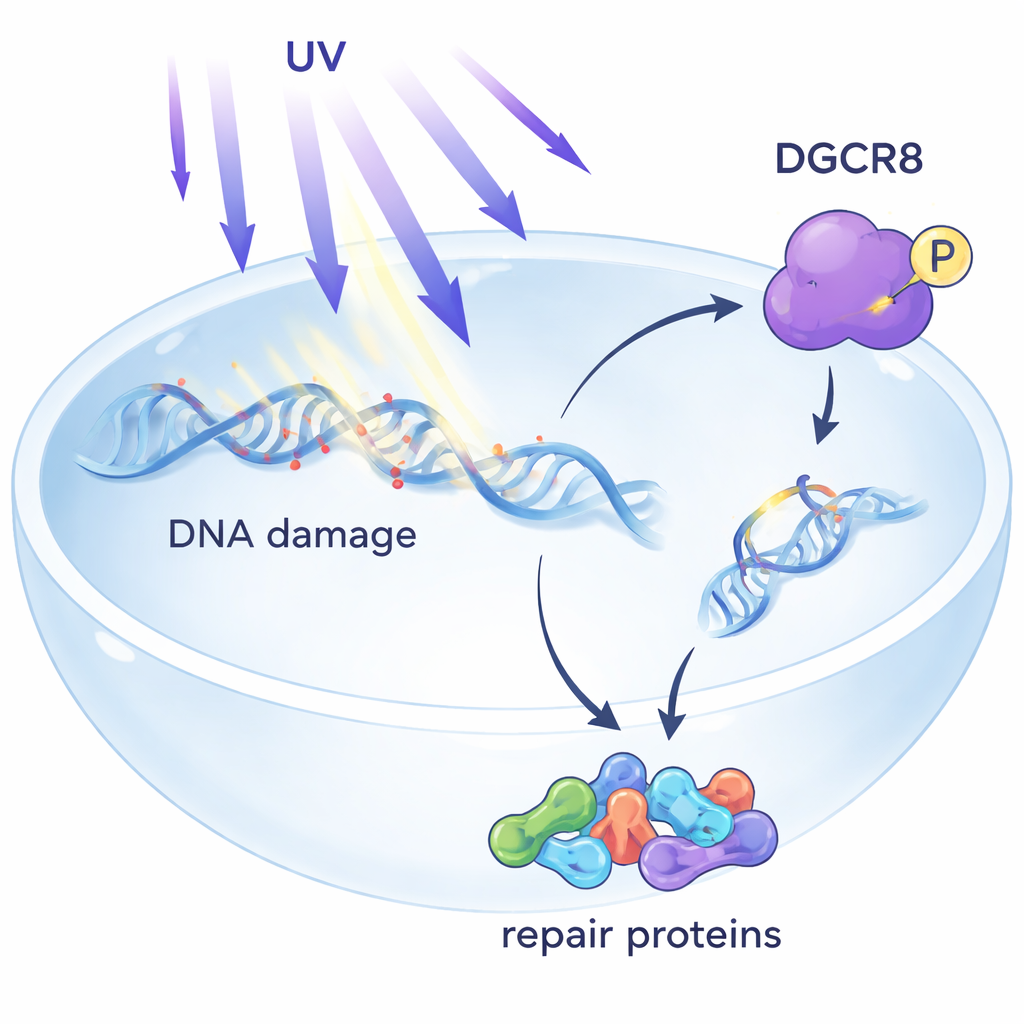
Ukryty strażnik w naprawie DNA
Światło UV tworzy drobne uszkodzenia w DNA, które mogą zatrzymywać molekularne maszyny czytające geny. Jedną z głównych obron organizmu jest sprzężona z transkrypcją nukleotydowa naprawa wycięciowa (TC-NER), która skupia się na uszkodzeniach blokujących enzymy czytające geny. Do tej pory DGCR8 było znane głównie z przetwarzania mikroRNA — krótkich cząsteczek RNA modulujących aktywność genów. Wcześniejsze prace sugerowały, że DGCR8 także chroni komórki przed UV, ale mechanizm był niejasny. W tej pracy wykazano, że po ekspozycji na UV DGCR8 fizycznie łączy się z centralnymi czynnikami TC-NER, działając jako organizator, który zbiera elementy naprawcze dokładnie tam, gdzie zatrzymuje się odczyt genów.
Cząsteczkowy przełącznik włącz/wyłącz dla DGCR8
Kluczem nowej roli DGCR8 jest pojedynczy chemiczny znacznik na jednym z jego aminokwasów — serynie na pozycji 153. Gdy to miejsce jest fosforylowane, czyli zostaje do niego przyłączona grupa fosforanowa, DGCR8 zyskuje zdolność wiązania się z podstawowymi białkami TC-NER, w tym polimerazą RNA II (enzym odczytujący geny) oraz czynnikami naprawczymi CSB, CSA i UVSSA. Komórki zmodyfikowane tak, by DGCR8 nie mogło być fosforylowane w tym miejscu (mutant S153A), wykazywały osłabione lub utracone interakcje między tymi białkami naprawczymi, a normalne, wywołane UV, tworzenie kompleksu naprawczego nie zachodziło. Wersja „fosfomimetyczna”, która zachowuje się, jakby była stale fosforylowana, miała odwrotny efekt, wzmacniając kluczowe interakcje nawet bez ekspozycji na UV. Wyniki te wskazują, że fosforylacja przy Ser153 działa jak przełącznik włącz/wyłącz, przemieniając DGCR8 z jego zwykłej roli w przetwarzaniu RNA w koordynatora naprawy DNA.
Rozplątywanie niebezpiecznych supłań DNA–RNA
Ponadto DGCR8 pomaga kontrolować struktury zwane pętlami R — krótkie odcinki, gdzie nowo powstałe RNA przywiera z powrotem do DNA, tworząc hybrydę DNA–RNA. W niewielkich ilościach pętle R mogą być użyteczne, ale gdy kumulują się po ekspozycji na UV, mogą zatrzymywać kopiowanie DNA i destabilizować chromosomy. Przy użyciu specjalistycznych przeciwciał i sond fluorescencyjnych autorzy wykazali, że komórki pozbawione DGCR8 lub noszące niefosforylowalną formę S153A gromadzą znacznie więcej pętli R po UV. Fosforylowane DGCR8 obserwowano w tych hybrydowych strukturach, zwłaszcza tam, gdzie nakładały się na uszkodzenia wywołane UV, co sugeruje, że pomaga zapobiegać lub usuwać szkodliwe pętle R dokładnie w aktywnych genach pod wpływem stresu.
Utrzymanie kontroli nad kopiowaniem DNA
Gdy uszkodzenia DNA lub pętle R zakłócają kopiowanie genomu, komórki zwykle zwalniają replikację dzięki układowi bezpieczeństwa znanemu jako punkt kontrolny ATR–CHK1. Eksperymenty śledzące włókna replikacyjne pokazały, że komórki z normalnym DGCR8 zwalniały długości śladów replikacyjnych po ekspozycji na UV, co odzwierciedla uruchomiony punkt kontrolny. W wyraźnym kontraście komórki bez DGCR8 lub z mutacją S153A kontynuowały replikację prawie z normalną prędkością, mimo nagromadzenia uszkodzeń DNA i pętli R. Dalsze testy wykazały, że chociaż sam ATR był aktywowany, jego kluczowy partner CHK1 słabo się włączał w tych mutantowych komórkach. To wskazuje, że fosforylowane DGCR8 pomaga przekazywać sygnał stresu z uszkodzonego DNA i pętli R do CHK1, co pozwala komórce zatrzymać się i ustabilizować replikację.
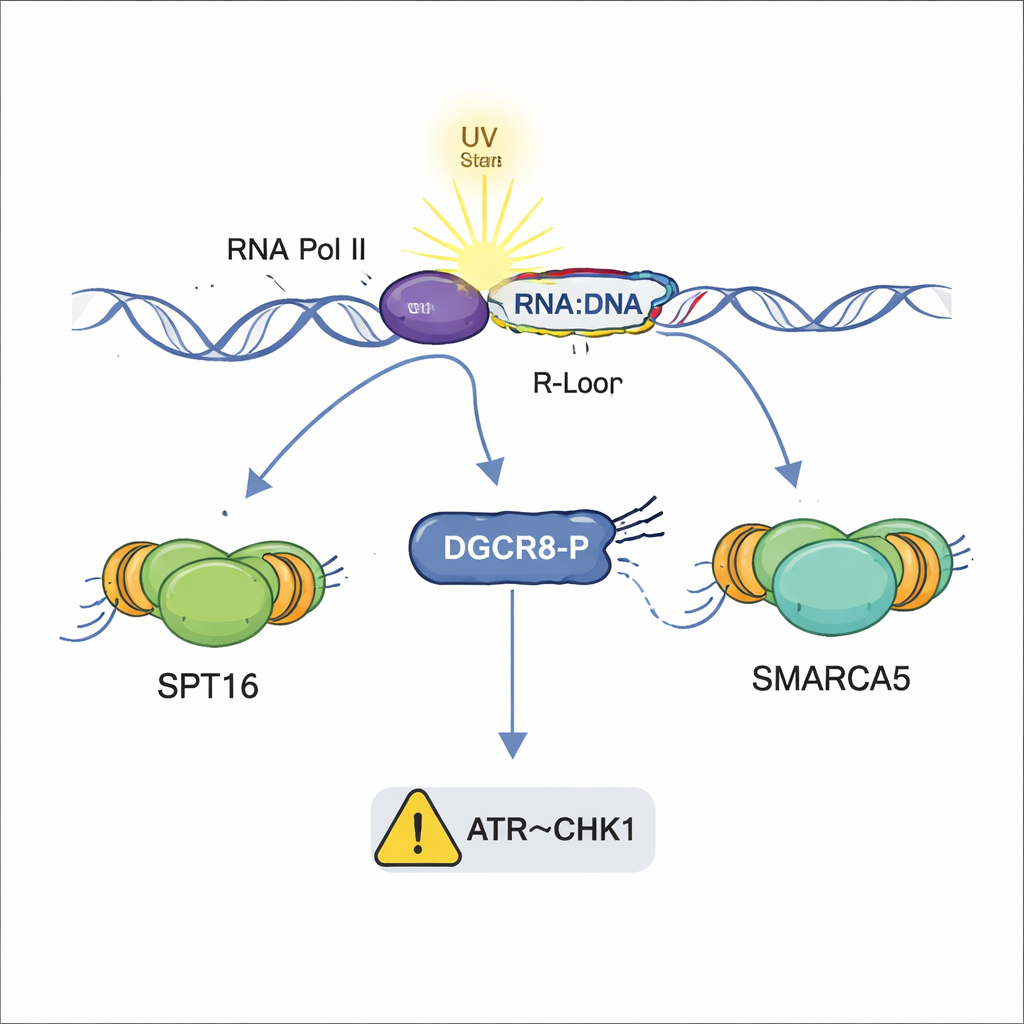
Dlaczego to ma znaczenie dla zdrowia i chorób
Podsumowując, wyniki ukazują DGCR8 jako wielozadaniowego strażnika, który koordynuje kilka warstw odpowiedzi na uszkodzenia wywołane UV: składanie zespołu naprawczego TC-NER, rekrutację remodelerów chromatyny otwierających DNA, powstrzymywanie szkodliwych hybryd DNA–RNA oraz pomoc w uruchomieniu spowolnienia replikacji przez ścieżkę ATR–CHK1. Co istotne, te działania są odrębne od tradycyjnej roli DGCR8 w biogenezie mikroRNA i zależą od fosforylacji pojedynczego miejsca. Ponieważ defekty w naprawie DNA i kontroli pętli R są powiązane z nowotworami i chorobami neurologicznymi, a mutacje DGCR8 wykryto w niektórych guzach, zrozumienie tego cząsteczkowego przełącznika może otworzyć nowe drogi diagnostyki lub terapii schorzeń związanych z uszkodzeniami UV i niestabilnością genomu.
Cytowanie: Watanabe, T., Yoshinami, D., Yamasaki, H. et al. DGCR8 regulates multiple processes of transcription coupled nucleotide excision repair. Sci Rep 16, 7112 (2026). https://doi.org/10.1038/s41598-026-38338-5
Słowa kluczowe: uszkodzenia DNA wywołane UV, DGCR8, naprawa DNA, pętle R, stabilność genomu