Clear Sky Science · pl
Selektywna inaktywacja Lis1 zaburza migrację i pozycjonowanie kortykalnych interneuronów somatostatynowych
Dlaczego małe komórki mózgowe i pojedynczy gen mają znaczenie
W naszych mózgach miliardy komórek nerwowych muszą trafić na dokładnie właściwe miejsce, żeby myśli, emocje i pamięć działały prawidłowo. W tym badaniu przyglądamy się niewielkiej, lecz istotnej grupie komórek zwanych interneuronami somatostatynowymi oraz genowi Lis1, znanemu z tego, że jego mutacje wywołują ciężkie zaburzenie „gładkiego mózgu” (lissencefalię). Pytań, co się dzieje, gdy Lis1 jest wyłączony tylko w tej małej populacji komórek, pozwoliły badaczom odkryć, jak subtelne błędy w ruchu komórek w czasie rozwoju mogą przekształcić kluczowe obszary mózgu związane z nastrojem, pamięcią i chorobami psychicznymi.
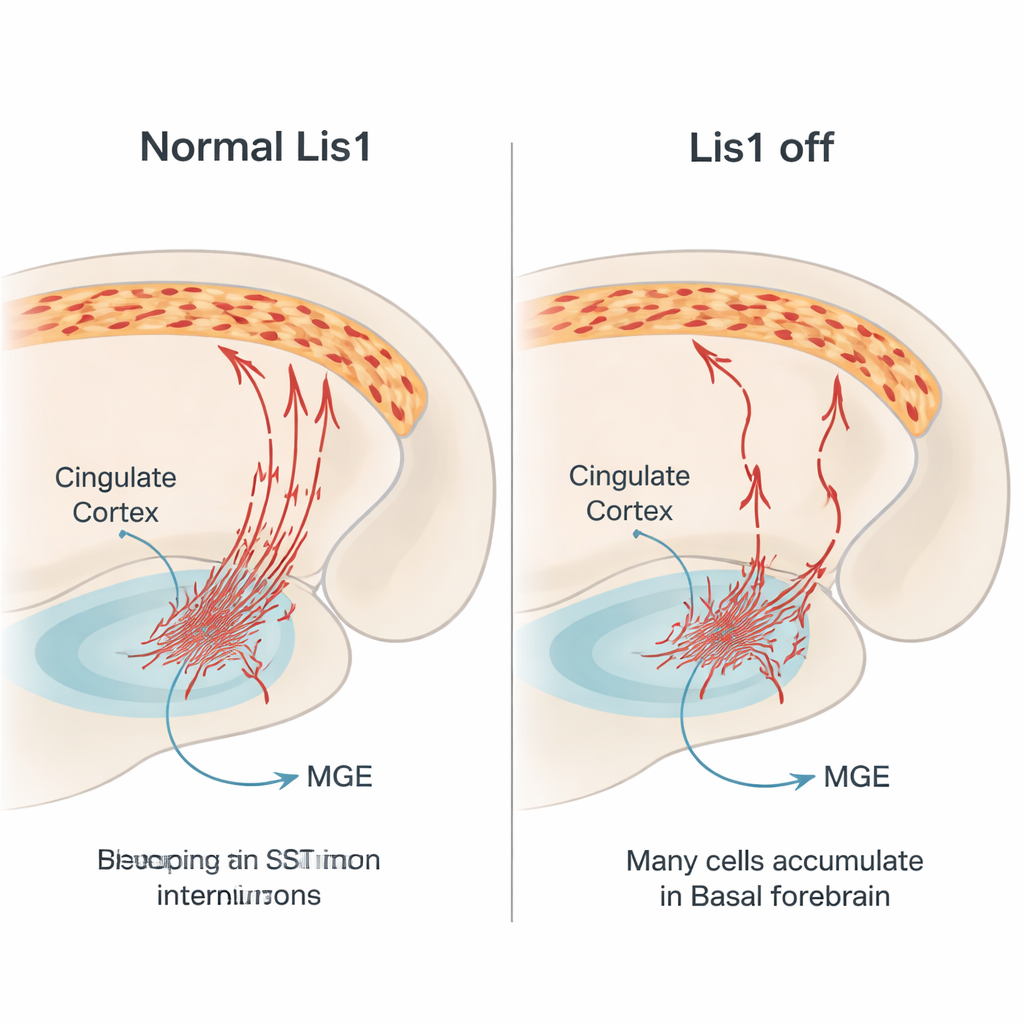
Główne elementy hamulcowego systemu mózgu
Interneurony somatostatynowe działają jako część hamulcowego systemu mózgu. Uwalniają hamujący neuroprzekaźnik GABA oraz peptyd somatostatynę, głównie celując w rozgałęzienia pobudzających neuronów piramidowych. To pomaga utrzymać równowagę aktywności mózgu, co jest niezbędne dla normalnego postrzegania, podejmowania decyzji i kontroli emocji. Wiele z tych interneuronów rodzi się w głębokim obszarze embrionalnego mózgu zwanym przyśrodkową eminencją prążkowiową (medial ganglionic eminence). Stamtąd wędrują bocznie na duże odległości do kory mózgowej, w tym do kory obręczy, która jest węzłem dla emocji, bólu i pamięci. Ponieważ ta podróż jest skomplikowana i ściśle zsynchronizowana, geny kierujące ruchem komórek są kluczowe. Lis1 jest jednym z takich genów, znanym z regulacji wewnętrznego szkieletu komórkowego i mechanizmów motorowych przesuwających jądro oraz kształtujących komórkę podczas migracji.
Skierowany eksperyment „wyłączenia” genetycznego
Aby ustalić, jaką rolę Lis1 pełni konkretnie w interneuronach somatostatynowych, autorzy zaprojektowali myszy, w których Lis1 jest usuwany tylko w komórkach uruchamiających ekspresję genu somatostatyny. Użyto też czerwonego białka fluorescencyjnego, by trwale oznaczyć te komórki i śledzić je w czasie rozwoju. Taki projekt pozwolił zespołowi odróżnić efekty wewnątrz samych komórek somatostatynowych od zmian w pozostałej części mózgu. Następnie badano dwa obszary kory obręczy — przednią korę obręczy i korę retrosplenialną — około miesiąca po urodzeniu, kiedy obwody korowe są stosunkowo dojrzałe, ale nadal plastyczne. Zastosowano staranne metody liczenia, aby oszacować zarówno bezwzględną liczbę, jak i gęstość interneuronów somatostatynowych w każdej warstwie kory.
Mniej interneuronów i przesunięty wzorzec korowy
U młodych dorosłych myszy pozbawionych Lis1 w interneuronach somatostatynowych zarówno przednia kora obręczy, jak i kora retrosplenialna zawierały znacznie mniej tych komórek niż u zwierząt kontrolnych. Ubytek był duży i spójny we wszystkich badanych warstwach, co wskazuje na rzeczywistą utratę, a nie prostą redystrybucję. Gdy badacze przyjrzeli się bliżej rozkładowi pozostałych komórek, odkryli zmianę zwykłego wzorca warstwowego. U zdrowych myszy interneurony somatostatynowe mają tendencję do koncentracji w głębszych warstwach kory. U mutantów gradient ten został odwrócony — relatywnie więcej komórek znajdowało się w warstwach powierzchownych, a mniej w warstwie najgłębszej. Co ważne, ogólny rozmiar obszarów obręczy nie zmniejszył się, więc niższa gęstość odzwierciedla rzeczywisty brak interneuronów, a nie skurcz tkanki.
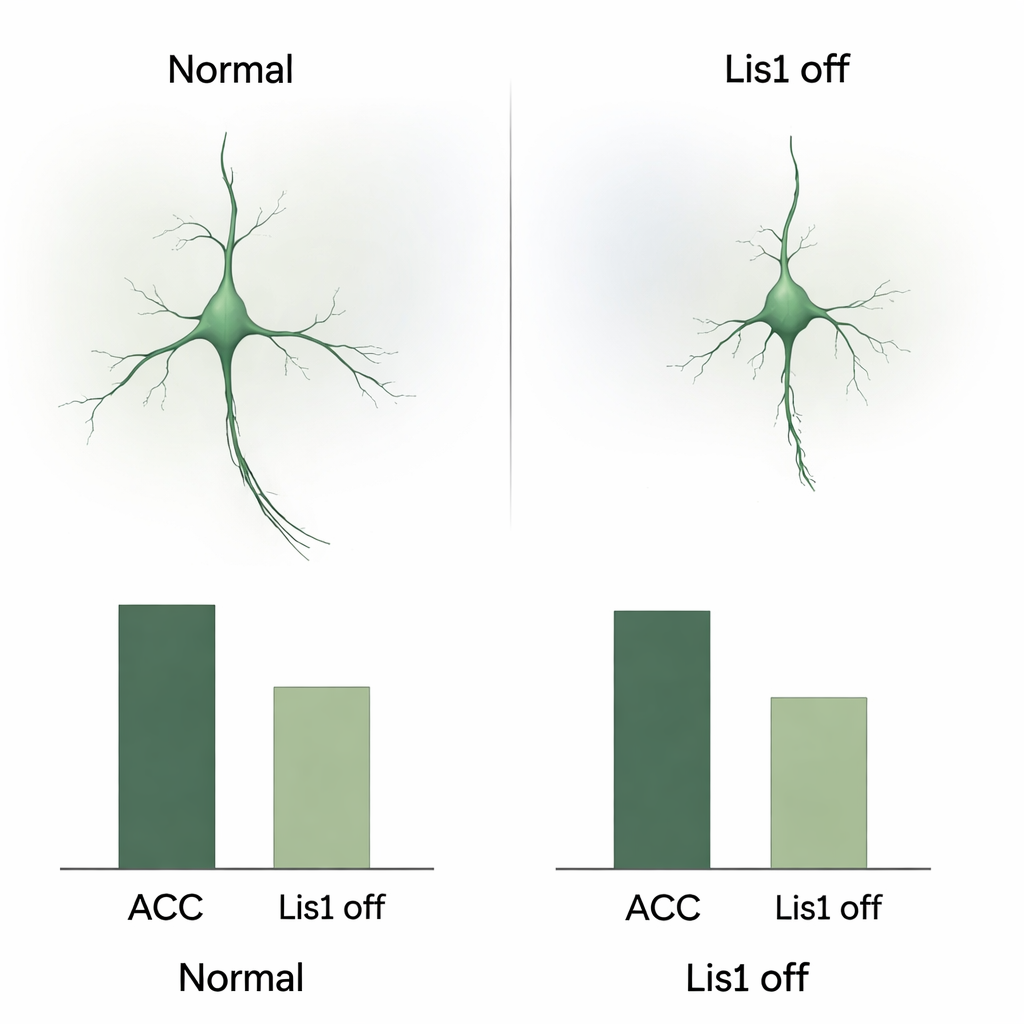
Podróż rozwojowa, która się nie powiodła
Aby zrozumieć, jak powstaje ta utrata, zespół śledził czerwono oznaczone komórki somatostatynowe w embrionach. Potwierdzili, że usunięcie Lis1 zaczyna się po zakończeniu podziałów tych komórek, co wyklucza bezpośredni wpływ na ich powstawanie. Problem pojawiał się podczas ich długiej migracji. W środkowych stadiach ciąży znacznie mniej oznaczonych komórek przemierzało normalne szlaki w kierunku kory, a wiele z nich zdawało się zatrzymywać w kresomózgowiu podstawy (basal forebrain), regionie brzusznym, który muszą przekroczyć. Migracyjne komórki, które jednak się poruszały, miały zmieniony kształt: krótsze wyrostki wiodące, mniej rozgałęzień i mniejsze, bardziej okrągłe ciała komórkowe — wszystkie te cechy wskazują na upośledzenie wewnętrznego mechanizmu transportu. W późniejszych stadiach region brzuszny u mutantów zawierał więcej komórek z markerami zaprogramowanej śmierci, co sugeruje, że wiele zatrzymanych interneuronów obumiera zanim dotrze do kory.
Co to oznacza dla zdrowia mózgu
Mówiąc wprost: gdy Lis1 jest wyłączony tylko w interneuronach somatostatynowych, wiele z tych komórek rozpoczyna normalnie podróż, lecz nie osiąga swoich ostatecznych miejsc w korze obręczy. Część gromadzi się i obumiera po drodze, a te, które docierają, są mniej liczne i nierówno rozmieszczone w warstwach kory. Ponieważ systemy somatostatynowe były wielokrotnie powiązane z depresją, schizofrenią, padaczką i chorobami neurodegeneracyjnymi, praca ta podkreśla bezpośrednią, komórkowo‑specyficzną drogę, przez którą zaburzenie funkcji Lis1 może przyczyniać się do zakłóceń rytmów mózgowych i objawów psychiatrycznych. Badanie pokazuje, że nawet umiarkowane liczebnie populacje neuronów, kierowane przez pojedynczy gen, mogą być kluczowe dla budowy zrównoważonych obwodów niezbędnych dla zdrowego myślenia i zachowania.
Cytowanie: Pombero, A., García-López, R., Geijo-Barrientos, E. et al. Selective Lis1 inactivation disrupts migration and positioning of cortical somatostatin interneurons. Sci Rep 16, 7330 (2026). https://doi.org/10.1038/s41598-026-38316-x
Słowa kluczowe: interneurony somatostatynowe, gen Lis1, migracja neuronów, <keyword>zaburzenia neurorozwojowe