Clear Sky Science · pl
Niejednorodne sieci neuronowe grafów ujawniają molekularne mechanizmy niedoboru foliatu w niewydolności łożyska poprzez integrację multiomiksową
Dlaczego to ma znaczenie dla matek i niemowląt
Folat jest najbardziej znany jako witamina w suplementach prenatalnych zapobiegająca wadom wrodzonym, jednak jego rola w zdrowej ciąży jest znacznie szersza. W tym badaniu sprawdzono, jak brak foliatu może po cichu uszkadzać łożysko — organ odżywiający i chroniący rozwijające się dziecko. Łącząc nowoczesną biologię z zaawansowaną sztuczną inteligencją, badacze pokazują, jak subtelne zmiany w genach, białkach i małych cząsteczkach współdziałają, by pozbawiać łożysko potrzebnych zasobów, i badają, jak ta wiedza mogłaby kiedyś pomóc lekarzom wcześniej wykrywać ciąże wysokiego ryzyka.
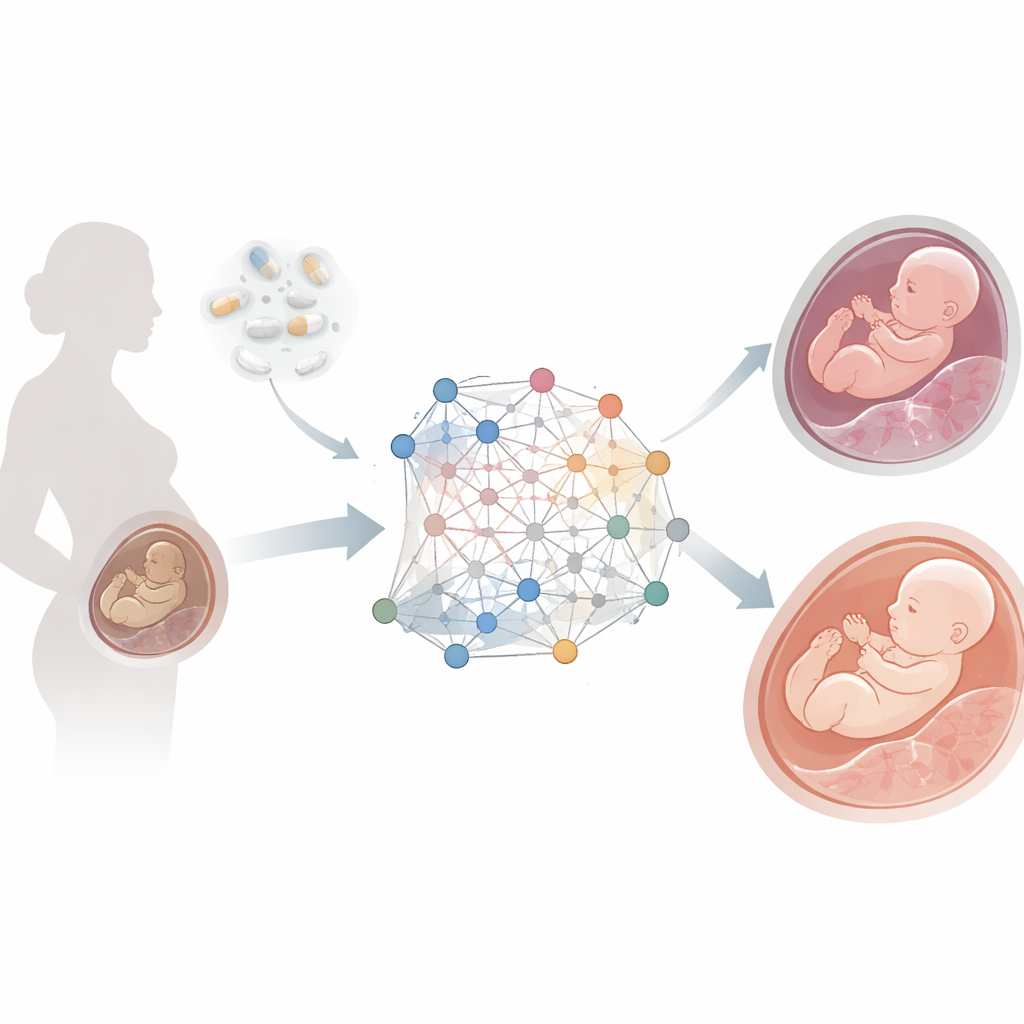
Kiedy łożysko nie nadąża
Niewydolność łożyska występuje, gdy łożysko nie dostarcza płodowi wystarczającej ilości tlenu i składników odżywczych, co prowadzi do powikłań, takich jak zahamowanie wzrostu, rzucawka ciążowa (preeklampsja) i poród przedwczesny. Dotyka ona około pięciu do dziesięciu procent ciąż na świecie. Folat stoi w centrum wielu procesów komórkowych — budowy DNA, regulacji włączania i wyłączania genów oraz wspierania zdrowia naczyń krwionośnych. Gdy poziomy foliatu są zbyt niskie, te systemy mogą zawodzić, ale precyzyjny ciąg zdarzeń zachodzących w tkance łożyska był trudny do odtworzenia. Tradycyjne badania zwykle analizują jeden rodzaj danych biologicznych naraz, na przykład geny lub metabolity, co pomija szerszy obraz interakcji między tymi warstwami.
Odczytywanie łożyska z wielu perspektyw
Aby sprostać tej złożoności, zespół zebrał próbki łożyska pobrane przy porodzie od 156 ciąż z niewydolnością łożyska związaną z folatem oraz 142 zdrowych kontroli. Z każdej próbki zmierzono cztery różne rodzaje informacji molekularnej: zmiany w DNA, aktywność genów, poziomy białek oraz małe metabolity. Zamiast traktować te pomiary jako długie, odrębne listy, powiązano je w dużą mapę biologiczną zawierającą 6 704 cząsteczki i ponad 16 000 znanych interakcji. Geny, białka i metabolity przedstawiono jako różne typy węzłów połączonych krawędziami odzwierciedlającymi, jak wiążą się, regulują lub przekształcają nawzajem w rzeczywistych komórkach.
Nauczanie inteligentnej sieci wykrywania problemów
Następnie badacze wyszkolili wyspecjalizowany model sztucznej inteligencji zwany niejednorodną siecią neuronową grafu na tej molekularnej mapie. W przeciwieństwie do standardowych algorytmów, które traktują każdy pomiar w izolacji, ten model „słucha”, jak sygnały rozchodzą się po całej sieci. Przypisuje wagi uwagi, aby wyróżnić najbardziej informatywne cząsteczki i połączenia istotne do rozróżnienia łożysk chorych od zdrowych. Na zestawie testowym model prawidłowo sklasyfikował 94,7% łożysk i osiągnął niemal doskonały pole pod krzywą ROC równy 0,978, wyraźnie przewyższając tradycyjne metody uczenia maszynowego oraz analizy oparte wyłącznie na jednym typie danych. To pokazuje, że sygnał chorobowy nie leży tylko w pojedynczych markerach, lecz w wzorcach dzielonych przez wiele warstw biologicznych.
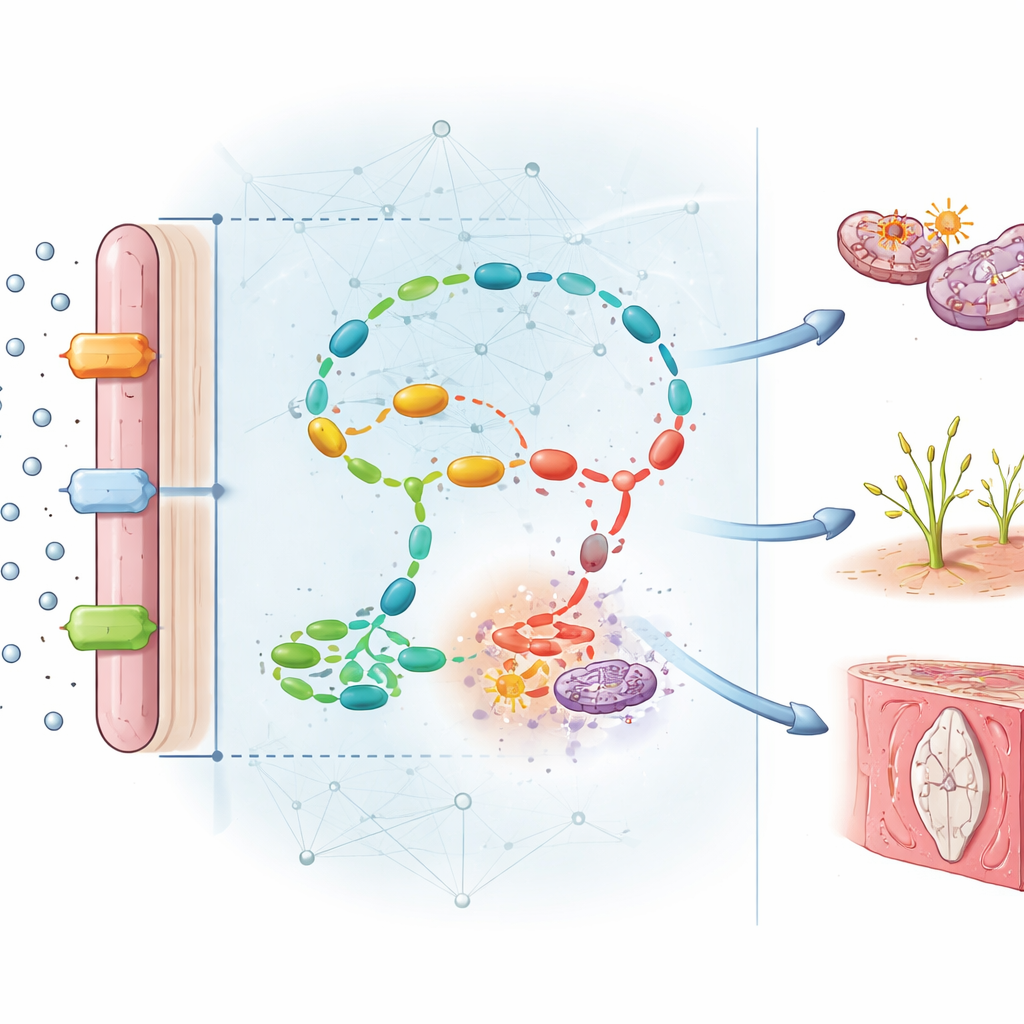
Odkrywanie ukrytych łańcuchów uszkodzeń
Ponad predykcję, konstrukcja modelu pozwoliła autorom zobaczyć, które cząsteczki miały największy wpływ na jego decyzje. Kilka z nich wyróżniało się. Kluczowe elementy obsługi foliatu — takie jak enzym MTHFR i transporter foliatu FOLR1 — były silnie zmniejszone w chorych łożyskach, podczas gdy homocysteina, toksyczny produkt uboczny, akumulowała się ponad sześciokrotnie. Z sieci wyłoniło się siedem głównych modułów funkcjonalnych, łączących zaburzoną chemię foliatu ze zmniejszeniem metylacji DNA, zwiększonym stresem oksydacyjnym, wadliwym rozwojem naczyń, stanem zapalnym i nadmierną śmiercią komórek. Inaczej mówiąc, niedobór foliatu nie szkodzi łożysku w jeden sposób; uruchamia sieć powiązanych awarii, które razem ograniczają przepływ krwi i dostarczanie składników odżywczych do płodu.
Co to może znaczyć dla przyszłej opieki
Na razie to badanie pełni głównie rolę potężnego mikroskopu, a nie testu przyłóżkowego. Ponieważ wszystkie próbki pobrano przy porodzie, model nie może jeszcze służyć do przewidywania ryzyka w trakcie ciąży, kiedy interwencja miałaby największe znaczenie. Mimo to ujawnione sygnatury molekularne — zwłaszcza skojarzone zmiany w transporcie foliatu, nagromadzenie homocysteiny i uszkodzone szlaki wzrostu naczyń — dają mapę drogową do poszukiwania markerów we krwi, które mogłyby odzwierciedlać procesy w łożysku. W przyszłych badaniach śledzących kobiety w czasie i porównujących ich krew z tkanką łożyskową, to podejście może pomóc zbudować wczesne, nieinwazyjne narzędzia przesiewowe oraz bardziej dopasowane strategie żywieniowe lub medyczne w celu ochrony narażonych ciąż.
Cytowanie: Xie, X., Li, Z., Xiao, Q. et al. Heterogeneous graph neural networks reveal molecular mechanisms of folate deficiency in placental insufficiency through multiomics integration. Sci Rep 16, 8417 (2026). https://doi.org/10.1038/s41598-026-38288-y
Słowa kluczowe: niewydolność łożyska, niedobór foliatu, sieci neuronowe grafów, multiomika, powikłania ciąży