Clear Sky Science · pl
Hamowanie szlaku SHH i ko‑kultura z astrocytami wywołują odrębne odpowiedzi w glejakach i komórkach macierzystych nowotworu
Dlaczego guzy mózgu są tak trudne do leczenia
Glejak wielopostaciowy to jeden z najgroźniejszych nowotworów mózgu — nawet przy zabiegu chirurgicznym, radioterapii i chemioterapii tylko niewielki odsetek pacjentów przeżywa ponad pięć lat. Jednym z powodów jest to, że te guzy nie składają się z jednego typu komórek. Zawierają małą grupę szczególnie opornych „komórek macierzystych nowotworu”, które potrafią przetrwać terapię i przyczynić się do nawrotu guza. W tym badaniu postawiono kluczowe pytanie: jak różne komórki guza reagują na zablokowanie sygnału wzrostowego i jak obecność normalnych komórek wsparcia mózgu, zwanych astrocytami, modyfikuje tę reakcję?
Bliższe spojrzenie na najtrudniejsze komórki guza
Naukowcy pracowali z dwoma głównymi typami komórek z modelu glejaka: komórkami masy guza oraz niewielką subpopulacją znakowaną białkiem CD133, która zachowuje się jak komórki macierzyste nowotworu. Te komórki o cechach macierzystych dzieliły się rzadziej, miały mniejsze, bardziej okrągłe kształty i tworzyły zwarte skupiska w porównaniu z komórkami masy guza. Zespół hodował również komórki nowotworowe razem z astrocytami — komórkami w kształcie gwiazdy, które pomagają utrzymać zdrową tkankę mózgową. Taka mieszanina lepiej naśladuje rzeczywiste środowisko guza, gdzie komórki nowotworowe nieustannie „rozmawiają” z sąsiadami. 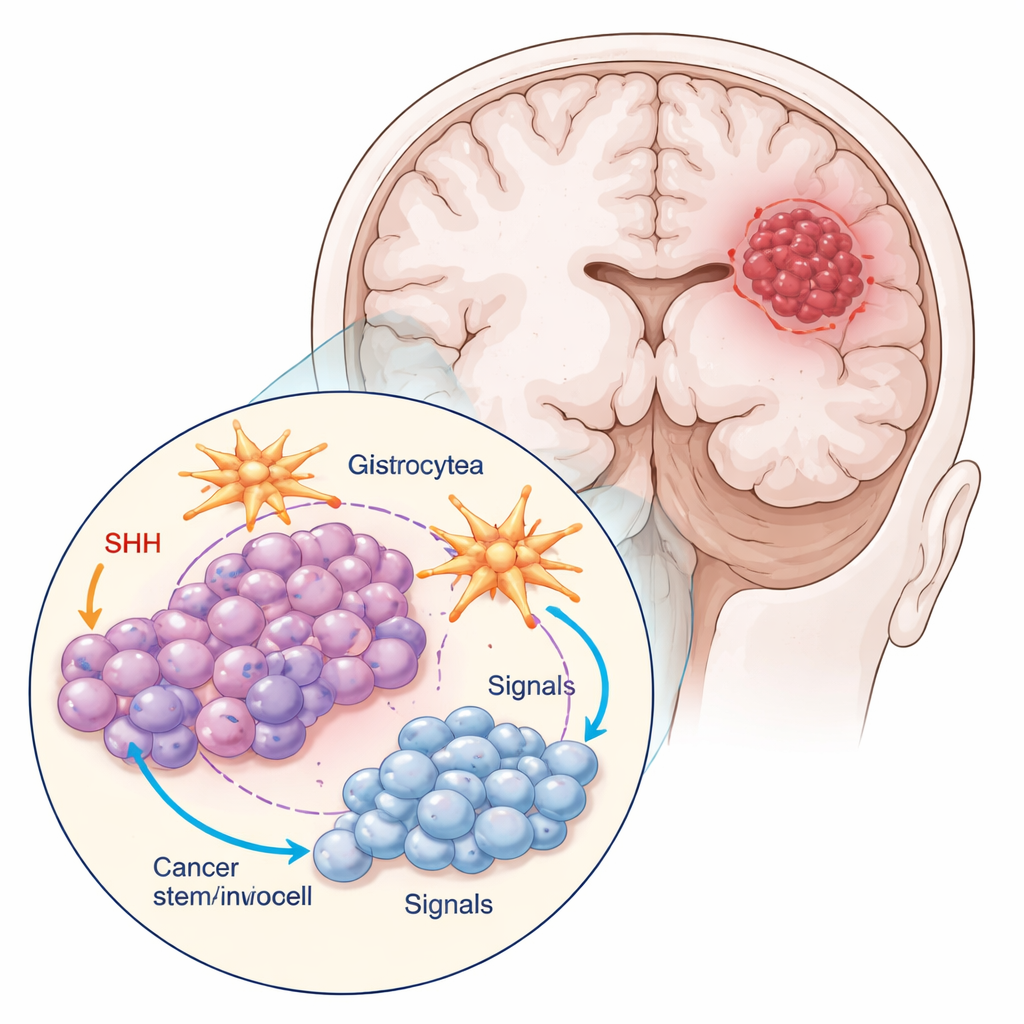
Wstrzymanie sygnału rozwojowego, którego guzy ponownie używają
Wiele glejaków, zwłaszcza ich komórek o cechach macierzystych, zawłaszcza molekularną ścieżkę komunikacji zwaną szlakiem Sonic Hedgehog (SHH), która normalnie działa podczas rozwoju mózgu. Zespół zastosował cyklopaminę — związek blokujący kluczowy składnik SHH — aby sprawdzić, jak reagują zarówno komórki masy guza, jak i komórki macierzyste nowotworu. Mierzono aktywność genów i białek związanych z SHH, tempo przechodzenia komórek przez cykl komórkowy oraz częstość zachodzenia zaprogramowanej śmierci komórkowej (apoptozy). Cyklopamina zmieniała sygnalizację SHH w sposób silnie zależny od typu komórki i obecności astrocytów. Komórki macierzyste nowotworu wydzielały najwięcej sygnału SHH, gdy były hodowane samotnie, ale ta sekrecja spadła, gdy hodowano je z astrocytami i poddano działaniu leku — co sugeruje, że otaczające komórki mózgu mogą osłabiać chemiczne „wzajemne wsparcie” guza.
Jak sąsiedztwo zmienia wzrost i śmierć
Ponad samym SHH, zespół śledził inne sieci genowe sterujące tym, czy komórki dalej się dzielą, zatrzymują, czy zaczynają różnicować. W prostych hodowlach zawierających tylko komórki guza, blokada SHH skłaniała komórki masy do zatrzymania w późnej fazie podziału (G2/M), podczas gdy komórki o cechach macierzystych gromadziły się częściej we wcześniejszej fazie spoczynkowej/rozpoczynającej (G0/G1). Po dodaniu astrocytów wzorce te uległy zmianie: komórki macierzyste, które wcześniej były bardziej uśpione, przesunęły się ku zatrzymaniu w fazie G2/M, co sugeruje inny zestaw „hamulców” działających w środowisku mieszanym. Naukowcy zaobserwowali też, że sygnały związane z przeznaczeniem komórkowym i kształtowaniem tkanki — takie jak szlaki WNT, BMP i TGF‑β — były inaczej regulowane w komórkach masy i komórkach macierzystych, gdy obecne były astrocyty, co oznacza, że mikrośrodowisko może przesuwać komórki w stronę utrzymania cech macierzystych albo ku większemu zróżnicowaniu i mniej agresywnemu fenotypowi.
Wywoływanie śmierci w najbardziej opornych komórkach
Badanie analizowało dalej skłonność komórek do apoptozy. Odczyty genetyczne i test wykrywający uszkodzenia DNA (test TUNEL) wykazały, że cyklopamina faworyzowała „zewnętrzną” drogę prowadzącą do śmierci komórki, napędzaną przez białko CASP8, szczególnie w populacji komórek macierzystych nowotworu. Co ciekawe, w komórkach guza hodowanych osobno ogólna śmiertelność czasem malała po zablokowaniu SHH, co sugeruje, że te komórki potrafią włączyć zapasowe strategie przetrwania. Natomiast gdy komórki o cechach macierzystych były ko‑hodowane z astrocytami, cyklopamina zwiększała markery apoptozy, wskazując, że otaczające komórki mózgowe mogą uczynić te inaczej oporne komórki bardziej podatnymi po zablokowaniu sygnalizacji SHH. 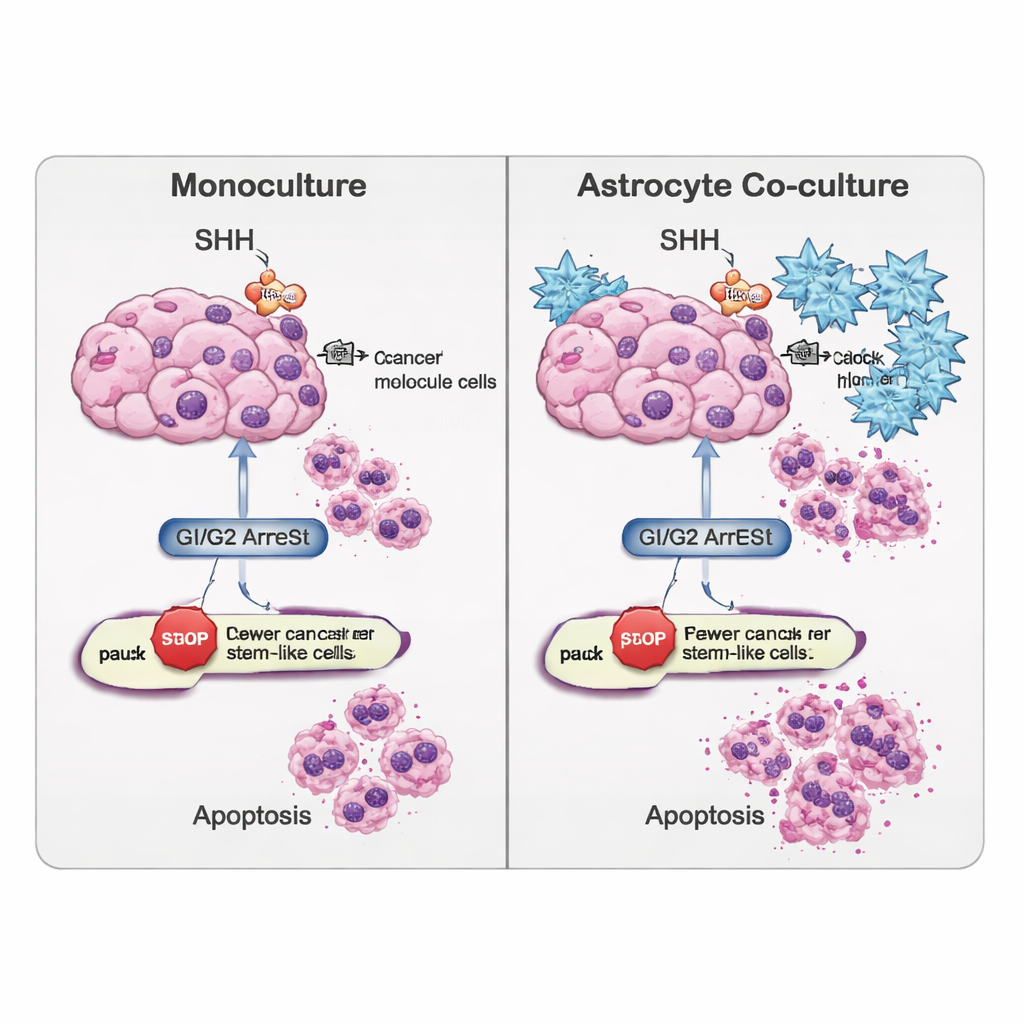
Co to znaczy dla przyszłych terapii nowotworów mózgu
Dla czytelnika nietechnicznego kluczowy wniosek jest taki, że ukierunkowanie jednego sygnału wzrostowego w glejaku nie wystarczy, jeśli ignorujemy otoczenie guza. Praca ta pokazuje, że astrocyty — normalne komórki współistniejące z guzem — mogą zasadniczo zmienić sposób, w jaki zarówno komórki masy, jak i komórki macierzyste nowotworu reagują na blokadę szlaku SHH. Szczególnie komórki macierzyste stały się bardziej skłonne do zatrzymania cyklu komórkowego i do formy śmierci komórkowej, gdy obecne były astrocyty. Autorzy wnioskują, że leki celujące w SHH i powiązane szlaki będą bardziej efektywne, jeśli będą testowane i stosowane w kontekstach odzwierciedlających prawdziwe środowisko mózgu, być może w kombinacji z innymi terapiami atakującymi zapasowe drogi przetrwania guza. Krótko: zrozumienie i wykorzystanie „rozmowy” między komórkami guza a ich sąsiadami może otworzyć drogi do bardziej precyzyjnych i trwałych strategii przeciwko temu wyjątkowo bezlitosnemu nowotworowi.
Cytowanie: Kocaturk, D.C., Ozdil, B., Adali, Y. et al. SHH pathway inhibition and astrocyte co-culture induce distinct responses in glioblastoma and cancer stem cells. Sci Rep 16, 7712 (2026). https://doi.org/10.1038/s41598-026-38199-y
Słowa kluczowe: glejak, komórki macierzyste nowotworu, szlak Sonic Hedgehog, mikrośrodowisko guza, astrocyty