Clear Sky Science · pl
Identyfikacja i walidacja nowego sygnaturowego zestawu genów związanych z ferroptozą, powiązanego z dziedziczną degeneracją siatkówki u myszy Rd10
Dlaczego umierające komórki oka mają znaczenie dla nas wszystkich
Retinitis pigmentosa to grupa dziedzicznych chorób oczu, które stopniowo odbierają wzrok — często zaczynając od ślepoty zmierzchowej i kończąc całkowitą utratą widzenia. Nie ma na nią lekarstwa, a dostępne terapie genowe pomagają jedynie niewielkiej części pacjentów. W tym badaniu przyjęto inne podejście: skupiono się na szczególnej formie śmierci komórki zwanej ferroptozą, napędzanej przez żelazo i uszkodzenia oksydacyjne, aby odkryć nowe cele genowe, które mogłyby pewnego dnia chronić komórki światłoczułe siatkówki — niezależnie od rodzaju mutacji, z którą osoba się urodziła.
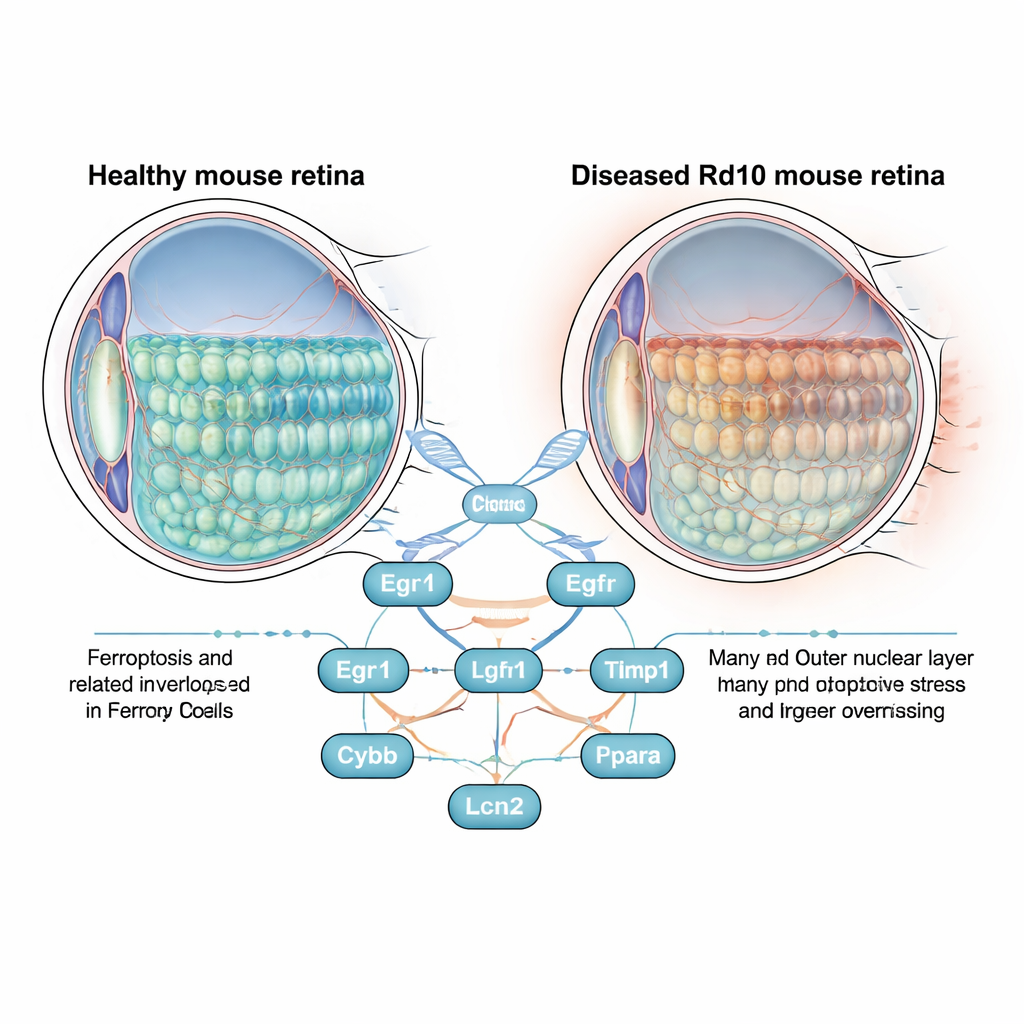
Bliższe spojrzenie na chorobę prowadzącą do ślepoty
Siatkówka to cienka warstwa tkanki z tyłu oka, zawierająca pręciki i czopki — fotoreceptory przetwarzające światło na sygnały elektryczne. W retinitis pigmentosa te komórki stopniowo obumierają, najpierw pozbawiając ludzi widzenia w nocy i peryferyjnego, a potem widzenia centralnego. Badacze często modelują ten proces na myszach Rd10, które niosą mutację dobrze odzwierciedlającą chorobę ludzką. Zamiast skupiać się wyłącznie na wadliwym genie, autorzy postawili szersze pytanie: w miarę degeneracji siatkówki, które geny związane z ferroptozą włączają się lub wyłączają i czy to one mogą napędzać utratę komórek?
Wyszukiwanie kluczowych genów w morzu danych
Zespół przeanalizował duże, publicznie dostępne zbiory danych ekspresji genów z zdrowych i Rd10 mysich siatkówek, robiąc globalne „zdjęcie” aktywności genów. Stwierdzili ponad 2000 zmienionych genów, a następnie porównali je z wyselekcjonowaną listą genów związanych z ferroptozą. To zawęziło pole do 37 kandydatów powiązanych z żelazem i oksydacyjną śmiercią komórki. Analizy komputerowe wykazały, że te geny skupiają się w procesach takich jak reakcja na stres oksydacyjny, regulacja śmierci neuronów i szlaki metabolizmu lipidów — cechy charakterystyczne ferroptozy i znane odpowiedzi na stres w degenerujących nerwach.
Osiem genów, które wyróżniają się najbardziej
Aby wskazać najbardziej wpływowe elementy, badacze zbudowali sieć interakcji białkowych i zastosowali kilka algorytmów rangowania. Wyłoniło się osiem „genów-hubów”: Egr1, Cd44, Egfr, Tlr4, Timp1, Cybb, Lcn2 i Ppara. Siedem z nich było bardziej aktywnych w chorych siatkówkach, podczas gdy Ppara wykazywał obniżoną aktywność. Wzory te potwierdzono w niezależnym zbiorze danych, a następnie badano lokalizację najważniejszych genów w oku. Przy użyciu barwienia fluorescencyjnego i sekwencjonowania RNA pojedynczych komórek wykazano, że Egr1 jest silnie zwiększony w pręcikach i czopkach, podczas gdy Cd44 jest wyraźnie podwyższony w komórkach Müllera — wspierających komórkach glejowych rozciągających się przez siatkówkę. Sugeruje to, że zestresowane fotoreceptory i ich komórki podporowe mogą współdziałać — być może w sposób szkodliwy — przez szlaki powiązane z ferroptozą.
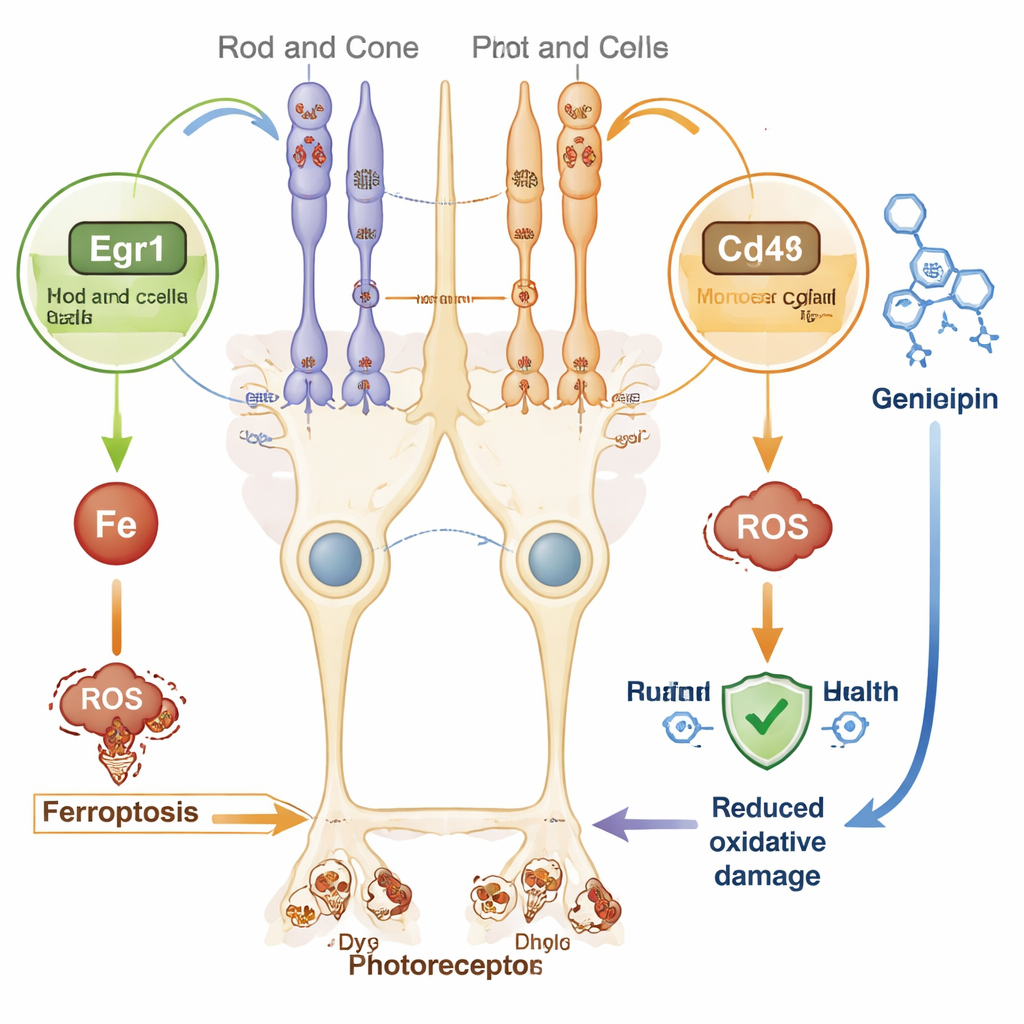
Co to oznacza dla przyszłych terapii
Ponieważ terapia genowa dopasowana do każdej wadliwej kopii genu jest skomplikowana i kosztowna, atrakcyjne są strategie o szerokim działaniu. Nowo zidentyfikowany sygnaturowy zestaw genów sugeruje kilka takich możliwości. Na przykład Egr1 to szybko działający przełącznik reagujący na stres oksydacyjny i w innych narządach może promować ferroptozę. Cd44, cząsteczka powierzchniowa komórek Müllera, w różnych tkankach wykazywała, że może pogarszać przeładowanie żelazem i śmierć komórek. Jednocześnie obniżenie Ppara, regulatora metabolizmu lipidów i wykorzystania energii, może uczynić komórki siatkówki bardziej podatnymi na uszkodzenia. Celowanie w te wspólne szlaki stresowe może umożliwić spowolnienie degeneracji siatkówki niezależnie od konkretnej formy genetycznej retinitis pigmentosa.
Leki, które mogą pomóc chronić wzrok
Korzystając z bazy danych interakcji lek–gen, autorzy poszukiwali związków, które mogłyby wpływać na Egr1 lub Cd44. Pojawiło się kilka istniejących molekuł, w tym naturalny związek genipina, który wykazał efekt ochronny w modelach choroby Parkinsona, degeneracji nerwów i retinopatii cukrzycowej przez tłumienie stresu oksydacyjnego i zapalenia. Chociaż żaden z tych kandydackich leków nie został jeszcze przetestowany w tym konkretnym modelu myszy retinitis pigmentosa, stanowią one obiecujący punkt wyjścia do dalszych badań laboratoryjnych i zwierzęcych mających na celu ochronę fotoreceptorów przed ferroptozą.
Główne przesłanie dla osób niebędących specjalistami
Praca ta pokazuje, że żelazem napędzana, oksydacyjna śmierć komórek jest ściśle powiązana ze zmianami aktywności genów obserwowanymi w klasycznym modelu dziedzicznej ślepoty. Poprzez wyróżnienie ośmiu kluczowych genów, w szczególności Egr1 reagującego na stres w fotoreceptorach i Cd44 w komórkach Müllera, badanie mapuje nowe obszary dla potencjalnych terapii niezależnych od naprawy pojedynczej zmutowanej kopii genu. Jeśli przyszłe eksperymenty potwierdzą, że łagodzenie ferroptozy przez te cele może utrzymać przy życiu komórki siatkówki, mogłoby to otworzyć drogę do terapii przynoszących korzyść szerokiej grupie pacjentów zagrożonych postępującą utratą wzroku.
Cytowanie: Qiu, X., Fu, XW., Lei, XL. et al. Identification and validation of a novel ferroptosis-related gene signature associated with inherited retinal degeneration in Rd10 mice. Sci Rep 16, 6992 (2026). https://doi.org/10.1038/s41598-026-38193-4
Słowa kluczowe: retinitis pigmentosa, ferroptoza, fotoreceptory, degeneracja siatkówki, Egr1 Cd44