Clear Sky Science · pl
Model myszy z napięciem skóry i niedotlenieniem jako model nadciśnienia płucnego grupy 3
Dlaczego to badanie ma znaczenie
Nadciśnienie płucne to poważny, często śmiertelny wzrost ciśnienia krwi w płucach. Jedna z jego najczęstszych postaci, określana jako nadciśnienie płucne grupy 3, rozwija się u osób z przewlekłymi chorobami płuc, takimi jak rozedma czy włóknienie płuc, albo u osób narażonych na długotrwałe niskie stężenie tlenu. Mimo to lekarzom nadal brakuje leków celowanych na tę jednostkę chorobową, częściowo dlatego, że naukowcy nie mieli modelu zwierzęcego, który wiernie odzwierciedlałby to, co dzieje się w ludzkich płucach. To badanie przedstawia nowy model myszy, który bardzo przypomina chorobę grupy 3, oraz ujawnia szkodliwy łańcuch sygnałowy, będący potencjalnym celem przyszłych terapii.
Mysz naśladująca uszkodzone płuca
Naukowcy skupili się na szczepie myszy znanym jako „tight-skin” (Tsk). Zwierzęta te mają mutację w białku strukturalnym zwanym fibryliną-1. Z powodu tej wady naturalnie rozwijają zmiany przypominające rozedmę i bliznowacenie w płucach, podobnie jak osoby z zaawansowaną przewlekłą chorobą płuc. Zespół porównał te myszy z normalnymi rodzeństwem, utrzymując je albo w powietrzu o normalnym stężeniu tlenu, albo w warunkach niskiego tlenu przez cztery tygodnie, by odtworzyć przewlekły niedobór tlenu doświadczany przez wielu pacjentów. 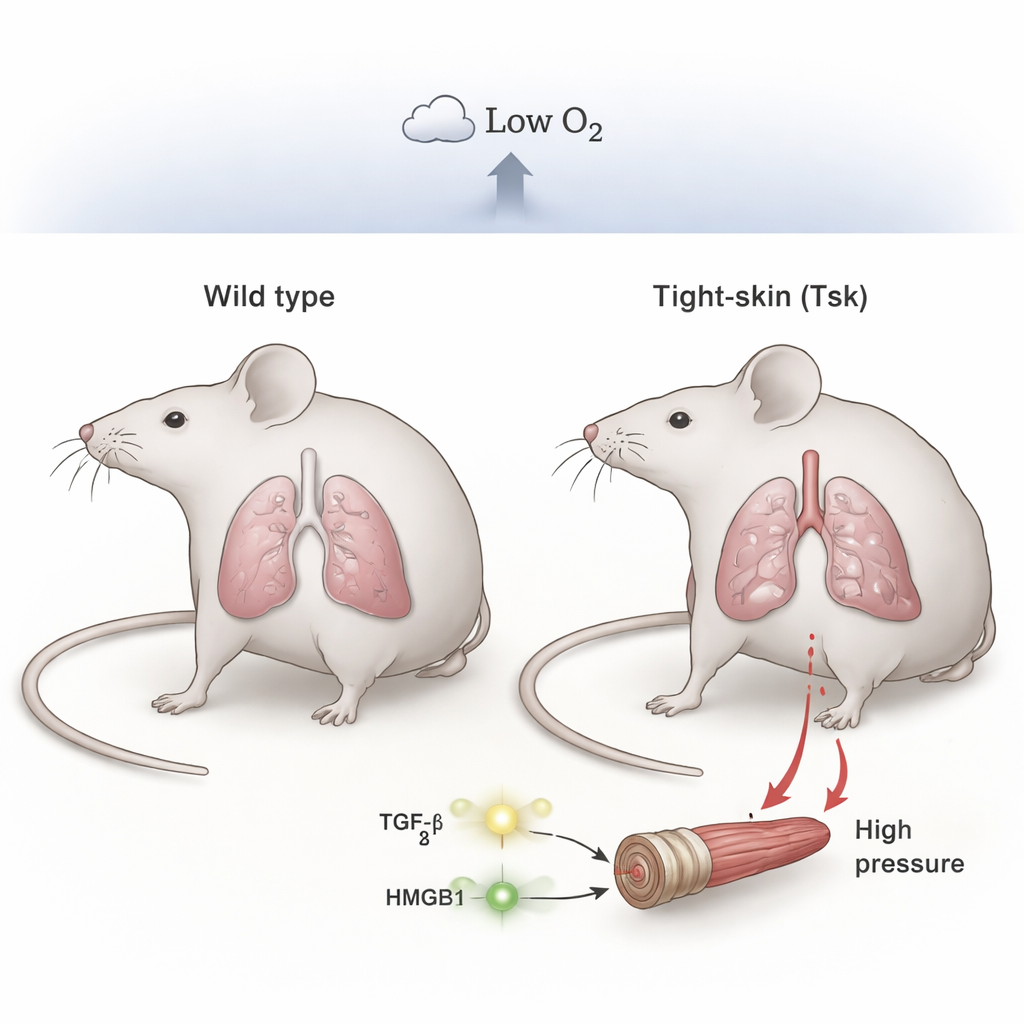
Niskie stężenie tlenu przekształca wrażliwe płuca w płuca o wysokim ciśnieniu
Gdy zarówno myszy normalne, jak i Tsk przebywały w powietrzu pokojowym, ciśnienia krwi w ich płucach były podobne i mieściły się w zakresie normalnym. Jednak w warunkach przewlekłego niedotlenienia różnice były uderzające. Myszy normalne rozwinęły tylko umiarkowane wzrosty ciśnienia, podczas gdy myszy Tsk rozwinęły ciężkie nadciśnienie płucne, z dużo wyższymi ciśnieniami po prawej stronie serca i wyraźnym pogrubieniem małych tętnic płucnych. Mikroskopia ujawniła powiększone przestrzenie oddechowe (rozedma) oraz silną muskularyzację drobnych naczyń u zwierząt Tsk, co bardzo przypomina uszkodzenia strukturalne obserwowane u pacjentów z chorobą grupy 3. Wskazuje to, że istniejące już uszkodzenie płuc wraz z niedotlenieniem razem przesuwają układ w znacznie bardziej niebezpieczny stan niż samo niedotlenienie.
Sygnał niebezpieczeństwa we krwi
Zespół zaczął badać, dlaczego myszy Tsk tak silnie reagują na niskie stężenie tlenu. Skupił się na cząsteczce zwanej HMGB1, białku pełniącym rolę „sygnału niebezpieczeństwa”, uwalnianym przez zestresowane lub uszkodzone komórki. Myszy Tsk już w stanie wyjściowym miały wyższe poziomy HMGB1 we krwi, a podczas hipoksji poziomy te jeszcze wzrastały. Podanie myszom małego peptydowego leku, P5779, który blokuje interakcję HMGB1 z jednym z jego kluczowych receptorów (TLR4), w dużym stopniu zapobiegło rozwojowi ciężkiego nadciśnienia płucnego u myszy Tsk. Leczone zwierzęta miały niższe ciśnienia w płucach, mniejsze pogrubienie naczyń i zmniejszone powiększenie prawej komory serca. Efekty ochronne były znacznie silniejsze u myszy Tsk niż u myszy normalnych, co wskazuje na HMGB1 jako centralny wzmacniacz choroby w tym modelu.
Jak sygnał wzrostu zasila sygnał niebezpieczeństwa
Kolejnym graczem w tej historii jest TGF-β, czynnik wzrostu od dawna powiązany z bliznowaceniem i przebudową w chorych płucach. Badacze stwierdzili, że myszy Tsk miały wyższą aktywność TGF-β w płucach już w stanie wyjściowym, co wykazano przez zwiększoną aktywację jego dalszego przekaźnika, SMAD-3, wokół naczyń krwionośnych. W eksperymentach na ludzkich fibroblastach adventycji tętnic płucnych — komórkach wyściełających zewnętrzną warstwę naczyń — dodanie TGF-β zwiększało produkcję HMGB1. Z kolei HMGB1 powodował proliferację zarówno tych fibroblastów, jak i sąsiednich komórek mięśni gładkich. Co ważne, efekt wzrostu zależał od receptora TLR4 i był blokowany przez P5779, ale nie przez blokowanie innego receptora HMGB1, zwanego RAGE. Razem te wyniki opisują pętlę, w której zmutowana fibrylina-1 sprzyja aktywacji TGF-β, TGF-β podnosi poziomy HMGB1, a HMGB1 napędza nadmierny wzrost komórek ściany naczyń, co zwęża tętnice płucne. 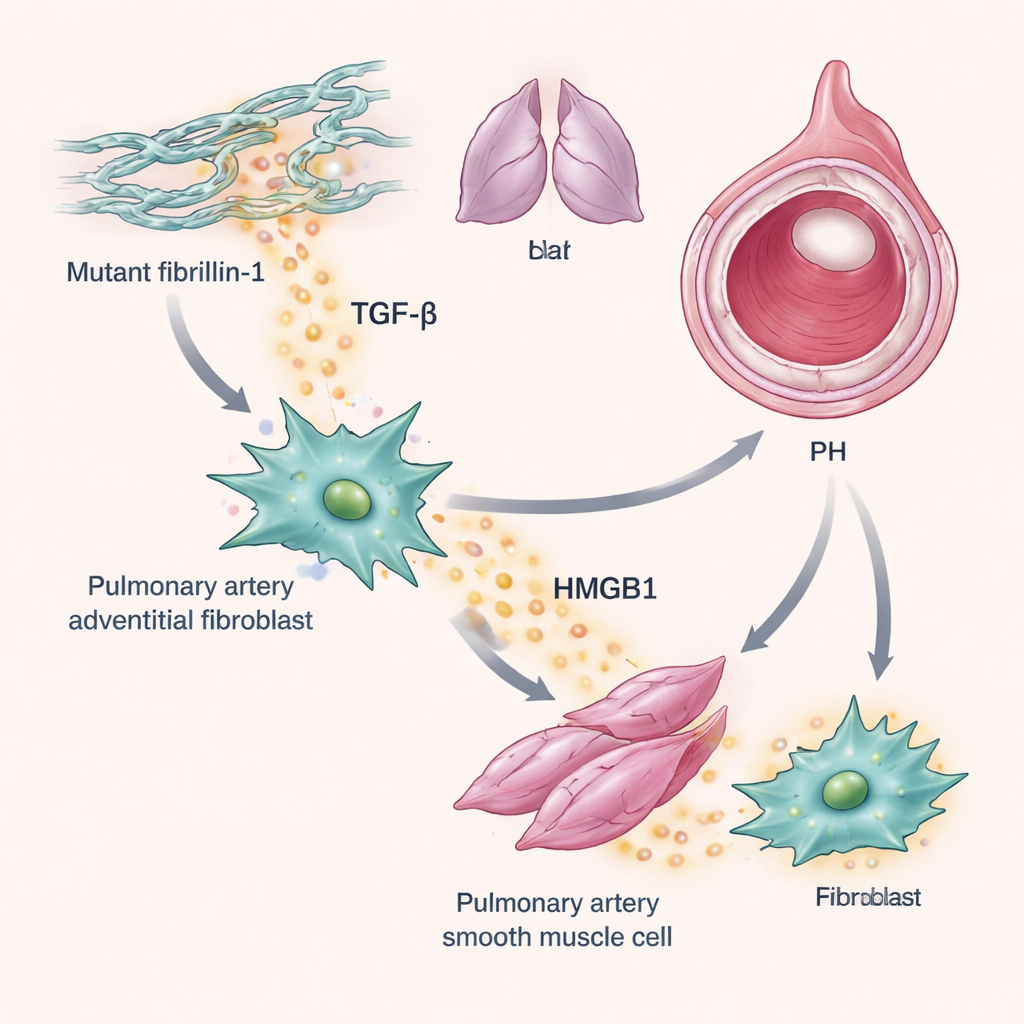
Implikacje dla pacjentów
Łącząc strukturę płuc przypominającą rozedmę z przewlekłym niedotlenieniem, model myszy tight-skin odtwarza wiele kluczowych cech nadciśnienia płucnego grupy 3, które prostsze modele oparte wyłącznie na hipoksji pomijają. Praca uwypukla szlak TGF-β–HMGB1–TLR4, który przekształca uszkodzone, niedotlenione płuca w płuca o wysokim ciśnieniu. Dla osób żyjących z przewlekłą chorobą płuc badanie to sugeruje nowe ścieżki terapeutyczne: leki tłumiące sygnalizację TGF-β lub blokujące interakcję HMGB1–TLR4, jak P5779 w modelu myszy, mogłyby w przyszłości pomóc zapobiegać lub spowalniać wzrost ciśnienia w naczyniach płucnych. Sam model stanowi także potężną nową platformę do testowania takich terapii przed wprowadzeniem ich do kliniki.
Cytowanie: Chi, L., Foley, A.E., Goodarzi, G. et al. The hypoxic tight-skin mouse model of Group 3 pulmonary hypertension. Sci Rep 16, 6968 (2026). https://doi.org/10.1038/s41598-026-38174-7
Słowa kluczowe: nadciśnienie płucne, przewlekła choroba płuc, niedotlenienie, HMGB1, TGF-beta