Clear Sky Science · pl
IL-18 promuje włóknienie trzustki poprzez uwalnianie IL-4 ze zrazikowych komórek gwiaździstych trzustki i wywołuje polaryzację makrofagów w kierunku M2
Dlaczego bliznowacenie trzustki ma znaczenie
Przewlekłe zapalenie trzustki to długotrwałe zapalenie tego narządu, które stopniowo niszczy jego strukturę, często powodując silny ból, problemy trawienne oraz zwiększone ryzyko raka trzustki. Charakterystyczną cechą choroby jest włóknienie — tkanka bliznowata zastępująca zdrowe komórki trzustki. Badanie stawia proste, lecz kluczowe pytanie: jakie sygnały wewnątrz trzustki zamieniają utrzymujące się zapalenie w trwałe bliznowacenie i czy zablokowanie tych sygnałów może spowolnić lub zatrzymać uszkodzenia?
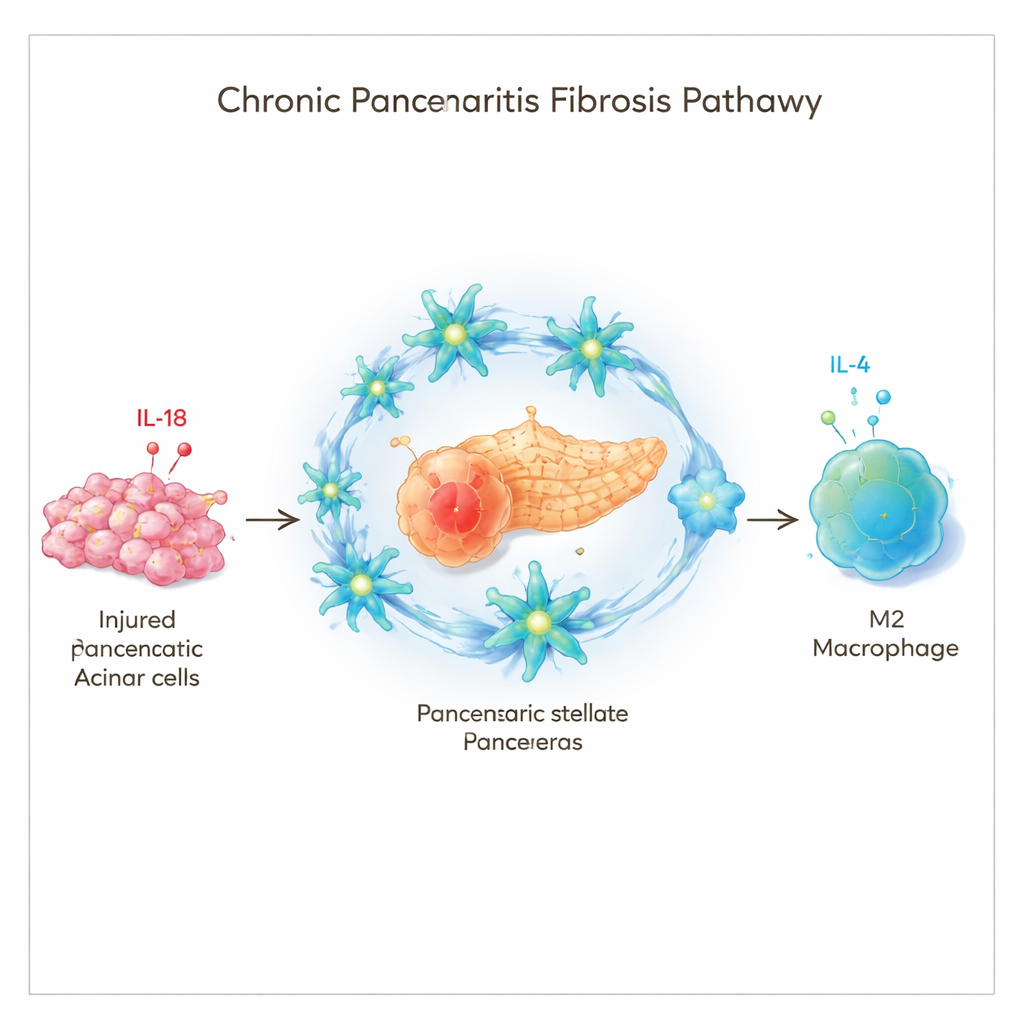
Sygnał alarmowy, który robi kłopoty
Naukowcy skoncentrowali się na cząsteczce nazywanej interleukiną‑18 (IL‑18), będącej elementem „systemu alarmowego” układu odpornościowego. Poziom IL‑18 wzrasta podczas zapalenia i powiązano go ze stwarzaniem blizn w sercu, nerkach i wątrobie. Analizując próbki tkankowe od osób z przewlekłym zapaleniem trzustki oraz stosując modele mysie choroby, zespół stwierdził, że stężenie IL‑18 jest znacznie wyższe w chorych trzustkach niż w zdrowych. Co ważne, im więcej IL‑18 w trzustce pacjenta, tym bardziej rozległe włóknienie. Głównym źródłem tego IL‑18 okazały się uszkodzone komórki acinarne — komórki produkujące enzymy trawienne — które uwalniają IL‑18 w momencie uszkodzenia.
Komórki wspierające, które przekształcają się w producentów blizn
Tkankę bliznowatą w przewlekłym zapaleniu trzustki w przeważającej mierze wytwarzają zrazikowe komórki gwiaździste (pancreatic stellate cells), rodzaj komórek podporowych, które zwykle pozostają uśpione, ale mogą przejść w aktywny, produkujący blizny stan. Badanie wykazało, że te komórki mają receptor dla IL‑18, co oznacza, że mogą bezpośrednio wyczuwać ten sygnał alarmowy. U myszy pozbawionych tego receptora powtarzające się uszkodzenia skutkowały znacznie mniejszym włóknieniem trzustki, mniejszą aktywacją komórek gwiaździstych oraz odmiennym wzorcem napływu komórek układu odpornościowego. Wskazuje to, że IL‑18 nie jest jedynie wskaźnikiem zapalenia; jest czynnikiem napędzającym, który pomaga pchać komórki gwiaździste i otaczającą tkankę w kierunku włóknienia.
Jak komórki odpornościowe są kierowane na tryb sprzyjający bliznowaceniu
Innym kluczowym graczem w przewlekłym zapaleniu trzustki jest makrofag — komórka odpornościowa, która może przyjmować różne „personalności”. W jednym stanie (często określanym jako M1) makrofagi pełnią rolę agresywnych obrońców; w innym (M2) przechodzą w tryb przebudowy tkanki i niestety mogą sprzyjać bliznowaceniu. Naukowcy odkryli, że u myszy pozbawionych receptora IL‑18 występowało mniej makrofagów typu M2 w trzustce. Co zaskakujące, sam IL‑18 nie przekształcał bezpośrednio makrofagów w typ M2 w warunkach in vitro. Zamiast tego IL‑18 działał na komórki gwiaździste, pobudzając je do wydzielania innego sygnałowego związku — interleukiny‑4 (IL‑4). IL‑4 jest dobrze znana z kierowania makrofagów w stronę stanu M2, sprzyjającego włóknieniu. Gdy makrofagi wystawiano na działanie płynu z komórek gwiaździstych traktowanych IL‑18, silnie przestawiały się na wzorzec M2 — efekt ten w dużej mierze znikał po zablokowaniu IL‑4.
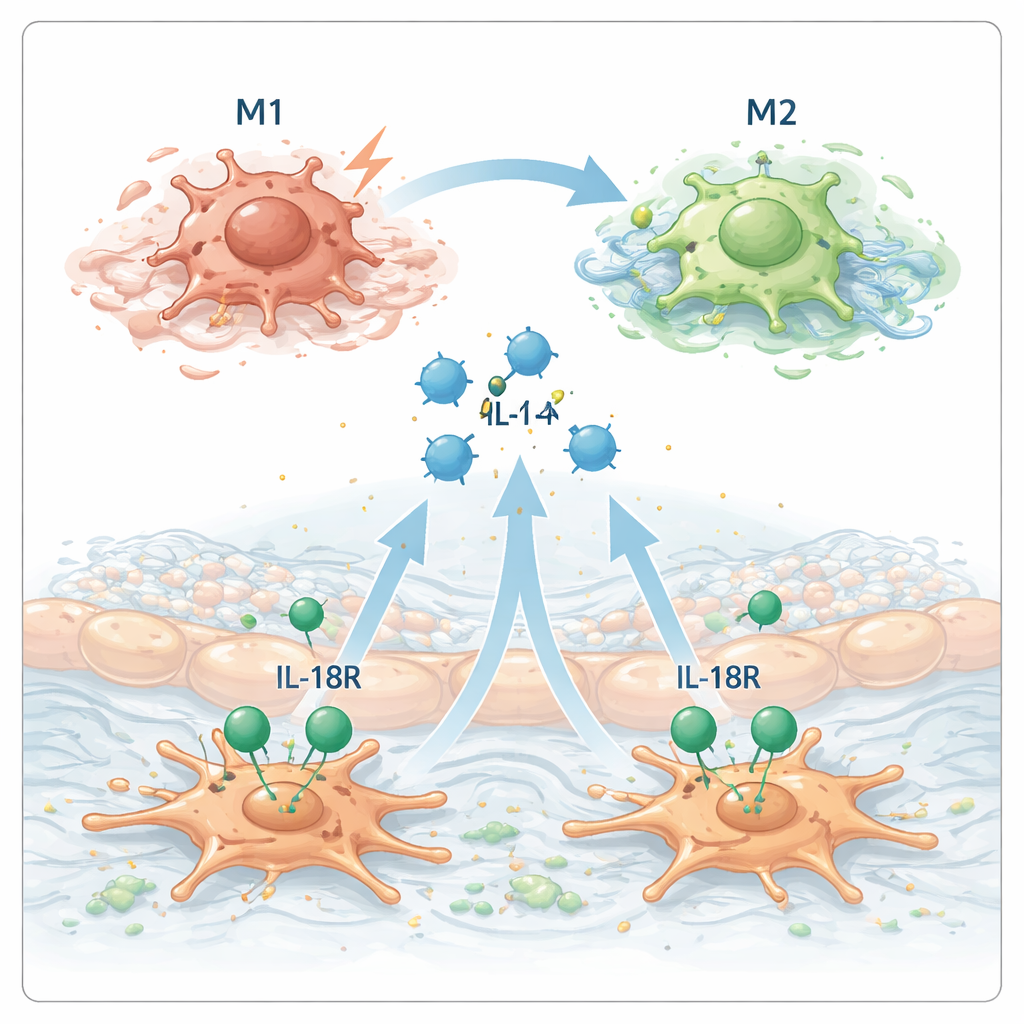
Reakcja łańcuchowa, która pogłębia bliznowacenie
Łącząc te elementy, badacze proponują reakcję łańcuchową zachodzącą w chorej trzustce. Najpierw komórki acinarne ulegają uszkodzeniu i uwalniają IL‑18. Następnie IL‑18 aktywuje pobliskie komórki gwiaździste przez ich receptor. W odpowiedzi komórki gwiaździste wydzielają IL‑4, które nakłania makrofagi do przyjęcia stanu M2 sprzyjającego bliznom. Te makrofagi M2 z kolei dodatkowo stymulują komórki gwiaździste i pomagają odkładać kolagen oraz inne składniki tkanki bliznowatej, pogłębiając włóknienie. W eksperymentach na myszach podawanie dodatkowego IL‑18 w przebiegu przewlekłego zapalenia trzustki zaostrzało chorobę i zwiększało bliznowacenie, natomiast blokada IL‑4 łagodziła te szkodliwe skutki.
Co to oznacza dla przyszłych terapii
Dla osób niebędących specjalistami najważniejszy wniosek jest taki, że bliznowacenie w przewlekłym zapaleniu trzustki nie jest przypadkowe; napędza je specyficzna komunikacja między uszkodzonymi komórkami trzustki, komórkami gwiaździstymi i komórkami odpornościowymi. IL‑18 znajduje się wysoko w tym łańcuchu sygnalnym, a IL‑4 działa jako istotny pośrednik. Przez zakłócenie działania IL‑18, jego receptora na komórkach gwiaździstych lub sygnalizacji IL‑4 do makrofagów, przyszłe terapie mogą potencjalnie zmniejszyć lub spowolnić odkładanie się tkanki bliznowatej w przewlekłym zapaleniu trzustki, zachowując funkcję trzustki i poprawiając jakość życia pacjentów.
Cytowanie: Tu, G., Peng, C., Xie, S. et al. IL-18 promotes pancreatic fibrosis via release of IL-4 from pancreatic stellate cells and induces macrophage M2 polarization. Sci Rep 16, 7540 (2026). https://doi.org/10.1038/s41598-026-38168-5
Słowa kluczowe: przewlekłe zapalenie trzustki, włóknienie trzustki, IL-18, IL-4, polaryzacja makrofagów