Clear Sky Science · pl
Potencjalny wpływ uzupełniania albuminy na modulację odporności i dynamikę sfingozyny 1‑fosforanowej
Dlaczego to ma znaczenie dla pacjentów na intensywnej terapii
Osoby przebywające na oddziałach intensywnej opieki często mają bardzo niskie stężenia białka krwi zwanego albuminą. Lekarze czasem podają infuzje albuminy, licząc na stabilizację ciśnienia krwi i poprawę przeżycia, lecz duże badania nie wykazały jednoznacznej korzyści. W tym badaniu postawiono inne pytanie: zamiast skupiać się wyłącznie na bilansie płynów, czy albumina może wpływać na układ odpornościowy przez przenoszenie w krwi małej, tłuszczopodobnej molekuły‑przekaźnika — i czy to może wyjaśniać, dlaczego niektórzy pacjenci wydają się korzystać bardziej niż inni?
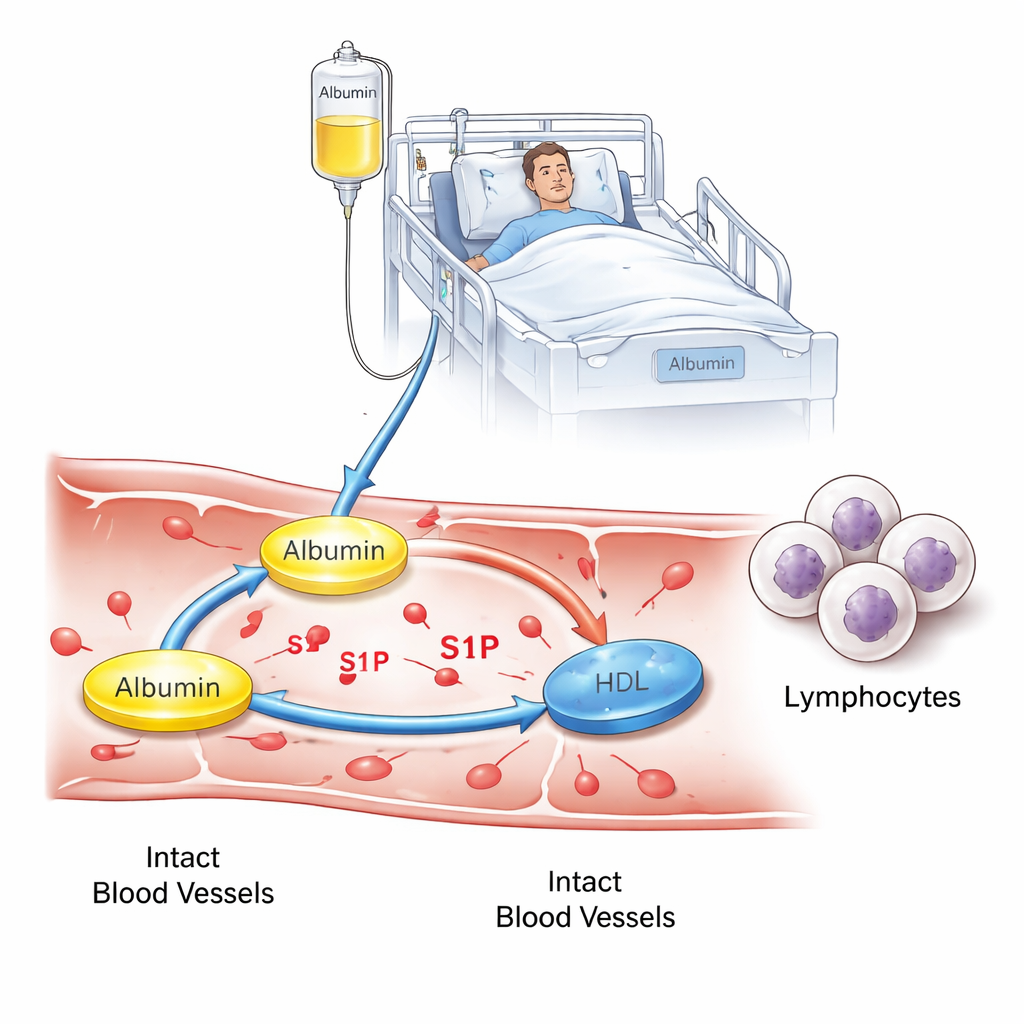
Bliższe spojrzenie na albuminę i drobnego przekaźnika
Albumina robi więcej niż tylko utrzymuje wodę w naczyniach krwionośnych. Transportuje także wiele małych cząsteczek, w tym sfingozynę 1‑fosforanową (S1P), która reguluje między innymi ruch białych krwinek po organizmie i przepuszczalność naczyń podczas ciężkiej choroby. U zdrowych osób S1P podróżuje głównie na dwóch nośnikach: albuminie i lipoproteinach o wysokiej gęstości (HDL, często nazywanych „dobrym cholesterolem”). Gdy pacjenci stają się krytycznie chorzy — szczególnie przy sepsie — zarówno poziomy albuminy, jak i HDL mogą się obniżyć, a wcześniejsze prace wykazały też spadek S1P, co wiąże się z gorszymi wynikami. Autorzy postanowili sprawdzić, czy podanie albuminy ludzkiej pacjentom OIOM z niską albuminą może zmienić dystrybucję S1P między albuminą a HDL oraz czy ta zmiana przełoży się na zmiany w komórkach odpornościowych lub stabilności naczyń.
Jak badanie przeprowadzono przy łóżku pacjenta
Zespół obserwował 47 dorosłych w jednym oddziale intensywnej terapii przez około rok. Wszyscy mieli niską albuminę, ale to ich lekarze prowadzący — nie badacze — decydowali, kto otrzyma infuzje albuminy. Na tej podstawie pacjenci zostali podzieleni na trzy grupy: małą grupę kontrolną z prawidłową albuminą, większą grupę z niską albuminą, która nie otrzymała albuminy, oraz grupę leczoną z niską albuminą, która otrzymała 180 g albuminy ludzkiej w ciągu trzech dni. Pobierano próbki krwi do standardowych badań laboratoryjnych, szczegółowego pomiaru S1P oraz oznaczeń różnych typów białych krwinek. Badacze stosowali też wyspecjalizowane metody, aby ustalić, czy S1P w każdej próbce był głównie związany z albuminą czy z HDL, a następnie przeprowadzili testy laboratoryjne, aby zobaczyć, jak osocze pacjentów wpływa na ruch białych krwinek i szczelność warstwy komórek naczyniowych.
Co się zmieniło we krwi — a co nie
Jak oczekiwano, infuzje albuminy wyraźnie podniosły stężenia albuminy we krwi w grupie leczonej, potwierdzając, że interwencja zadziałała w podstawowym sensie. Ku zaskoczeniu, całkowite poziomy S1P we krwi nie wzrosły po terapii albuminą i pozostały niższe niż u pacjentów OIOM, których albumina była prawidłowa od początku. Ważna zmiana dotyczyła jednak nośnika S1P: po leczeniu więcej S1P znajdowało się związane z albuminą, a mniej z HDL, co pokazuje mierzalną redystrybucję między nośnikami bez zmiany całkowitej ilości. Równocześnie liczby dwóch kluczowych typów komórek odpornościowych we krwi — limfocytów CD4 i komórek B — spadły w ciągu trzech dni leczenia. Ten wzorzec zgadza się z hipotezą, że zmiany w gospodarce S1P mogą modyfikować re-cyrkulację komórek odpornościowych, choć projekt badania nie pozwala udowodnić przyczynowości.
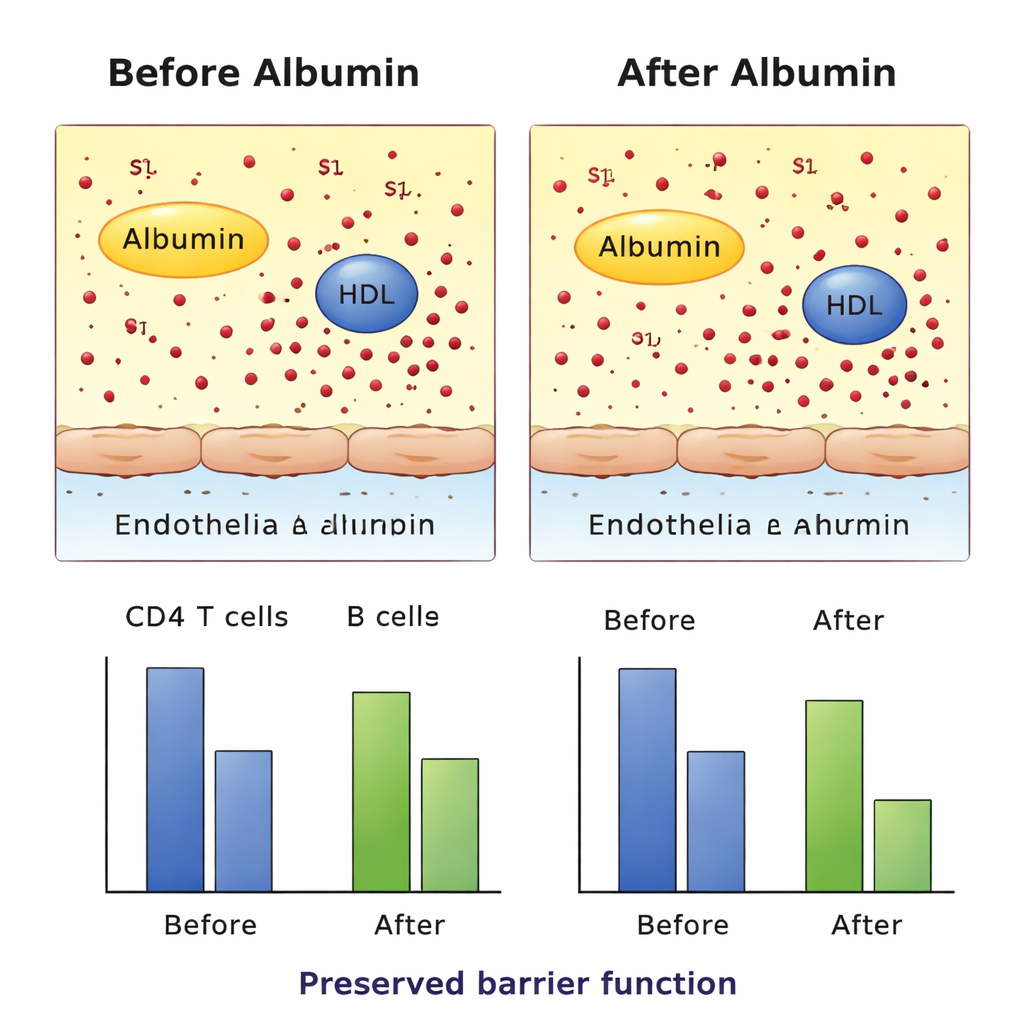
Badanie ochrony naczyń i ruchu komórek w laboratorium
Aby sprawdzić, czy ta zmiana nośnika miała szkodliwe skutki uboczne, badacze testowali próbki pacjentów w kilku kontrolowanych systemach laboratoryjnych. Narażali hodowane komórki śródbłonka na osocze z różnych grup pacjentów i monitorowali, jak dobrze warstwa komórek opiera się przepływowi prądu elektrycznego — wskaźnik szczelności bariery. Wykorzystali także test migracji, w którym fluorescencyjne komórki odpornościowe przechodziły przez membranę w kierunku osocza pacjenta, symulując „kierowanie” przez S1P. W tych eksperymentach ex vivo osocze od pacjentów leczonych albuminą nie osłabiło bariery naczyniowej i nie zmniejszyło istotnie migracji komórek napędzanej przez S1P w porównaniu z kontrolami. Dodatkowe testy na poziomie receptorów wykazały, że S1P przenoszona zarówno przez HDL, jak i albuminę nadal może aktywować swoje receptory, przynajmniej w badanych warunkach.
Co to oznacza dla przyszłych decyzji terapeutycznych
Dla osób niebędących specjalistami sedno sprawy jest takie: infuzje albuminy u bardzo chorych pacjentów nie wydają się przywracać całkowitej ilości ważnej cząsteczki‑przekaźnika S1P, ale przesuwają ją we krwi z HDL na albuminę. Ta zmiana wiąże się z subtelnymi zmianami w krążących komórkach odpornościowych, bez widocznych szkód dla stabilności naczyń w testach laboratoryjnych. Wyniki wspierają pogląd, że albumina pełni role modulujące układ odpornościowy wykraczające poza proste przyciąganie płynów do krążenia i że jej korzyści — jeśli występują — mogą dotyczyć określonych typów pacjentów, na przykład tych z bardzo niskim HDL lub silnym stanem zapalnym. Konieczne będą większe, celowane badania, aby ustalić, czy starannie wybrani pacjenci mogą odnieść istotną kliniczną korzyść z tego bardziej zniuansowanego działania terapii albuminą.
Cytowanie: Winkler, M.S., Enzmann, F., Schilder, M. et al. The potential effect of albumin replacement on immune modulation and sphingosine 1-phosphate dynamics. Sci Rep 16, 5412 (2026). https://doi.org/10.1038/s41598-026-38157-8
Słowa kluczowe: terapia albuminą, choroba krytyczna, sfingozyna 1‑fosforan, immunologia sepsy, bariera naczyniowa