Clear Sky Science · pl
Sekwencjonowanie RNA ujawnia zróżnicowaną ekspresję RNA kołowych w ludzkim drobnokomórkowym raku płuca
Dlaczego małe pętle RNA mogą zmienić opiekę nad rakiem płuca
Drobnokomórkowy rak płuca jest jednym z najgroźniejszych nowotworów — szybko się rozprzestrzenia i często opiera się chemioterapii. Lekarze wciąż nie mają dobrych testów umożliwiających wczesne wykrycie ani przewidzenie, kto odpowie na leczenie. W tym badaniu przyjrzano się nietypowej klasie cząsteczek genetycznych zwanych RNA kołowymi — małym pętelkom RNA, które w komórkach wykazują zaskakującą stabilność — aby sprawdzić, czy mają rolę w napędzaniu tego agresywnego nowotworu i czy mogłyby służyć jako nowe, bardziej wiarygodne biomarkery.
Rozumiejąc najsilniej agresywny rak płuca
Drobnokomórkowy rak płuca (SCLC) stanowi tylko około jednej piątej przypadków raka płuca, ale odpowiada za nieproporcjonalnie wiele zgonów, ponieważ rośnie szybko, wczesnie się rozprzestrzenia i zwykle nawraca po chemioterapii. Większość pacjentów jest diagnozowana w zaawansowanym stadium, gdy operacja nie wchodzi w grę, a materiał tkankowy jest ograniczony. Chociaż badacze zmapowali wiele mutacji DNA w SCLC, wiedzą znacznie mniej o tym, jak RNA niekodujące — cząsteczki, które nie kodują białek, ale silnie wpływają na zachowanie komórek — kształtują przebieg choroby. RNA kołowe (circRNA) są szczególnie intrygującą grupą, ponieważ ich zamknięta pętla sprawia, że są bardziej odporne na rozkład niż zwykłe RNA, co daje nadzieję, że można je mierzyć wiarygodnie w tkance, a nawet we krwi.
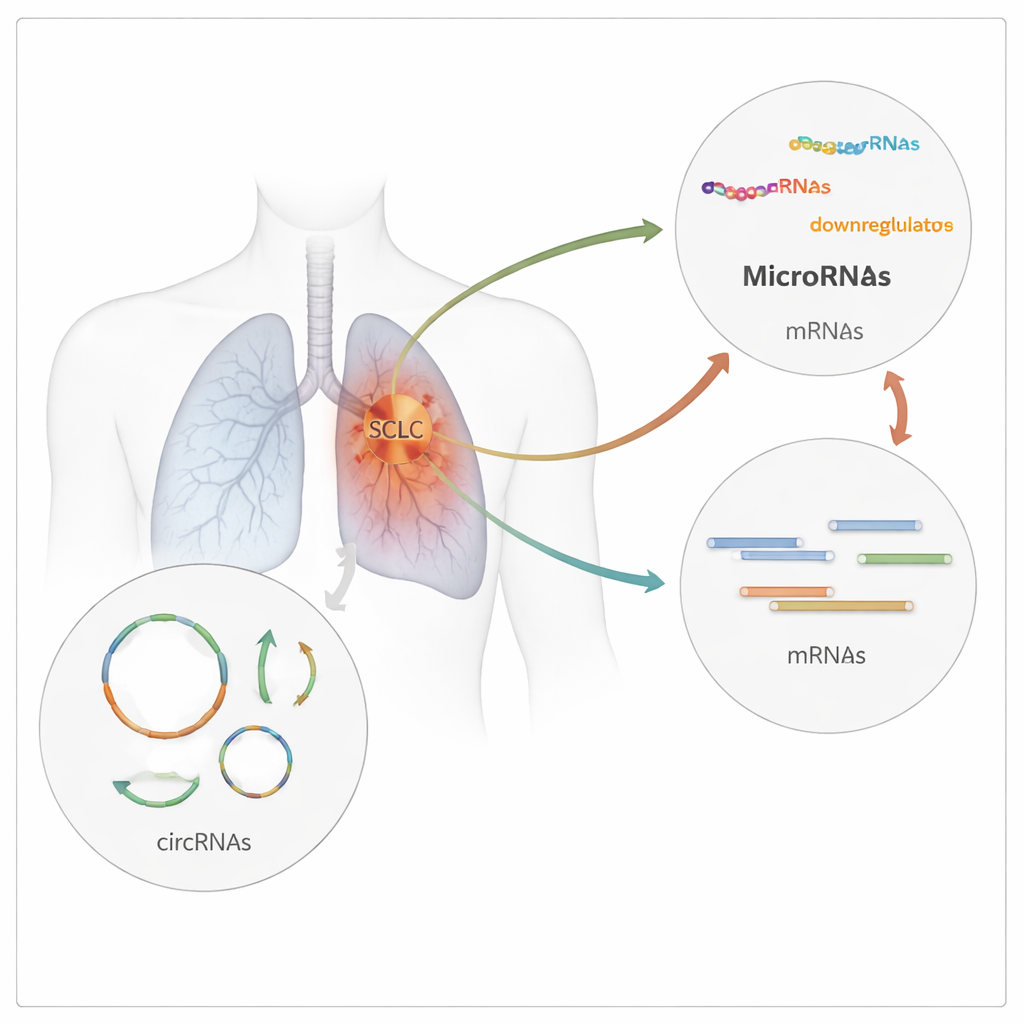
Poszukiwanie pętelek RNA w tkance guza
Zespół badawczy z Indii zebrał biopsje guza od pacjentów z nowo rozpoznanym SCLC i porównał je z normalną tkanką płuca pobraną od osób poddawanych operacji z powodu wczesnego stadium niedrobnokomórkowego raka płuca. Korzystając z wysokoprzepustowego sekwencjonowania RNA, zeskanowali ponad 26 000 złączeń, w których mogą powstawać RNA kołowe, a następnie przefiltrowali i przeanalizowali dane, aby zidentyfikować circRNA naprawdę różniące się między próbkami nowotworowymi i nienowotworowymi. Znaleźli 23 RNA kołowe, których aktywność zmieniła się istotnie w SCLC: 13 było bardziej obfitych, a 10 mniej obfitych w guzach niż w normalnej tkance płuca. Cząsteczki te pochodziły z 21 różnych genów, co sugeruje szeroką reorganizację regulacji RNA w SCLC.
Budowanie trójwarstwowej sieci kontroli RNA
RNA kołowe często działają jak molekularne gąbki, wychwytując microRNA — krótkie fragmenty RNA, które zwykle tłumią aktywność określonych genów. Aby odwzorować tę sieć kontroli, badacze wykorzystali publiczne bazy danych do przewidzenia, które microRNA mogą wiązać się z każdym z 23 zmienionych circRNA oraz które geny są prawdopodobnymi celami tych microRNA. Wynikiem była gęsta, trójwarstwowa sieć łącząca 23 RNA kołowe z 241 microRNA i około 7 800 genami kodującymi białka. Analiza funkcji tych genów wykazała, że wiele z nich skupia się wokół kontroli cyklu komórkowego, degradacji białek, reakcji na stres oraz dobrze znanych szlaków nowotworowych, takich jak p53, MAPK, Hippo i procesy starzenia komórkowego. Innymi słowy, nieprawidłowo regulowane pętelki RNA wydają się znajdować na styku kluczowych obwodów wzrostu i przeżycia w komórkach SCLC.
Dwie wyróżniające się pętelki RNA o obiecującym potencjale diagnostycznym
Spośród wszystkich zmienionych circRNA dwie wyróżniały się najbardziej. Jedna, nazwana circLIFR, była konsekwentnie zmniejszona w tkance SCLC i w kilku liniach komórkowych SCLC w porównaniu z normalnymi komórkami płuca. Jej partnerzy microRNA, w tym miR‑1234‑3p i miR‑375‑3p, byli silnie podwyższeni, co pasuje do koncepcji, że utrata gąbki z circRNA pozostawia więcej wolnych microRNA zdolnych wpływać na geny związane z rakiem. Druga pętla, circCAMSAP1, wykazywała odwrotny wzorzec: była podwyższona w guzach, podczas gdy jeden z raportowanych partnerów microRNA, miR‑145‑5p, był wyraźnie obniżony. Pacjenci, u których choroba pogorszyła się mimo chemioterapii pierwszego rzutu, mieli skłonność do wyższych poziomów circCAMSAP1, co sugeruje związek z opornością na leczenie. Gdy zespół sprawdzał, jak dobrze te cząsteczki odróżniają tkankę SCLC od normalnej tkanki płuca, circLIFR wypadł szczególnie dobrze, z miarą dokładności (AUC) powyżej 0,9, podczas gdy circCAMSAP1 i powiązane microRNA wykazywały umiarkowaną, lecz wciąż użyteczną moc diagnostyczną.
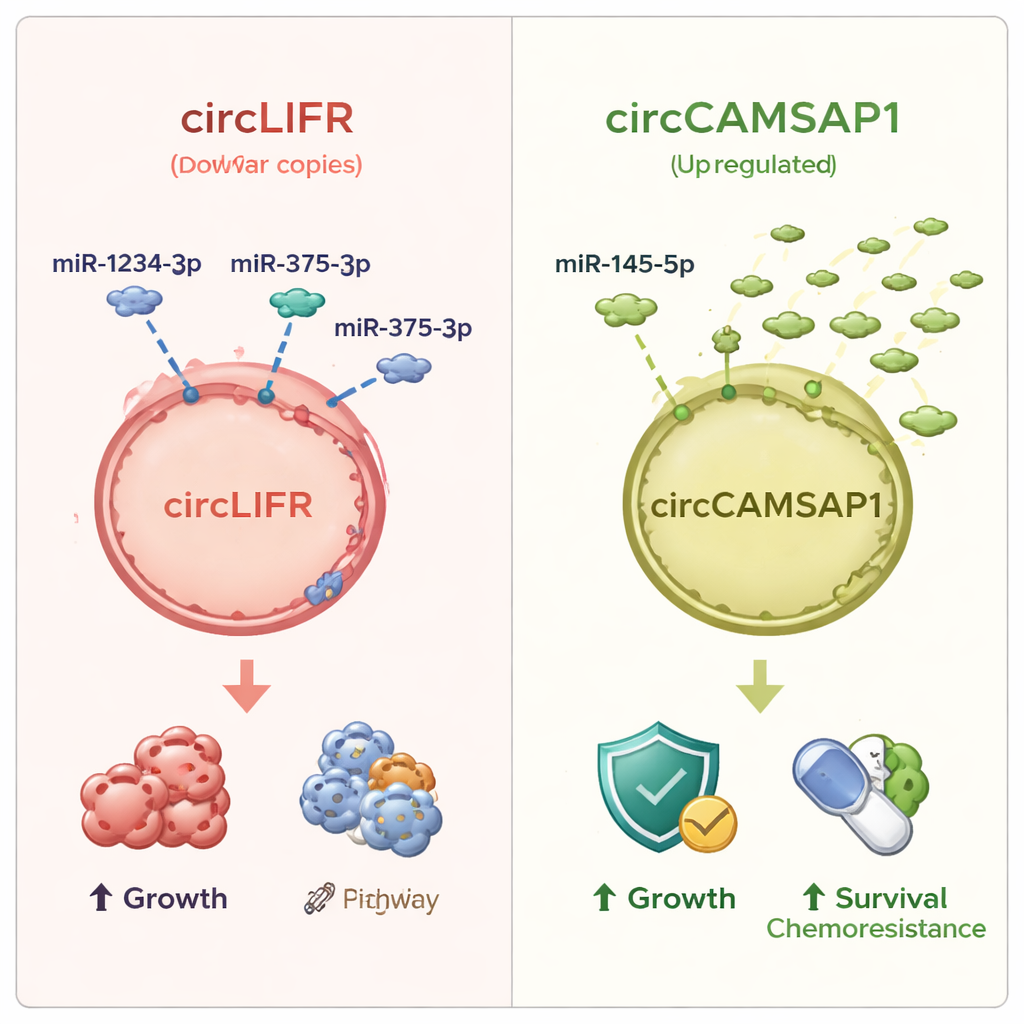
Co to może znaczyć dla pacjentów
Dla laika najważniejsze jest to, że badanie odkrywa nową warstwę kontroli w drobnokomórkowym raku płuca — zbudowaną z małych pętelek RNA i ich partnerów — która pomaga regulować tempo wzrostu komórek nowotworowych, ich odpowiedź na stres i potencjalnie zdolność przetrwania chemioterapii. Dwa konkretne RNA kołowe, circLIFR i circCAMSAP1, wyróżniają się jako obiecujące markery: jeden ma tendencję do zaniku w guzach, drugi do wzrostu, i razem z powiązanymi microRNA mogą pomóc odróżnić tkankę nowotworową od prawidłowej oraz sugerować, jak choroba pacjenta zareaguje na leczenie. Chociaż wyniki te wymagają jeszcze eksperymentów laboratoryjnych, by potwierdzić zależności przyczynowo‑skutkowe, oraz większych badań klinicznych, by przetestować ich użyteczność w praktyce, wskazują na przyszłe testy z krwi lub tkanki oparte na RNA kołowych, które mogłyby poprawić diagnozę i opiekę nad jednym z najtrudniejszych typów raka płuca.
Cytowanie: Saxena, V., Abhilash, D., Budhraja, A. et al. RNA sequencing reveals differential expression of circular RNAs in human small cell lung cancer. Sci Rep 16, 7134 (2026). https://doi.org/10.1038/s41598-026-38145-y
Słowa kluczowe: drobnokomórkowy rak płuca, RNA kołowe, microRNA, biomarkery nowotworowe, sekwencjonowanie RNA