Clear Sky Science · pl
Nanocząsteczki z albuminy surowicy bydlęcej poprawiają stabilność bakteriofagów i ich aktywność przeciwdrobnoustrojową wobec Pseudomonas aeruginosa
Dlaczego warto chronić pożyteczne wirusy
W miarę jak narasta oporność na antybiotyki, lekarzom coraz trudniej leczyć groźne zakażenia. Jednym z uporczywych sprawców jest Pseudomonas aeruginosa — bakteria często atakująca płuca osób z osłabioną odpornością, potrafiąca opierać się wielu lekom. W tym badaniu sprawdzono kreatywną strategię: użycie „przyjaznych” wirusów atakujących bakterie, zwanych bakteriofagami, i zabezpieczenie ich wewnątrz mikroskopijnych białkowych pęcherzy wykonanych z powszechnego białka krwi — albuminy surowicy bydlęcej (BSA). Celem jest utrzymanie stabilności i aktywności tych wirusów na tyle długo, by skuteczniej zwalczać trudne zakażenia płuc.
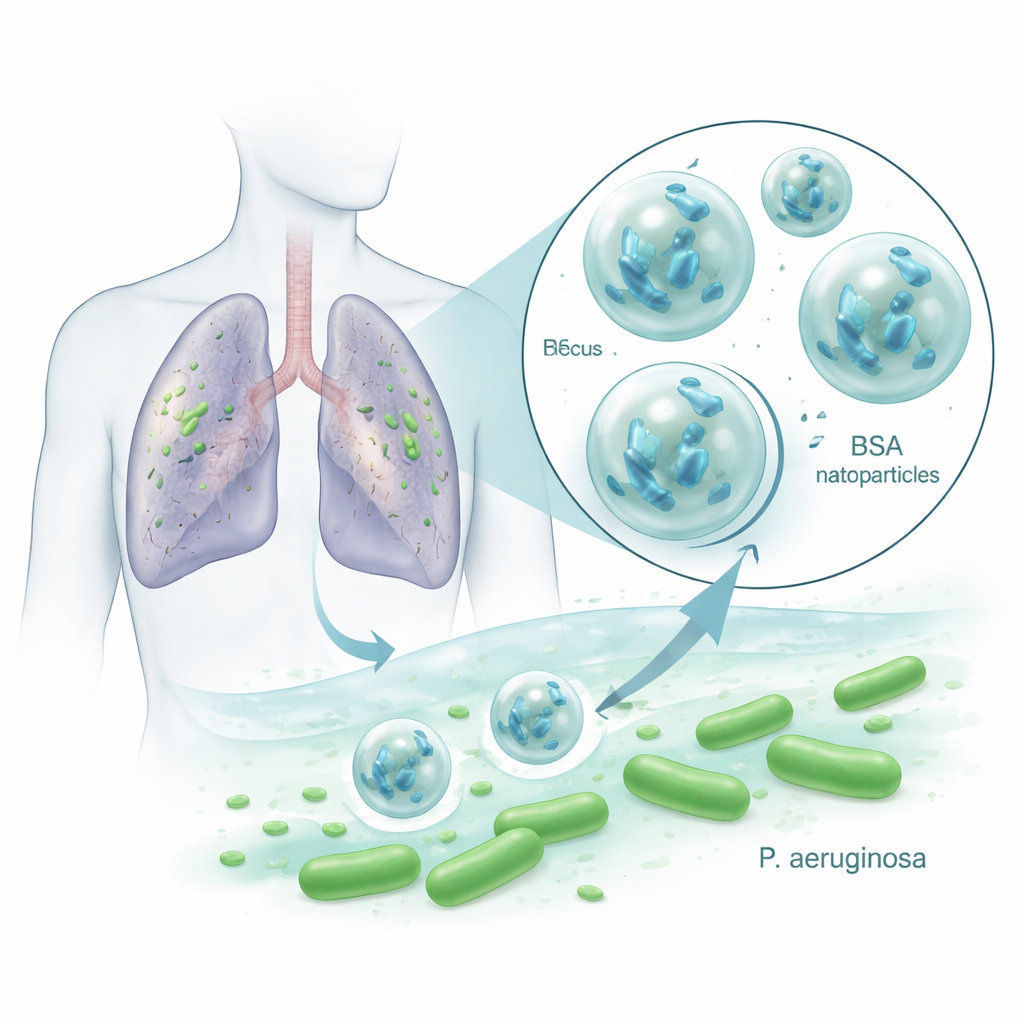
Maleńcy sojusznicy przeciw uporczywym drobnoustrojom płuc
Pseudomonas aeruginosa jest znana ze szpitali z uwagi na wielolekooporność i zdolność tworzenia śluzowych biofilmów, które chronią ją przed leczeniem. Bakteriofagi, czyli fagi, to wirusy infekujące i rozrywające określone bakterie, przy czym komórki ludzkie i korzystne mikroby pozostają w dużej mierze nietknięte. Fagi mogą się namnażać tam, gdzie obecny jest ich bakteryjny gospodarz, co czyni je atrakcyjnym uzupełnieniem lub alternatywą dla antybiotyków. Jednak fagi są kruche: wysoka temperatura, kwaśne środowisko, enzymy i odpowiedź immunologiczna szybko je inaktywują, co ograniczało ich skuteczność u pacjentów. Badacze zapytali, czy zapakowanie fagów VAC1 zabijających Pseudomonas wewnątrz nanocząsteczek BSA mogłoby je chronić i zwiększyć skuteczność terapii.
Budowa ochronnej białkowej powłoki
Zespół musiał najpierw zaprojektować cząsteczkę, która nie zaszkodzi fagowi. Testowali powszechnie stosowane rozpuszczalniki do formowania nanocząsteczek BSA i stwierdzili, że etanol i metanol niszczyły VAC1, podczas gdy aceton nie — dlatego użyli acetonu w procesie. Zmieszali fag z roztworem BSA, a następnie ostrożnie dodawali aceton, by białko skondensowało się w nanoskopijne sfery, stabilizując je związkiem sieciującym. Te nośniki z fagiem, nazwane NPPha, miały średnio około 220 nanometrów średnicy — znacznie mniej niż komórka ludzka — i uwięziły ponad 95% fagów wewnątrz. Obrazy w mikroskopii elektronowej wykazały nieregularne cząsteczki BSA zawierające gęstsze obszary, prawdopodobnie odpowiadające fagom, a testy potwierdziły, że aktywne wirusy były powoli uwalniane przez co najmniej dwa dni w temperaturze ciała, bez utraty zakaźności.
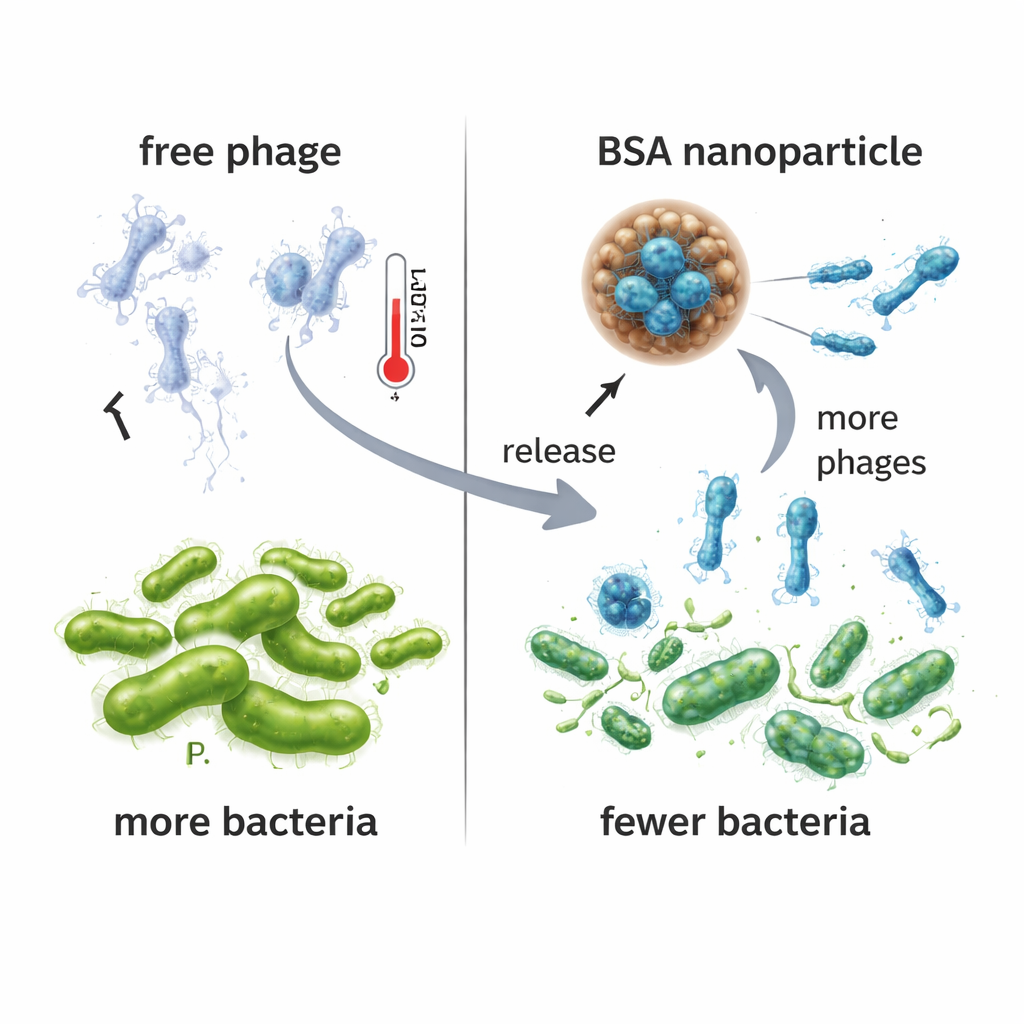
Silniejsza moc zabijania bakterii w laboratorium
Następnie badacze porównali, jak wolny VAC1 i NPPha kontrolują Pseudomonas w hodowlach płynnych. Gdy bakterie były eksponowane na NPPha, ich wzrost był tłumiony znacznie skuteczniej niż przy tej samej dawce samego faga lub pustych nanocząsteczek. W ciągu 24 godzin kultury traktowane NPPha wytwarzały około sto tysięcy razy więcej nowych cząstek fagowych niż kultury z wolnym VAC1, co sugeruje, że stałe uwalnianie z nanocząsteczek tworzyło dłużej trwającą walkę wirus–bakteria. Co ważne, nanocząsteczki BSA — zarówno wypełnione fagiem, jak i puste — nie uszkadzały komórek pochodzenia wątrobowego człowieka w testach toksyczności, co przemawia za ich potencjalnym bezpieczeństwem jako nośnika. Eksperymenty stabilności w 37 °C wykazały, że wolny fag szybko tracił aktywność w ciągu dwóch dni, podczas gdy fag wewnątrz NPPha pozostawał zakaźny nawet do pięciu dni.
Testy podejścia na zakażonych myszach
Aby sprawdzić, czy korzyści te przenoszą się na organizmy żywe, zespół wykorzystał model myszy z ostrym zakażeniem płuc Pseudomonas. Myszy zostały zakażone przez nos, a godzinę później leczone NPPha, wolnym VAC1, pustymi nanocząsteczkami lub roztworem soli. W tym bardzo ciężkim modelu wszystkie zwierzęta, niezależnie od leczenia, zmarły w ciągu 12 godzin, więc przeżywalność się nie poprawiła. Jednak przy badaniu płuc okazało się, że myszy otrzymujące NPPha miały mniej bakterii i częściej wykrywano w nich obecne fagi niż u zwierząt leczonych wolnym VAC1. Preparaty tkankowe z płuc traktowanych NPPha wykazywały mniej uszkodzeń strukturalnych, cieńsze przegrody między pęcherzykami płucnymi i mniejsze nagromadzenie komórek zapalnych w porównaniu z innymi zakażonymi grupami, co wskazuje, że zakażenie zostało w pewnym stopniu stłumione, choć nie wystarczająco, by uratować zwierzęta w tych surowych warunkach.
Co to oznacza dla przyszłych terapii zakażeń
Dla osób niebędących specjalistami kluczowa wiadomość jest taka, że zapakowanie bakteriofagów w malutkie białkowe pęcherzyki może utrzymać je przy życiu i w pełni aktywnymi przez dłuższy czas, co pomaga im skuteczniej atakować trudne do leczenia bakterie, takie jak Pseudomonas aeruginosa. W doświadczeniach in vitro i w płucach myszy nanocząsteczki BSA zwiększały liczebność fagów, hamowały wzrost bakterii i zmniejszały uszkodzenia płuc, choć nie zapobiegły śmierci w bardzo agresywnym modelu zakażenia. Praca sugeruje, że nanocząsteczki albuminowe oferują prosty, niedrogi i pozornie bezpieczny sposób stabilizacji fagów terapeutycznych. Przy dopracowanym dawkowaniu, harmonogramie podawania i ewentualnym zastosowaniu w mniej ekstremalnych lub przewlekłych zakażeniach takie nanopakietowane fagi mogłyby stać się cennym narzędziem obok antybiotyków w walce z bakteriami wielolekoopornymi.
Cytowanie: Cunha, G.A.d., Marangoni, G.S., Durante, M.F.R. et al. Bovine serum albumin nanoparticles improve bacteriophage stability and antimicrobial activity against Pseudomonas aeruginosa. Sci Rep 16, 7146 (2026). https://doi.org/10.1038/s41598-026-38106-5
Słowa kluczowe: terapia fagowa, nanocząsteczki, Pseudomonas aeruginosa, oporność na antybiotyki, infekcja płuc