Clear Sky Science · pl
Obinutuzumab wywołuje destabilizację lizosomalną poprzez zależne od sfingomieliny hamowanie TRPML2
Dlaczego ta historia przeciwciała ma znaczenie
Dla wielu osób z chłoniakami komórek B nowoczesne leki oparte na przeciwciałach przekształciły niegdyś niemal zawsze śmiertelną diagnozę w chorobę możliwą do leczenia. Nie wszystkie jednak przeciwciała są jednakowe: niektóre zabijają komórki nowotworowe silniej i bardziej niezawodnie niż inne. Artykuł ten bada, dlaczego jeden z takich leków, obinutuzumab, lepiej zabija bezpośrednio komórki chłoniaka niż jego poprzednik rytuksymab, przyglądając się nieoczekiwanemu sprawcy głęboko wewnątrz komórki — własnym centrom recyklingu komórkowego, zwanym lizosomami, oraz delikatnej równowadze tłuszczów i kanałów jonowych w ich błonach.
Od celu na powierzchni do wewnętrznego samozniszczenia
Zarówno rytuksymab, jak i obinutuzumab rozpoznają ten sam cel na komórkach B, białko zwane CD20. Autorzy wykazują jednak, że obinutuzumab jest pobierany do wnętrza komórki znacznie szybciej i wydajniej. Po związaniu z CD20 na powierzchni komórki nowotworowej kompleksy przeciwciało–receptor są wciągane do wnętrza przez proces endocytozy i dostarczane do kwaśnych przedziałów, w tym lizosomów. Tam obinutuzumab wywołuje przepuszczalność błony lizosomalnej: zazwyczaj wytrzymała błona lizosomu staje się nieszczelna, co pozwala enzymom trawiennym, takim jak katepsyny, wydostać się do wnętrza komórki i uruchomić szlaki prowadzące do jej śmierci. Zmiany w równowadze soli i wody w tych przedziałach, które powodują pęcznienie lizosomów, znacząco wzmacniają ten śmiertelny efekt.
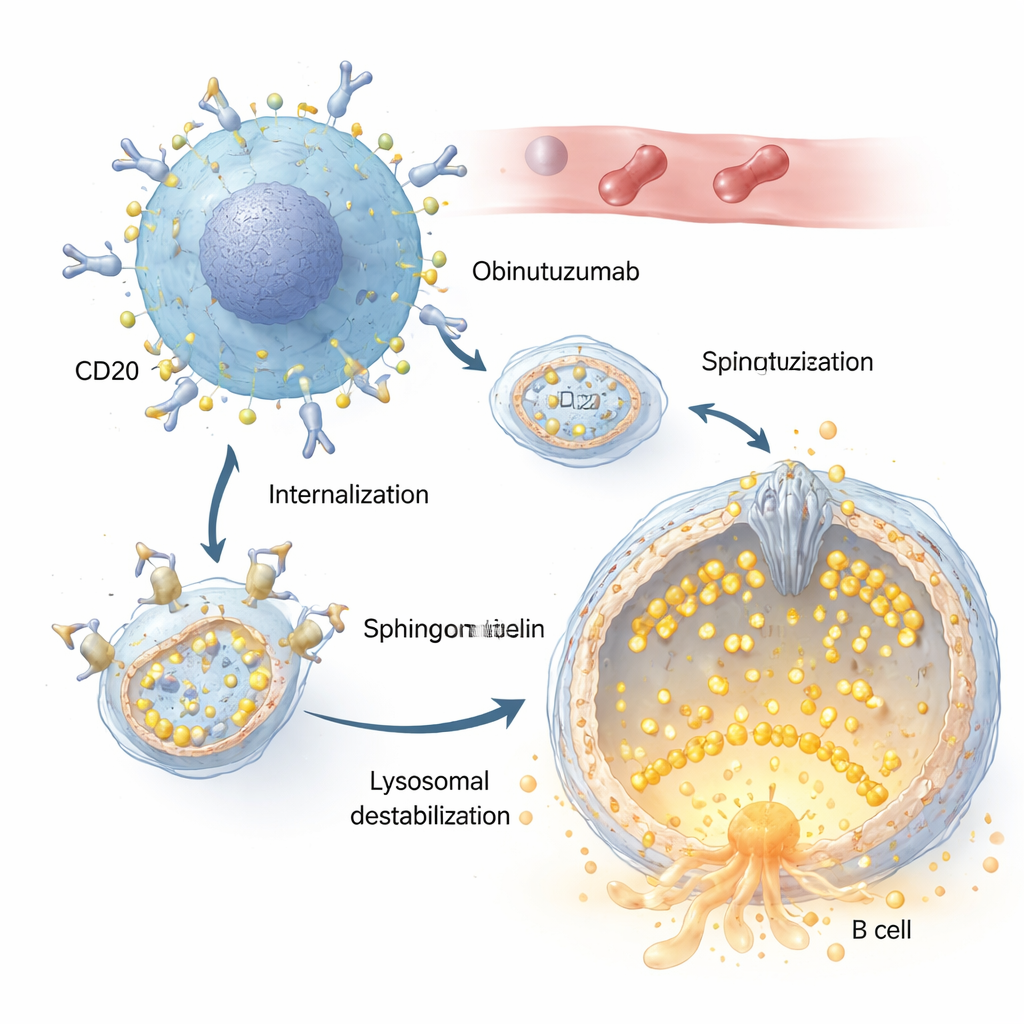
Rola maleńkiego kanału strażnika
W centrum tej opowieści stoi TRPML2, kanał wapniowy osadzony w błonie lizosomalnej. W normalnych warunkach TRPML2 pomaga lizosomom radzić sobie ze stresem mechanicznym i osmotycznym poprzez uwalnianie wapnia, co wspiera naprawę błony, transport i kontrolę objętości. Korzystając z kombinacji fluorescencyjnych barwników wapniowych i zmodyfikowanych, czułych na wapń wariantów TRPML2, badacze pokazują, że obinutuzumab szybko wyłącza ten kanał: w ciągu minut od zastosowania lek, który zwykle otwiera kanały TRPML, przestaje wywoływać wyrzut wapnia. Podejścia genetyczne obniżające poziom TRPML2 lub małocząsteczkowe inhibitory blokujące aktywność TRPML sprawiają, że komórki chłoniaka stają się bardziej podatne na obinutuzumab, co prowadzi do większego wycieku lizosomalnego i wyższych wskaźników bezpośredniej śmierci komórek.
Jak tłuszcze błonowe przechylają szalę
W dalszej części badania pytano, co łączy pobieranie przeciwciała z wyłączeniem kanału. Uwagę zwrócono na sfingomielinę, lipid (tłuszcz) obfity w błonach komórkowych, znany z interferencji z kanałami TRPML. Przy użyciu fluorescencyjnego sondy wiążącej sfingomielinę autorzy stwierdzili, że pęcherzyki zawierające obinutuzumab są bogate w sfingomielinę po dotarciu do kwaśnych przedziałów, znacznie bardziej niż pęcherzyki zawierające rytuksymab. Gdy komórki traktowano sfingomielinazą, enzymem usuwającym sfingomielinę, aktywność uwalniania wapnia przez TRPML2 została przywrócona nawet w obecności obinutuzumabu. W tych warunkach lizosomy były mniej podatne na wycieki, a mniej komórek ginęło, co silnie sugeruje, że nagromadzona sfingomielina dezaktywuje TRPML2 i przygotowuje lizosomy do pęknięcia.
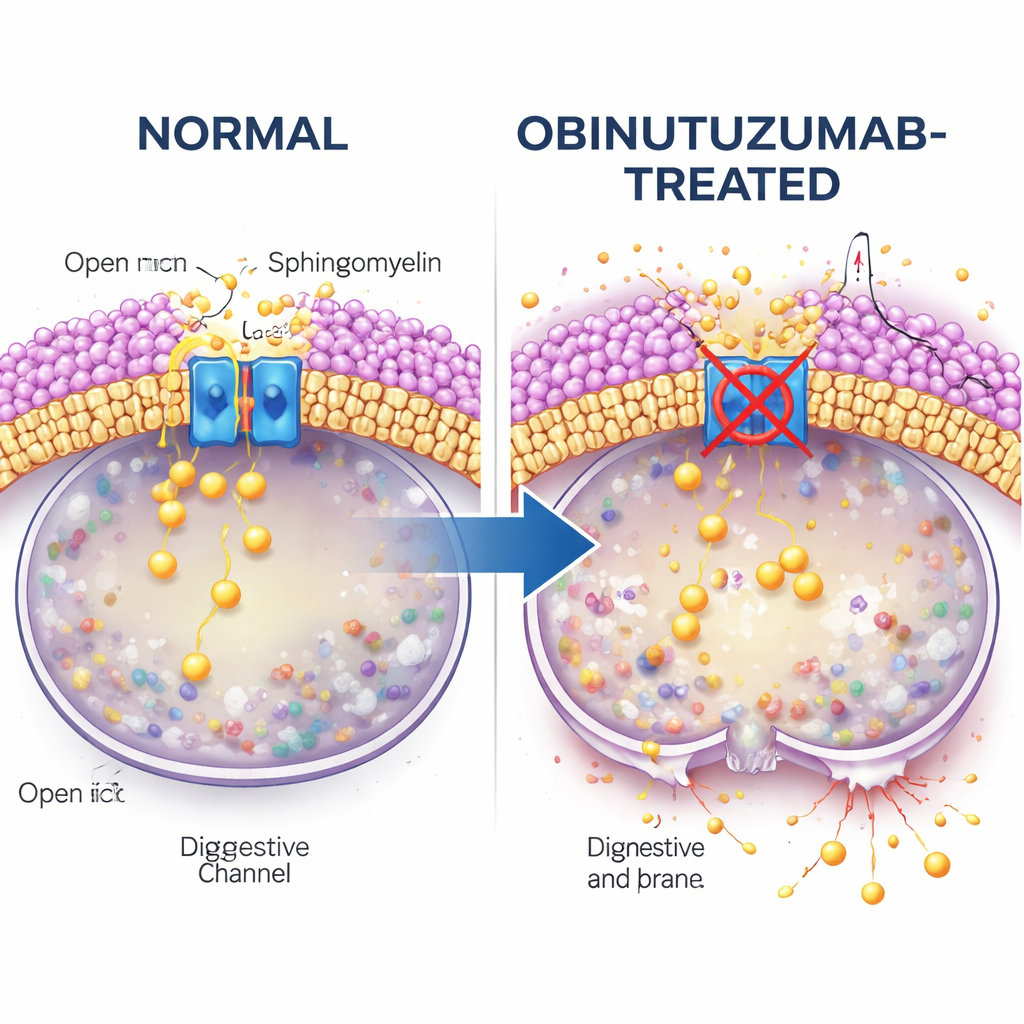
Trasy transportu i punkty kontrolne cholesterolu
Również droga, jaką obinutuzumab przebywa do wnętrza komórki, ma znaczenie. Mikroskopia elektronowa i znakowanie przeciwciał czułych na pH ujawniają, że obinutuzumab szybciej opuszcza powierzchnię komórki i trafia do pęcherzyków wewnątrzkomórkowych niż rytuksymab. Gdy badacze zakłócili konkretne szlaki pobierania, odkryli, że zablokowanie zależnej od cholesterolu formy endocytozy (przy użyciu związku o nazwie filipina) zapobiega wyłączaniu TRPML2 przez obinutuzumab i częściowo zmniejsza uszkodzenia lizosomów oraz śmierć komórek. Inne inhibitory endocytozy nie wykazywały tego ochronnego efektu. Wskazuje to na wyspecjalizowaną ścieżkę bogatą w cholesterol i sfingomielinę, która dostarcza obinutuzumab do lizosomów w sposób prowadzący do hamowania TRPML2 i następnej destabilizacji błony.
Co to oznacza dla przyszłych terapii przeciwnowotworowych
Mówiąc prosto, praca ta pokazuje, że obinutuzumab zabija chłoniaki komórek B tak skutecznie, ponieważ wpędza ich lizosomy w stan kruchości. Wprowadzając kompleksy przeciwciało–CD20 do przedziałów bogatych w sfingomielinę, lek pośrednio wyłącza ochronny kanał wapniowy TRPML2. Gdy ta zapora znika, lizosomy są bardziej podatne na pęknięcie pod wpływem stresu, wylewając żrące enzymy, które od wewnątrz rozkładają komórkę nowotworową. Zrozumienie tej osi lipid–kanał jonowy wyjaśnia nie tylko, dlaczego obinutuzumab przewyższa rytuksymab, lecz także sugeruje nowe strategie wzmacniania terapii przeciwciałowych — na przykład łączenie ich z lekami modyfikującymi sfingolipidy lub wzmacniającymi aktywność TRPML2, aby precyzyjnie regulować, jak i kiedy lizosomy komórek nowotworowych ulegają samozniszczeniu.
Cytowanie: Oh, J., Jin, N., Kwon, S. et al. Obinutuzumab induces lysosomal destabilization via sphingomyelin-dependent inhibition of TRPML2. Sci Rep 16, 7079 (2026). https://doi.org/10.1038/s41598-026-38087-5
Słowa kluczowe: obinutuzumab, nowotwór komórek B, lizosom, sfingomielina, TRPML2