Clear Sky Science · pl
Właściwości funkcjonalne pęcherzyków zewnątrzkomórkowych pochodzących z miotub szkieletowych na podstawie profili microRNA: analiza porównawcza z pęcherzykami zewnątrzkomórkowymi pochodzącymi z komórek macierzystych mezenchymalnych
Mięśniowe komunikaty w maleńkich paczkach
Nasze mięśnie robią znacznie więcej niż tylko poruszają nami — nieustannie wysyłają molekularne „wiadomości tekstowe” po całym organizmie. W tym badaniu porównano, jak drobne cząstki wydzielane przez komórki mięśniowe mają się do podobnych cząstek pochodzących z szeroko stosowanych komórek macierzystych, które rozważane są w przyszłych terapiach. Odkodowując sygnały genetyczne niesione przez te pęcherzyki, autorzy stawiają praktyczne pytanie: w jakich rodzajach chorób cząstki pochodzące z mięśni mogą być korzystniejsze niż te z komórek macierzystych?
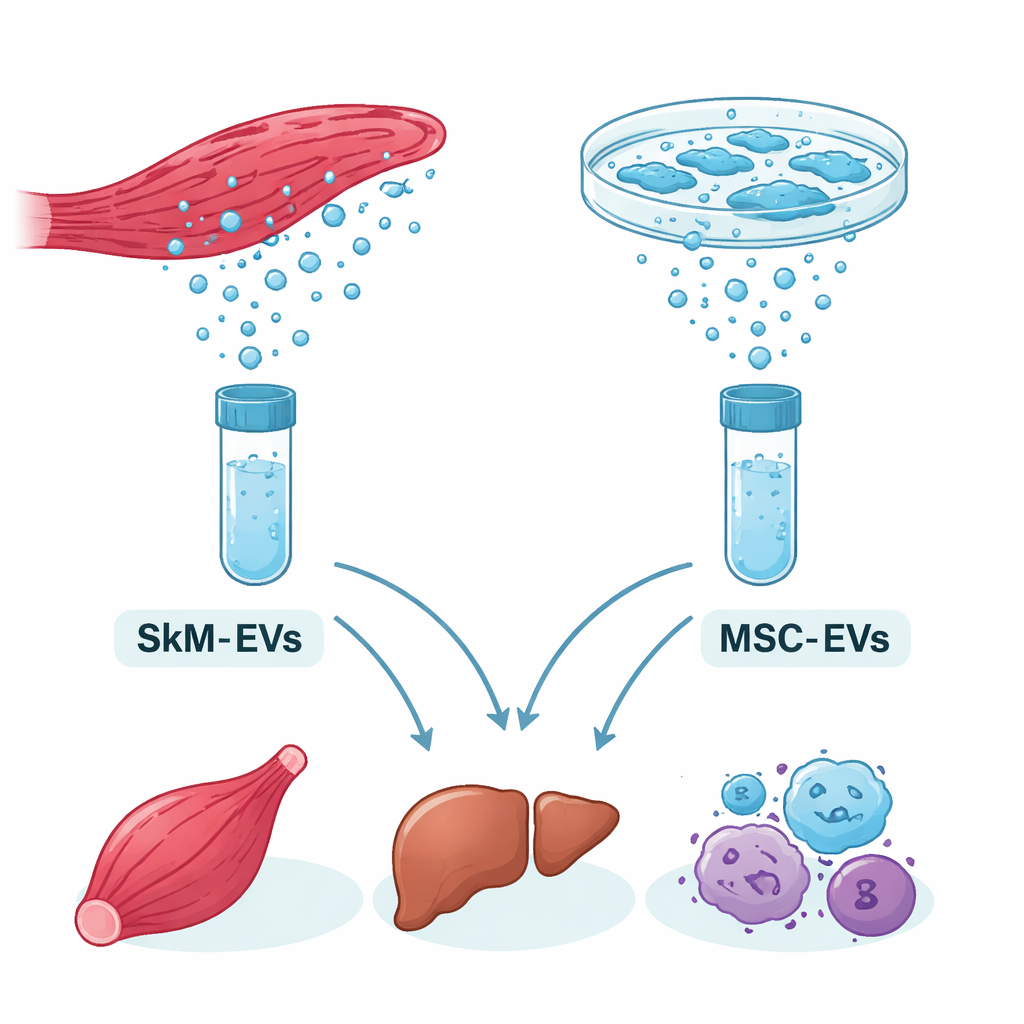
Drobni kurierzy przemierzający organizm
Wszystkie komórki uwalniają mikroskopijne pęcherzyki zwane pęcherzykami zewnątrzkomórkowymi (EV). To nanometrowe paczki otoczone tłuszczową błoną, wypełnione molekularnym ładunkiem. Jednym z kluczowych typów ładunku są microRNA — krótkie fragmenty RNA, które pomagają ściszać lub wzmacniać ekspresję genów i kształtować zachowanie komórek. Mięsień szkieletowy, tkanka napędzająca ruch, okazuje się największym organem wydzielniczym organizmu i może uwalniać duże ilości EV, szczególnie po stymulacjach nieinwazyjnych, takich jak ultradźwięki. Komórki macierzyste mezenchymalne natomiast są już powszechnie wykorzystywane w badaniach klinicznych — ich EV testuje się pod kątem naprawy tkanek i łagodzenia stanów zapalnych.
Odczytywanie kodu genetycznego ładunku
Zamiast testować EV bezpośrednio na zwierzętach czy ludziach, badacze ponownie przeanalizowali istniejące zbiory danych z sekwencjonowania, katalogujące, które microRNA występują w EV pochodzących z mysich miotub (hodowanych w laboratorium włókien mięśniowych) i z mezenchymalnych komórek macierzystych pochodzących z szpiku kostnego. EV mięśniowe zawierały kilka dominujących microRNA, takich jak miR-206-3p i miR-378a-3p, stanowiących ponad 60 procent ich ładunku, podczas gdy EV komórek macierzystych niosły bardziej wyrównaną mieszankę, w tym szeroko działającą rodzinę let-7. Ponieważ każde microRNA może wpływać na wiele genów docelowych, a wiele microRNA może koncentrować się na tych samych szlakach, zespół opracował metody obliczeniowe, by zrozumieć, jak całe profile — nie pojedyncze cząsteczki — mogą przekształcać programy komórkowe.
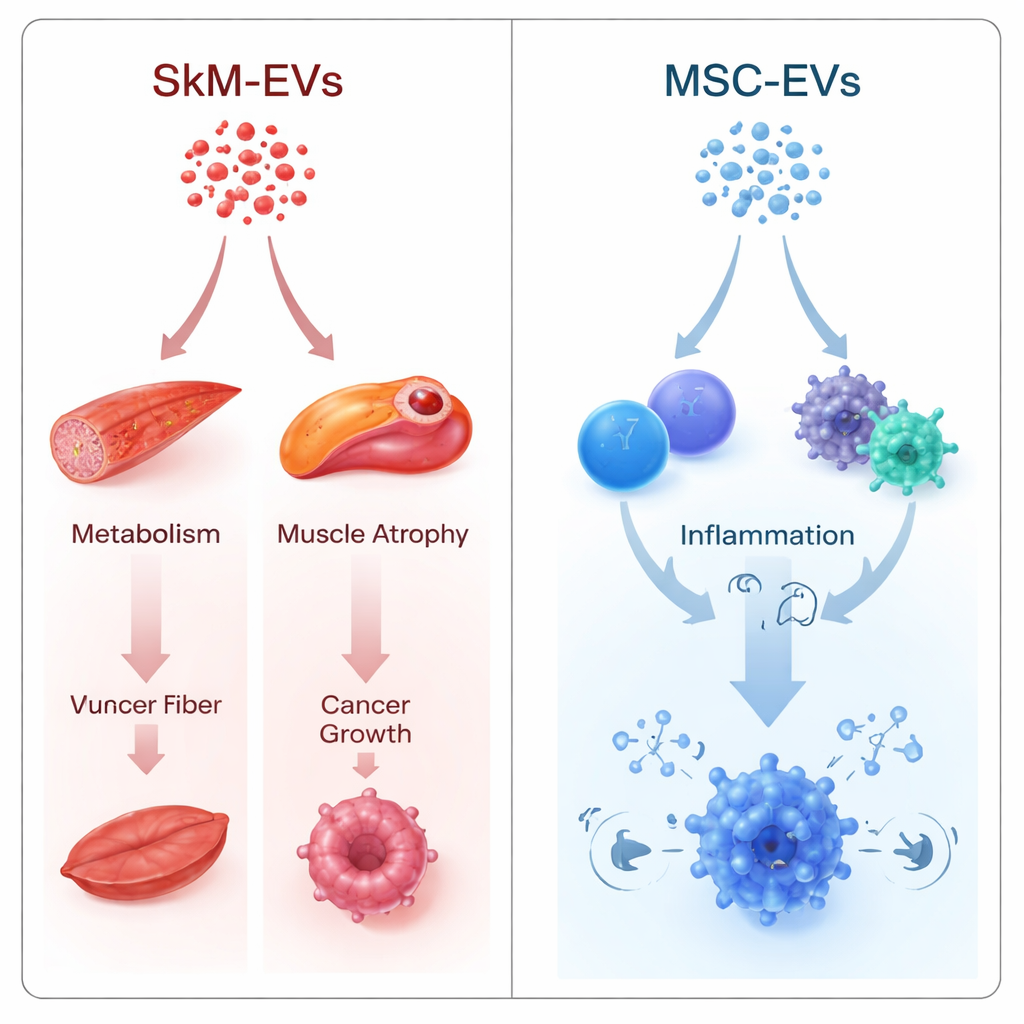
Szlaki związane z mięśniem, metabolizmem i rakiem
Autorzy zastosowali dwie uzupełniające się strategie. Jedna porównywała EV mięśniowe i macierzyste bezpośrednio, pytając, gdzie ich microRNA się różnią. Druga traktowała każdy typ EV oddzielnie, konwertując jego profil microRNA na poziom genowy „wskaźnik wpływu”, szacujący, jak silnie ładunek mógłby tłumić konkretne szlaki. Pomimo różnych metod obliczeniowych obie ścieżki wskazały w tym samym kierunku. EV pochodzące z mięśni wykazywały przewidywaną tendencję do hamowania szlaków związanych z wyniszczeniem mięśni (sygnalizacja FoxO i TGF-β), regulacją poziomu cukru i bilansu energetycznego (FoxO, mTOR, AMPK) oraz szlakami wspierającymi wzrost nowotworów (sygnalizacja ErbB i zbiorcza kategoria „microRNA w raku”). Wiele najbardziej wpływowych celów to centralne regulatory glukoneogenezy w wątrobie, kluczowe czynniki wywołujące zanik mięśni oraz podstawowe geny sprzyjające nowotworzeniu.
Pęcherzyki komórek macierzystych a układ odpornościowy
Pęcherzyki komórek macierzystych opowiadały inną historię. Ich ładunek microRNA przewidywano jako silniej oddziałujący na szlaki związane z układem odpornościowym: sygnalizację NF-κB, interakcje cytokin z receptorami, sygnalizację receptorów B i T oraz różnicowanie komórek Th17. Te szlaki są kluczowe dla tego, jak organizm wykrywa infekcje, włącza i wyłącza stan zapalny oraz kształtuje tożsamość komórek odpornościowych. To przesunięcie koresponduje z rosnącymi dowodami eksperymentalnymi, że EV komórek macierzystych mogą szeroko modulować odpowiedzi immunologiczne i są testowane w stanach, gdzie tłumienie zapalenia jest istotne, takich jak choroby autoimmunologiczne i zapalne.
Od przewidywań komputerowych do przyszłych terapii
Ogólnie rzecz biorąc, praca sugeruje, że EV pochodzące z mięśni mogą być naturalnie dopasowane do chorób związanych z wyniszczeniem mięśni, zaburzeniami metabolizmu lub niekontrolowanym wzrostem komórek, podczas gdy EV komórek macierzystych mogą być lepiej dopasowane do schorzeń napędzanych nieprawidłową odpowiedzią immunologiczną. Wyniki opierają się wyłącznie na analizie obliczeniowej istniejących danych i nie dowodzą jeszcze korzyści u pacjentów; nie uwzględniają też innych składników ładunku EV, takich jak białka czy lipidy. Mimo to, przekształcając złożone profile microRNA w „odciski palców” na poziomie szlaków, to badanie oferuje mapę drogową do dopasowywania źródeł EV do typów chorób i pomaga priorytetyzować, które kombinacje warto najpierw testować w laboratorium, a ostatecznie w klinice.
Cytowanie: Kawamoto, Y., Yamaguchi, A., Ma, X. et al. Functional properties of skeletal myotube-derived extracellular vesicles based on microRNA profiles: a comparative analysis with mesenchymal stem cell-derived extracellular vesicles. Sci Rep 16, 7436 (2026). https://doi.org/10.1038/s41598-026-38076-8
Słowa kluczowe: pęcherzyki zewnątrzkomórkowe, mięsień szkieletowy, microRNA, komórki macierzyste mezenchymalne, szlaki sygnalizacji komórkowej