Clear Sky Science · pl
Projektowanie kriżeliinów polietylenoiminowo‑metalowych dla lepszego wiązania katalazy, aktywności i długoterminowej trwałości
Dlaczego ważne jest utrzymanie enzymów na miejscu
Nadtlenek wodoru jest powszechnym produktem ubocznym w procesach od przetwórstwa żywności po zabiegi medyczne, a komórki żywe polegają na enzymie katalazie, aby rozłożyć go na nieszkodliwą wodę i tlen. W przemyśle katalaza jest jednak zwykle stosowana w postaci wolnej, rozpuszczonej, która szybko traci aktywność, nie można jej łatwo odzyskać i trzeba ją często wymieniać. W tym badaniu opisano sposób „zaparkowania” katalazy wewnątrz gąbczastego materiału, dzięki czemu pozostaje aktywna dłużej, można ją wielokrotnie używać i działa wydajniej — co razem może obniżyć koszty i uczynić procesy oparte na enzymach czystszymi i bardziej zrównoważonymi.

Budowanie inteligentnej gąbki
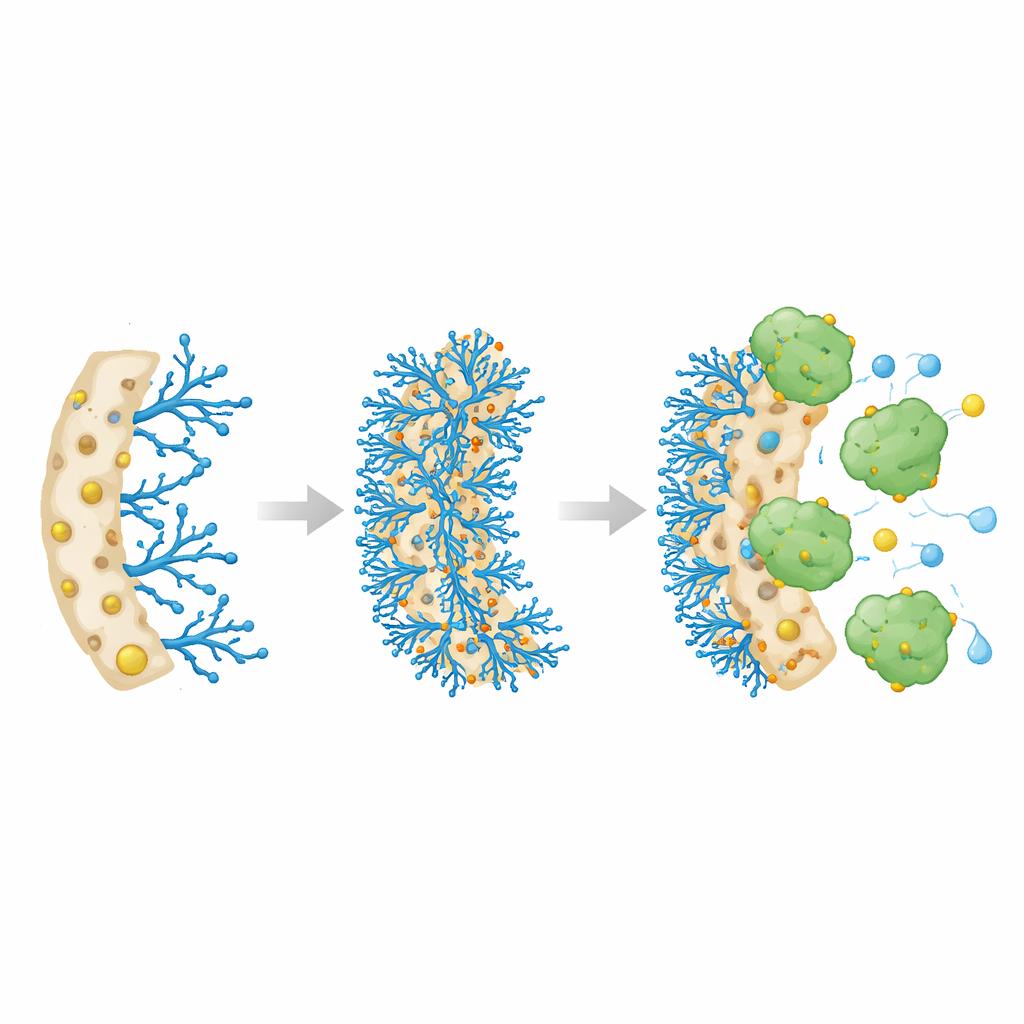
Naukowcy zaprojektowali specjalną polimerową gąbkę, zwaną kriogelem, powstającą przez zamrażanie i rozmrażanie ciekłej mieszaniny, tak że kryształy lodu wyżłobiają duże, połączone ze sobą pory. Te pory pozwalają cieczom swobodnie przepływać, podobnie jak woda przez loofah, podczas gdy stały szkielet pozostaje wytrzymały i elastyczny. Zastosowano materiał bazowy o nazwie Poly(HEMA-co-GMA), a następnie chemicznie przyłączono do niego rozgałęzioną cząsteczkę bogatą w grupy azotowe — polietylenoiminę (PEI). Na koniec do tych miejsc azotowych przyłączono jony metali — miedź, nikiel lub kobalt. Założeniem było, że jony metali będą pełnić rolę punktów dokujących, które silnie przyciągają i utrzymują cząsteczki katalazy na miejscu, nie blokując przy tym przepływu cieczy przez gąbkę.
Dostrajanie materiału dla najlepszych właściwości
Aby zrozumieć, jak każdy etap projektu wpływał na materiał, zespół zastosował kilka technik laboratoryjnych do badania jego struktury, chemii i stabilności. Pokazali, że dodanie PEI, a potem metali nie powodowało zapadnięcia się sieci porów, lecz wręcz zwiększało zdolność gąbki do zatrzymywania wody, co sprzyja utrzymaniu enzymów w komfortowych i aktywnych warunkach. Spośród trzech metali miedź stworzyła najbardziej nawodnione i dobrze zorganizowane środowisko. Obrazy mikroskopowe ujawniły, że oryginalny materiał przypominał upakowane granulki, podczas gdy wersje traktowane PEI i metalami otworzyły się do czystszej, bardziej ciągłej sieci dużych porów. Pomiary zawartości metali potwierdziły, że miedź wiązała się silniej i w większych ilościach niż nikiel czy kobalt, co sugeruje, że zapewni najbardziej efektywne miejsca dokujące dla katalazy.
Zablokowanie katalazy na miejscu
Gdy katalaza została wprowadzona do różnych gąbek zawierających metale, wszystkie trzy szybko wychwyciły enzym, ale wersja z miedzią wyróżniała się. Załadowała największą ilość katalazy — około 392 miligramów na gram suchej gąbki — i osiągnęła stan równowagi w ciągu około ośmiu godzin. Badacze następnie porównali, jak dobrze immobilizowany enzym działa w porównaniu z wolną katalazą w roztworze. Chociaż maksymalna prędkość reakcji przypadająca na gram enzymu nieco spadła, immobilizowana katalaza wykazała znacznie silniejsze pozorne powinowactwo do substratu, nadtlenku wodoru. W praktyce oznacza to, że związany enzym działał wydajniej przy niższych stężeniach substratu, prawdopodobnie dlatego, że porowata, nasycona wodą miedziana gąbka koncentrowała substrat w pobliżu enzymu i pomagała utrzymać jego aktywną konformację.
Enzym, który wytrzymuje
Jedną z największych zalet immobilizacji enzymów jest obietnica wielokrotnego użycia i długiego okresu przechowywania. W tym przypadku katalaza związana z kriogelem na bazie miedzi okazała się znacznie bardziej trwała niż jej wolny odpowiednik. Po 15 powtórnych cyklach użytkowania immobilizowany enzym zachował nadal około jednej trzeciej pierwotnej aktywności, podczas gdy wolna katalaza zwykle byłaby odrzucana po jednorazowym użyciu. W testach trwałości w warunkach chłodniczych przez 70 dni immobilizowana katalaza utrzymała ponad 60% swojej aktywności, mniej więcej dwukrotnie więcej niż enzym wolny. Gąbka umożliwiała również odłączenie i ponowne załadowanie enzymu wielokrotnie przy użyciu prostego roztworu soli, pokazując, że sam materiał może być ponownie użyty bez istotnej utraty pojemności.
Co to oznacza w praktyce
Dla osoby niezwiązanej z tematyką główny wniosek jest taki, że badacze stworzyli rodzaj wielokrotnego użytku „gąbki enzymatycznej”, która mocno, ale delikatnie utrzymuje katalazę, pomagając jej działać lepiej przy niższych poziomach chemikaliów i przetrwać znacznie dłużej w użytkowaniu i przechowywaniu. Łącząc wysoce porowaty kriogel z PEI i jonami miedzi, opracowali platformę łączącą wysokie załadowanie enzymu, poprawioną wydajność i silną stabilność długoterminową. Takie materiały mogłyby zostać zastosowane w systemach przemysłowych lub środowiskowych do rozkładu nadtlenku wodoru i związków pokrewnych w sposób bardziej niezawodny i z mniejszą ilością odpadów, oferując praktyczny krok w kierunku bardziej ekologicznych technologii napędzanych enzymami.
Cytowanie: Erol, K., Alkan, M.H. & Alacabey, İ. Engineering polyethylenimine–metal functionalized cryogels for superior catalase binding, activity, and long-term durability. Sci Rep 16, 7880 (2026). https://doi.org/10.1038/s41598-026-38040-6
Słowa kluczowe: immobilizacja enzymów, katalaza, kriogel, polimery funkcjonalizowane miedzią, biokataliza