Clear Sky Science · pl
Identyfikacja obliczeniowa i charakterystyka mechanistyczna naturalnych związków wiążących tunel wiążący prenyl PDE6D
Obrócenie ulubionego przełącznika nowotworów przeciwko nim samym
Wiele z najbardziej śmiertelnych nowotworów — od trzustki po jelito grube i płuca — polega na jednym molekularnym „włączniku” nazywanym RAS. Gdy ten przełącznik utknie w pozycji WŁ., komórki rosną niekontrolowanie. Przez dziesięciolecia twórcy leków mieli trudności z bezpośrednim wyłączeniem RAS. To badanie eksploruje inną taktykę: poszukiwanie naturalnych związków, które mogą po cichu zablokować białko pomocnicze, którego RAS potrzebuje, aby dotrzeć na miejsce działania, potencjalnie przyciemniając jego sygnał bez bezpośredniego uderzania w RAS. 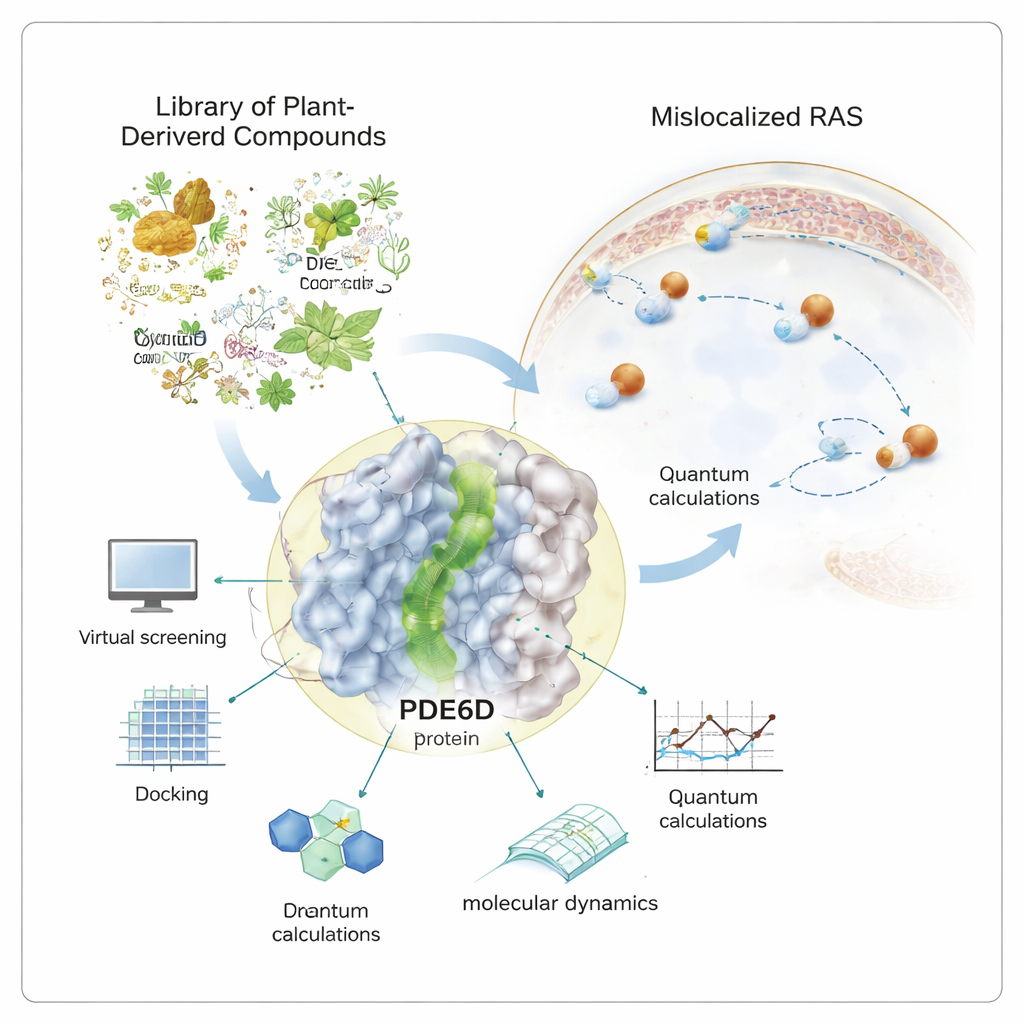
Ukryty pomocnik w komórkach nowotworowych
Białka RAS muszą znajdować się na wewnętrznej powierzchni błony komórkowej, aby przekazywać sygnały wzrostu. Aby tam dotrzeć, niosą tłusty ogon, który pozwala im zakotwiczyć się w błonie. Białko opiekuńcze zwane PDE6D działa jak taksówka, osłaniając ten ogon, gdy RAS podróżuje przez wodniste wnętrze komórki. PDE6D ma wąski, wyścielony tłuszczem tunel, który chwyta ogon RAS. Jeśli ten tunel zostanie zablokowany, RAS częściej kończy w niewłaściwym miejscu, osłabiając jego zdolność do napędzania nowotworu. Ponieważ wiele istniejących leków na RAS działa tylko dla niewielkiej podgrupy mutacji, badacze chętnie badają PDE6D jako pośredni, lecz potencjalnie bardziej uniwersalny cel.
Wykorzystywanie komputerów do przeszukiwania chemicznej biblioteki natury
Zamiast opierać się wyłącznie na związkach syntetycznych, autor zwrócił się do kurationej biblioteki ponad tysiąca dostępnych komercyjnie produktów naturalnych — cząsteczek pochodzenia roślinnego, mikrobiologicznego i innych żywych źródeł. Potężne narzędzia komputerowe zostały użyte do przesiewu tej biblioteki względem struktury 3D PDE6D. W tym wirtualnym teście każdą cząsteczkę „zadokowano” w tunelu, by ocenić, jak ciasno i korzystnie mogłaby się związać. Najlepiej oceniane kandydatury poddano następnie dokładniejszym obliczeniom na poziomie kwantowym, które badają rozmieszczenie elektronów w cząsteczce i ich skłonność do uczestniczenia w stabilizujących interakcjach w kieszeni białka.
Poddawanie obiecujących kandydatów testom wytrzymałościowym w ruchu
Białka i małe cząsteczki nie zatrzymują się w komórkach, dlatego badanie poszło dalej niż statyczne migawki. Korzystając z długich symulacji dynamiki molekularnej śledzących ruchy atomów przez pół mikrosekundy, badacz obserwował, jak każde z obiecujących naturalnych związków zachowuje się wewnątrz tunelu PDE6D w czasie. Dwa kandydaty, oznaczone MolPort-039-052-621 i MolPort-002-507-186, pozostały osadzone w tunelu z stabilnymi sieciami kontaktów, podczas gdy trzecia cząsteczka przesunęła się w stronę wyjścia tunelu i stała się słabiej związana. Dodatkowe analizy mapowały, które części struktury PDE6D ulegały uginaniu lub uspokojeniu po związaniu oraz jak kompleks eksplorował swój „krajobraz energetyczny” — zasadniczo, które kształty były najbardziej komfortowe i długotrwałe. 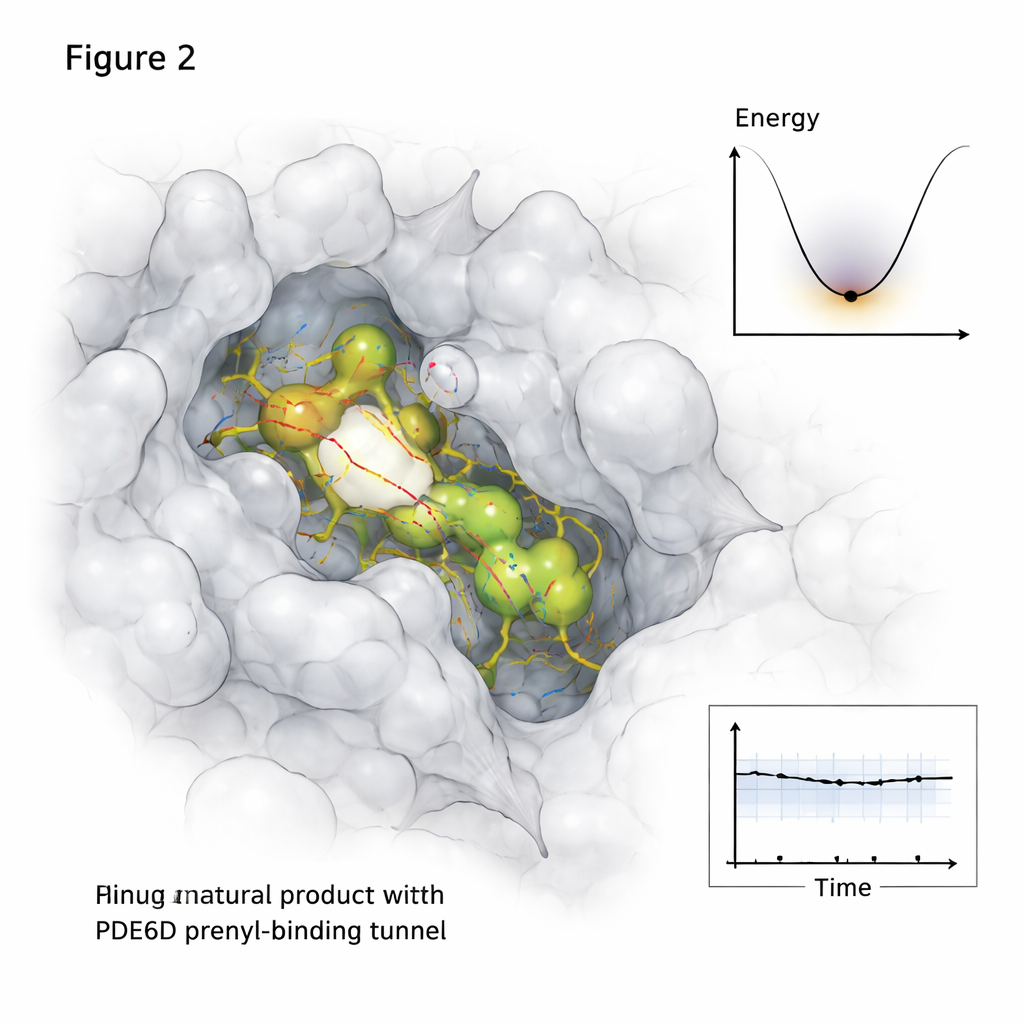
Równoważenie siły wiązania i właściwości podobnych do leków
Badanie wykorzystało również narzędzia predykcyjne online, aby ocenić, czy te naturalne związki wyglądają na realistyczne punkty wyjścia do leków. Wszystkie trzy najlepsze trafienia miały cechy chemiczne zgodne z podstawową „lekowością”, lecz każdy niósł ze sobą czerwone flagi. Niektóre przewidywano jako słabo wchłanialne lub słabo rozpuszczalne; inne wykazywały oznaki potencjalnej toksyczności, takie jak wpływ na rytm serca czy DNA. Te problemy oznaczają, że cząsteczki w obecnej postaci raczej nie są gotowymi lekami. Zamiast tego najlepiej traktować je jako szablony strukturalne, które chemicy mogą modyfikować, zachowując cechy dopasowujące do tunelu i redukując problematyczne fragmenty.
Co to oznacza dla przyszłych terapii przeciwnowotworowych
Mówiąc prosto, ta praca nie dostarcza nowego leku przeciwnowotworowego, ale wytycza obiecującą drogę. Łącząc kilka warstw obliczeń — od szybkiego dokowania po szczegółowe symulacje i obliczenia kwantowe — badanie zawęża ogromny zestaw naturalnych cząsteczek do niewielkiej grupy, które wydają się dobrze nadawać do zablokowania tunelu PDE6D. Jeśli przyszłe eksperymenty laboratoryjne potwierdzą, że związki te rzeczywiście wprowadzają RAS w błąd wewnątrz komórek i spowalniają wzrost nowotworów zależnych od RAS, mogłyby zainspirować nową klasę terapii, które celują w „logistykę” nowotworu, a nie bezpośrednio w jego głównego sprawcę.
Cytowanie: Alshahrani, M.M. Computational identification and mechanistic characterization of natural product binders targeting the PDE6D prenyl binding tunnel. Sci Rep 16, 6571 (2026). https://doi.org/10.1038/s41598-026-37939-4
Słowa kluczowe: sygnalizacja RAS, inhibitory PDE6D, produkty naturalne, komputerowe odkrywanie leków, terapia przeciwnowotworowa