Clear Sky Science · pl
Radiomika MRI oparta na habitatach dla ulepszonej diagnostyki choroby Parkinsona
Dlaczego to ma znaczenie dla pacjentów i rodzin
Choroba Parkinsona często rozwija się powoli, rozpoczynając się subtelnymi drżeniami lub sztywnością, które trudno jednoznacznie wychwycić. Obecnie lekarze wciąż w dużej mierze opierają się na objawach oraz na specjalistycznych, kosztownych badaniach obrazowych, przez co wczesne przypadki bywają łatwo przeoczone. Badanie to pokazuje, że te same rutynowe skany MRI, które wiele szpitali już wykonuje, można analizować w poszukiwaniu ukrytych wzorców, oferując szybszy, mniej inwazyjny i zaskakująco dokładny sposób wykrywania choroby Parkinsona.
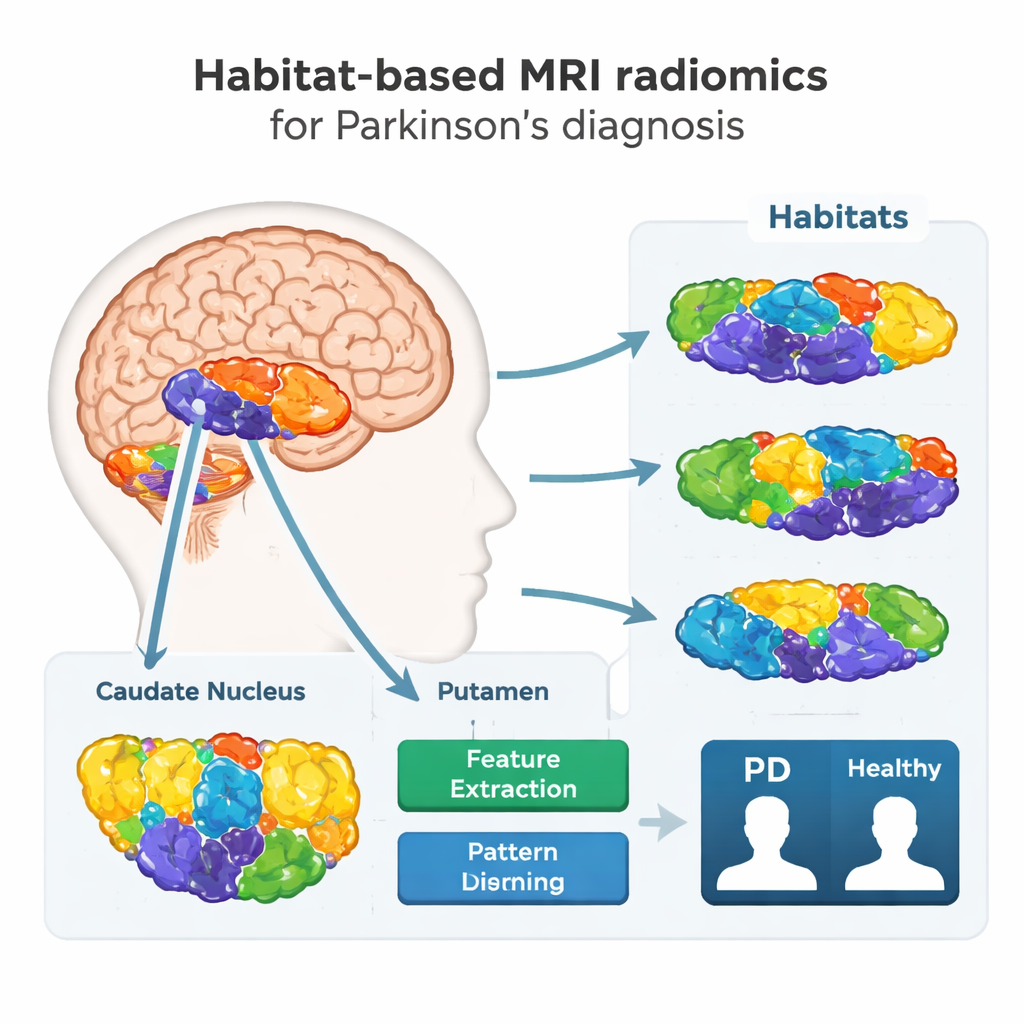
Nowe spojrzenie do wnętrza mózgu
Naukowcy skupili się na dwóch głębokich strukturach mózgu: jądrach ogoniastych i skorupie, które odgrywają kluczową rolę w kontroli ruchu i są mocno zajęte w chorobie Parkinsona. Zamiast traktować każdą strukturę jako jednorodny fragment tkanki, zadali bardziej szczegółowe pytanie: czy różne fragmenty wewnątrz tych obszarów zachowują się inaczej na MRI i czy te różnice mogą ujawniać chorobę? Aby to sprawdzić, zebrali rutynowe skany MRI od 308 osób — 173 z chorobą Parkinsona i 135 zdrowych ochotników — w dwóch szpitalach używających różnych aparatów, naśladując zróżnicowanie spotykane w praktyce klinicznej.
Od „sąsiedztw” mózgowych do cyfrowych odcisków
Wykorzystując technikę nazwaną radiomiką opartą na habitatach, zespół podzielił każdy docelowy obszar na mniejsze „sąsiedztwa” lub habitaty, bazując na subtelnych różnicach jasności i tekstury na obrazach MRI. Algorytm komputerowy grupował woksele (maleńkie trójwymiarowe piksele) o podobnych cechach obrazowych w te habitaty, a następnie wydobywał z każdego setki liczbowych cech. Te cechy tworzą rodzaj cyfrowego odcisku zdrowia tkanki, rejestrując drobne nieregularności niewidoczne gołym okiem, które mogą odzwierciedlać utratę komórek nerwowych, bliznowacenie lub gromadzenie żelaza związane z chorobą Parkinsona.
Trenowanie modelu diagnostycznego na rutynowych skanach
Mając te odciski w ręku, naukowcy wytrenowali model uczenia maszynowego, znany jako maszyna wektorów nośnych (support vector machine), aby odróżnić pacjentów z chorobą Parkinsona od zdrowych kontrol. Testowali różne sposoby dzielenia obszarów mózgu na habitaty, od jednej dużej strefy do dziesięciu mniejszych. Zarówno główny zestaw treningowy, jak i niezależny zestaw walidacyjny posłużyły do oceny wydajności. Gdy regiony podzielono na pięć habitatów, model osiągnął najlepsze wyniki: na nowych, niewidzianych wcześniej danych prawidłowo rozpoznawał chorobę Parkinsona u prawie 9 na 10 osób, a całkowita dokładność diagnostyczna w pełnym badaniu przekroczyła 94%. To przewyższało wcześniejsze podejścia, które traktowały każdy obszar mózgu jako jedną jednostkę i często osiągały plateau wokół 80–85% dokładności.
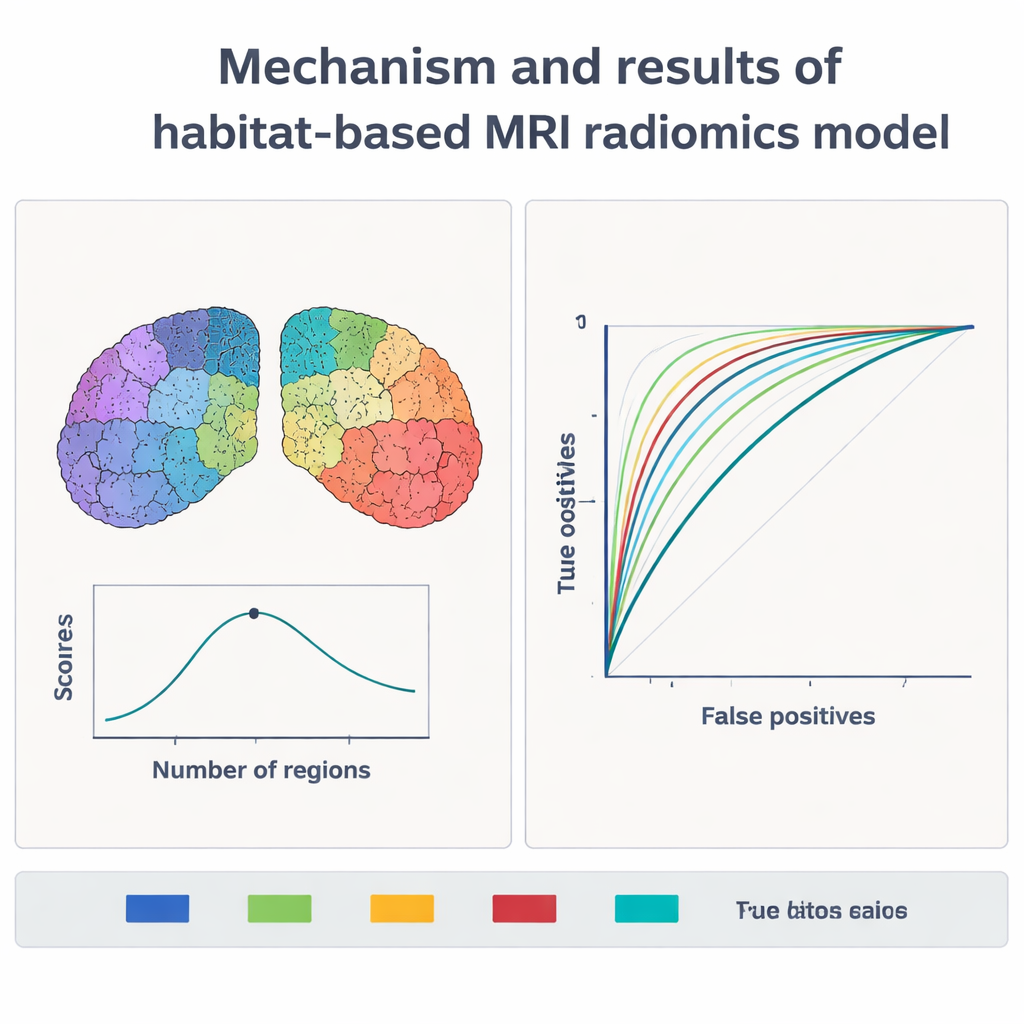
Co model naprawdę widzi
Aby uniknąć stworzenia „czarnej skrzynki”, zespół zastosował metodę wyjaśniającą zwaną SHAP, aby zidentyfikować, które cechy obrazu wpływały na decyzje modelu. Najważniejsze sygnały pochodziły z obrazów T2-zważonych MRI, powszechnej sekwencji klinicznej. U osób z chorobą Parkinsona odpowiednie habitaty wykazywały większą zmienność intensywności, bardziej ekstremalne jasne i ciemne plamy oraz skośne rozkłady intensywności w porównaniu ze zdrowymi ochotnikami. Wzorce te prawdopodobnie odzwierciedlają znane procesy chorobowe w zwojach podstawy, takie jak utrata neuronów produkujących dopaminę, miejscowe bliznowacenie i nieprawidłowe nagromadzenia żelaza. Co ważne, te same cechy powtarzały się po ponownym podziale i analizie danych w różny sposób oraz pozostawały stabilne między różnymi skanerami, co sugeruje, że metoda jest solidna, a nie przypadkowym efektem jednego aparatu.
Od narzędzia badawczego do kliniki
Analizy krzywych decyzyjnych, które bilansują korzyści wykrywania prawdziwych przypadków z kosztami fałszywych alarmów, wskazały, że model mógłby pomóc klinicystom decydować, kto naprawdę potrzebuje dalszych badań, takich jak DaTscan, a kto może bezpiecznie uniknąć dodatkowych, kosztownych procedur. Ponieważ metoda opiera się wyłącznie na standardowych skanach MRI i oprogramowaniu, może być szczególnie przydatna w miejscach, gdzie zaawansowane obrazowanie jądrowe jest niedostępne lub zbyt drogie. Autorzy twierdzą, że radiomika oparta na habitatach przekształca dobrze znane obrazy MRI w bogate mapy danych, oferując potężne, nieinwazyjne wsparcie dla wcześniejszej i dokładniejszej diagnostyki Parkinsona oraz tworząc podstawy pod przyszłe narzędzia, które mogłyby śledzić postęp choroby i wspomagać leczenie.
Cytowanie: Li, YZ., Wang, Y., Cai, C. et al. Habitat-based MRI radiomics for enhanced parkinson’s diagnosis. Sci Rep 16, 4755 (2026). https://doi.org/10.1038/s41598-026-37923-y
Słowa kluczowe: Choroba Parkinsona, MRI, radiomika, uczenie maszynowe, wczesna diagnoza