Clear Sky Science · pl
Interleukina-7 wywołuje EMT, sprzyjając wzrostowi i przerzutom nowotworu w NSCLC poprzez szlak Notch1/TGF-β
Dlaczego białko sygnalizacyjne ma znaczenie w raku płuca
Rak płuca pozostaje jednym z najgroźniejszych nowotworów na świecie, w dużej mierze dlatego, że często jest wykrywany dopiero po rozprzestrzenieniu się. W badaniu skoncentrowano się na naturalnym komunikatorze układu odpornościowego — interleukinie‑7 (IL‑7) — i postawiono ważne pytanie: w niedrobnokomórkowym raku płuca (NSCLC) czy IL‑7 pomaga organizmowi zwalczać nowotwór, czy wręcz przeciwnie — sprzyja jego wzrostowi i przemieszczaniu się? Śledząc wpływ IL‑7 na komórki raka płuca u pacjentów, w hodowlach komórkowych i u myszy, badacze odkryli drogę sygnalizacyjną, która wydaje się skłaniać guzy ku większemu wzrostowi, rozsiewowi i oporności na leczenie.
Bliższe spojrzenie na guzy płuca i przebieg choroby
Zespół rozpoczął od analizy próbek guzów od 119 pacjentów z NSCLC. Przy użyciu barwień w utrwalonych tkankach zmierzono poziomy IL‑7, jego receptora (IL‑7R) oraz dwóch kluczowych markerów opisujących, jak „zakotwiczone” lub „ruchome” są komórki nowotworowe. E‑kadheryna wiąże się z mocno połączonymi, mniej ruchliwymi komórkami, podczas gdy Vimentyna kojarzona jest z komórkami bardziej plastycznymi i inwazyjnymi. Większość guzów wykazywała wysokie poziomy IL‑7 i IL‑7R. Gdy IL‑7 i IL‑7R były obfite, E‑kadheryna miała tendencję do niskich poziomów, a Vimentyna do wysokich — wzór niekorzystny. Pacjenci, których guzy zachowały więcej E‑kadheryny, przeżywali dłużej, podczas gdy wysoki poziom IL‑7R korelował z gorszym rokowaniem, czyniąc IL‑7R silnym predyktorem wyniku.
Jak komórki nowotworowe przełączają się z przywiązania na oddalanie się
Aby wyjść poza korelacje, badacze sprawdzili bezpośredni wpływ IL‑7 na komórki raka płuca hodowane w laboratorium. Kiedy dwie linie komórkowe NSCLC wystawiono na działanie IL‑7, komórki przeszły z zwartego, „brukowanego” wyglądu w kierunku bardziej wydłużonego, swobodnie poruszającego się kształtu. Wewnątrz komórek poziomy białek zmieniały się zgodnie z tym obrazem: E‑kadheryna spadała, podczas gdy markery „ruchomych” komórek, takie jak N‑kadheryna, Vimentyna i Snail1, wzrastały. Szkielet aktynowy komórek, który umożliwia poruszanie się, stał się bardziej wyraźny i utworzył wypustki. Zablokowanie receptora IL‑7 odwracało te efekty, co wskazuje, że IL‑7 napędza ten proces zmiany kształtu — znany jako przejście nabłonkowo‑mezenchymalne (EMT) — poprzez własny receptor na komórkach raka płuca.
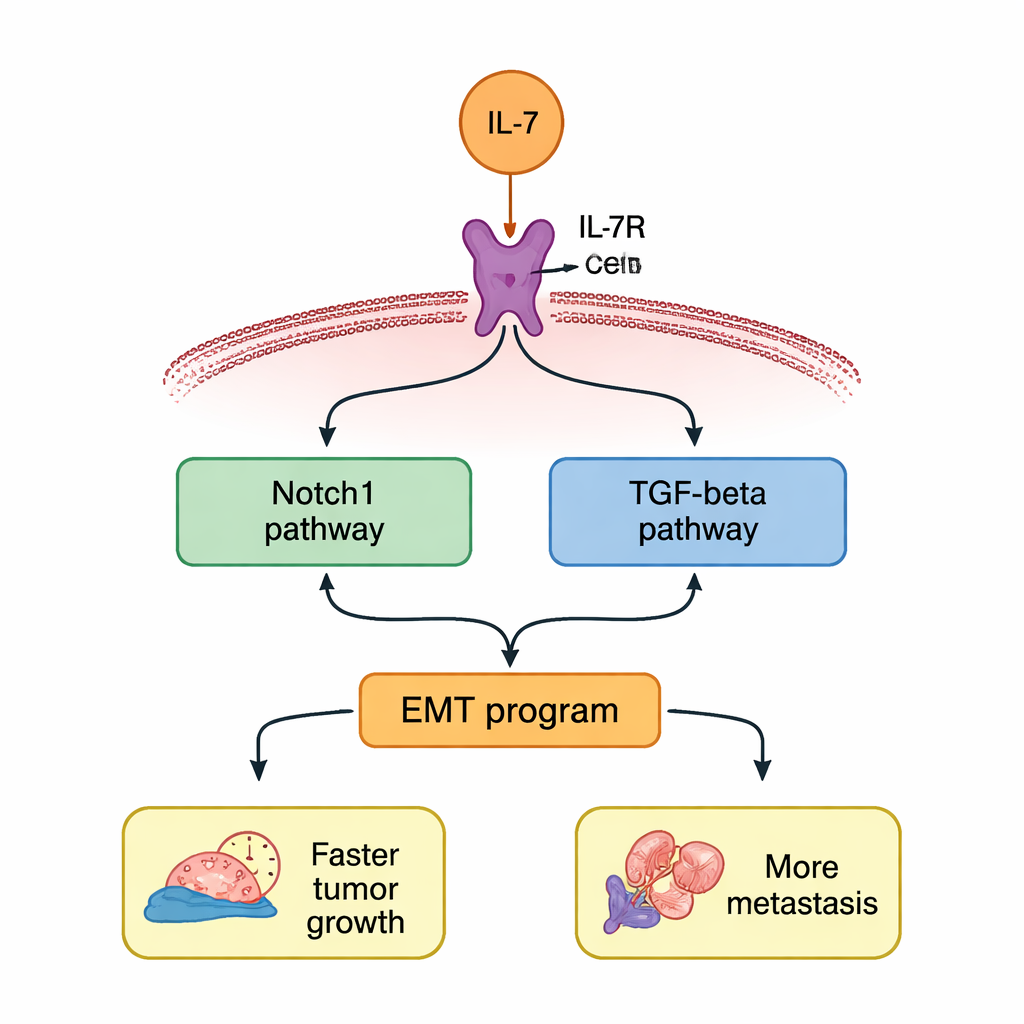
Dwa powiązane szlaki, które wzmacniają zagrożenie
W dalszej części badania zapytano, jak IL‑7 przekazuje te instrukcje wewnątrz komórki. Autorzy skupili się na dwóch dobrze znanych drogach sygnalizacyjnych, często aktywnych w agresywnych nowotworach: Notch1 i TGF‑β. Po leczeniu IL‑7 zarówno Notch1, jak i TGF‑β wzrosły na poziomie genów i białek w komórkach raka płuca. Jeśli badacze zablokowali IL‑7R, te wzrosty znikały. Gdy użyli specyficznych leków hamujących Notch1 lub TGF‑β, oba szlaki wyciszały się jednocześnie, sugerując rodzaj pętli dodatniego sprzężenia zwrotnego, w której każda z dróg pomaga utrzymać aktywność drugiej. Zablokowanie którejkolwiek z dróg częściowo wyłączało program EMT i zmniejszało napędzany przez IL‑7 wzrost, migrację i inwazję komórek.
Od szalki Petriego do żywych płuc
Aby sprawdzić, czy te wyniki z laboratorium utrzymują się w organizmach żywych, zespół przeszedł do modeli mysich. W jednym zestawie eksperymentów komórki raka płuca wszczepiono pod skórę. Myszy otrzymujące IL‑7 rozwinęły większe, cięższe guzy niż kontrolne. Tkanki guzów z tych zwierząt wykazywały niższe poziomy E‑kadheryny, wyższe Vimentyny i Snail1 oraz większą aktywność Notch1 i TGF‑β. Gdy myszy otrzymywały także inhibitory Notch1 lub TGF‑β, wzrost guza i te agresywne markery były wyraźnie zmniejszone. W drugim modelu komórki nowotworowe wstrzyknięto do krwiobiegu przez ogon. Tam myszy traktowane IL‑7 miały więcej przerzutów do płuc i cięższe płuca, podczas gdy leki blokujące szlaki znowu ograniczały ten rozprzestrzenianie się.
Co to oznacza dla przyszłej opieki nad rakiem płuca
Podsumowując, praca ta przedstawia IL‑7 nie jako prostego sprzymierzeńca układu odpornościowego, lecz jako miecz obosieczny w NSCLC. W tym kontekście IL‑7 wydaje się skłaniać komórki nowotworowe do rozluźnienia połączeń, przyjęcia bardziej ruchomej tożsamości i przemieszczania się do nowych miejsc, wszystko poprzez wzmacniające się sieci oparte na szlakach Notch1 i TGF‑β. Dla pacjentów wyniki te sugerują, że wysoki poziom IL‑7R w guzach może zwiastować gorsze rokowanie oraz że starannie zaprojektowane terapie ukierunkowane na IL‑7/IL‑7R lub ich szlaki efektorowe mogą pomóc spowolnić wzrost guza i przerzuty. Choć potrzebne są dalsze badania, by rozrysować dokładne powiązania molekularne i sprawdzić bezpieczeństwo u ludzi, badanie to uwydatnia obiecujący zestaw dźwigni do przesunięcia równowagi przeciwko rakowi płuca.
Cytowanie: Shao, Y., Cheng, H., Ni, W. et al. Interleukin-7 induces EMT to promote tumor growth and metastasis in NSCLC via Notch1/TGF-β pathway. Sci Rep 16, 7326 (2026). https://doi.org/10.1038/s41598-026-37876-2
Słowa kluczowe: nierdzeniakokomórkowy rak płuca, interleukina-7, przejście nabłonkowo-mezenchymalne, szlak Notch1, szlak sygnalizacyjny TGF-beta