Clear Sky Science · pl
Protein nukleokapsydu SARS‑CoV‑2 tworzy kompleksy z rozpuszczalnymi regulatorami dopełniacza, które mogą wiązać się z wirionem
Dlaczego ten ukryty wirusowy trik ma znaczenie
Większość z nas słyszała o białku „kolca” koronawirusa, ponieważ jest ono głównym celem szczepionek. Wewnątrz wirusa znajduje się jednak inne białko, zwane nukleokapsydowym lub białkiem N, które okazuje się czymś więcej niż tylko opakowaniem strukturalnym. Badanie to pokazuje, że białko N może przyłączać kluczowe ludzkie regulatory układu odpornościowego krążące we krwi i przenosić je na powierzchnię wirusa. Dzięki temu SARS‑CoV‑2 może częściowo wyłączać jeden z naszych najwcześniejszych mechanizmów obronnych — układ dopełniacza — co pomaga wirusowi przetrwać i może przyczyniać się do ciężkiego przebiegu COVID‑19.
Bliższe spojrzenie na wewnętrzne białko wirusa
Białko N to „opakowanie” genomu wirusa, pomagające pakować i stabilizować jego RNA. Lekarze wykryli wysokie poziomy białka N krążącego we krwi pacjentów z COVID‑19, zwłaszcza w ciężkich przypadkach, a wcześniejsze prace sugerują, że może ono pobudzać sygnały zapalne. Autorzy zastanawiali się, czy N może też zakłócać działanie dopełniacza — sieci białek krwi, które oznaczają najeźdźców do zniszczenia i mogą tworzyć otwory w błonach mikroorganizmów. Wiele wirusów wyewoluowało sprytne sposoby pożyczania lub naśladowania własnych regulatorów dopełniacza, by uniknąć ataku. Zespół postawił sobie trzy pytania: czy N wiąże się z białkiem kolca i z samym wirusem, czy wiąże ludzkie regulatorzy dopełniacza we krwi oraz czy może przenosić te regulatory na powierzchnię wirusa?
Jak N i kolce spotykają się na wirusie
Przy użyciu kilku testów wiązania białek badacze wykazali, że białko N może bezpośrednio przyłączać się do białka kolca, zarówno gdy kolce są wytworzone w laboratorium, jak i gdy występują na prawdziwych cząstkach SARS‑CoV‑2. Potwierdzili tę interakcję w różnych konfiguracjach eksperymentalnych i zmierzyli jej siłę, znajdując powinowactwo podobne do wielu przeciwciał. Przez pocięcie białka kolca na fragmenty i zidentyfikowanie, które części nadal pozostają związane z N, zmapowali prawdopodobne strefy kontaktu głównie do domeny N‑terminalnej kolca — regionu już znanego jako gorący punkt dla wiązania przeciwciał i dokowania niektórych cząsteczek gospodarza. To sugeruje, że N może tworzyć silny, biologicznie istotny most z kolcem na rzeczywistych wirionach.
Przechwytywanie własnych wyłączników organizmu
Układ dopełniacza jest ściśle kontrolowany przez rozpuszczalne „hamulce” zwane regulatorami dopełniacza, które chronią nasze własne komórki przed ostrzałem własnych mechanizmów obronnych. Zespół skupił się na czterech z nich — inhibitorze C1, białku wiążącym C4, czynniku H oraz witronektynie — ponieważ działają na różnych etapach kaskady dopełniacza. W testach opartych na surowicy i w doświadczeniach z oczyszczonymi białkami białko N wiązało wszystkie cztery regulatory, podczas gdy kolce nie wiązały ich w tych samych warunkach. Oznacza to, że N może tworzyć kompleksy N–CRP w osoczu. Co istotne, gdy N zostało wymieszane z ludzką surowicą, a następnie wystawione na cząstki wirusa, badacze wykryli te białka regulatorowe przyłączone do wirionów — ale tylko gdy obecne było N. Im więcej N użyto, tym więcej regulatorów dopełniacza pojawiało się na wirusie, co wskazuje na mechanizm rekrutacji zależny od dawki. 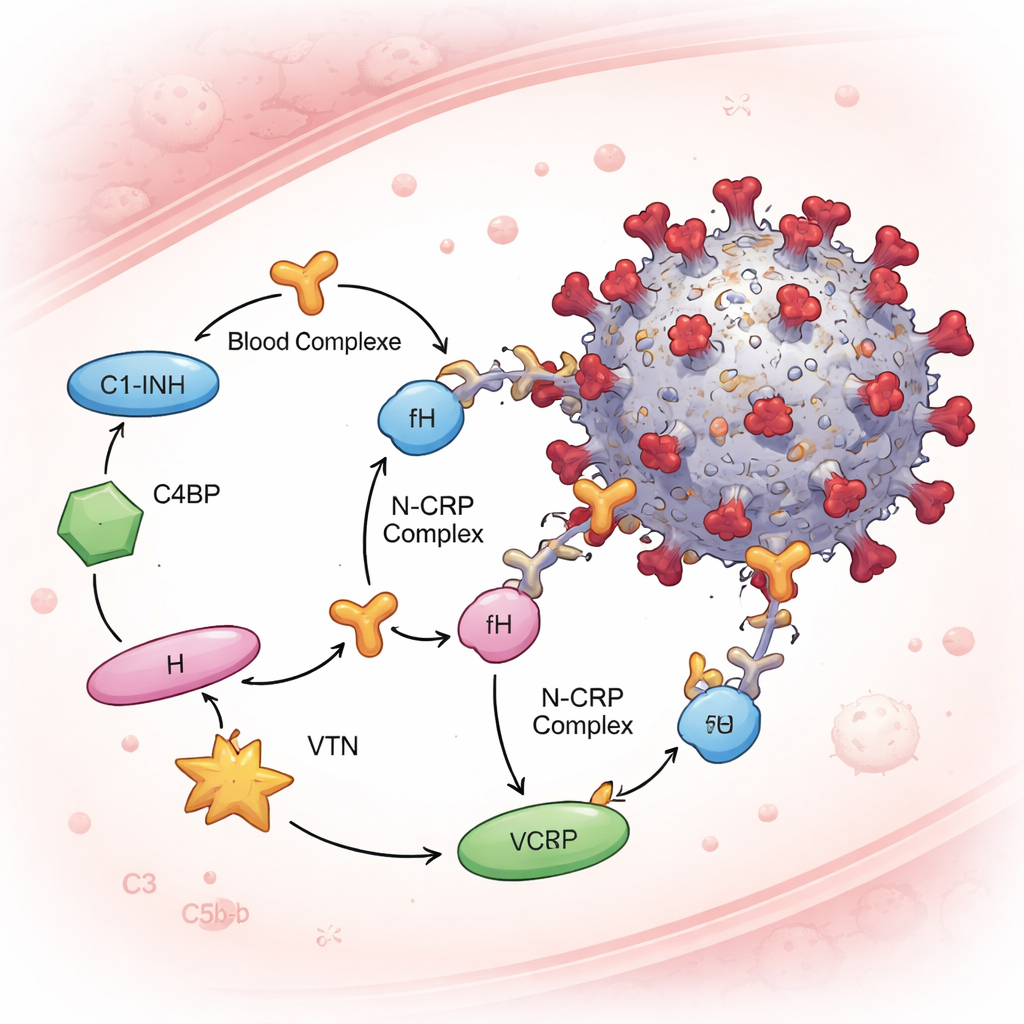
Przyciszanie końcowego etapu ataku
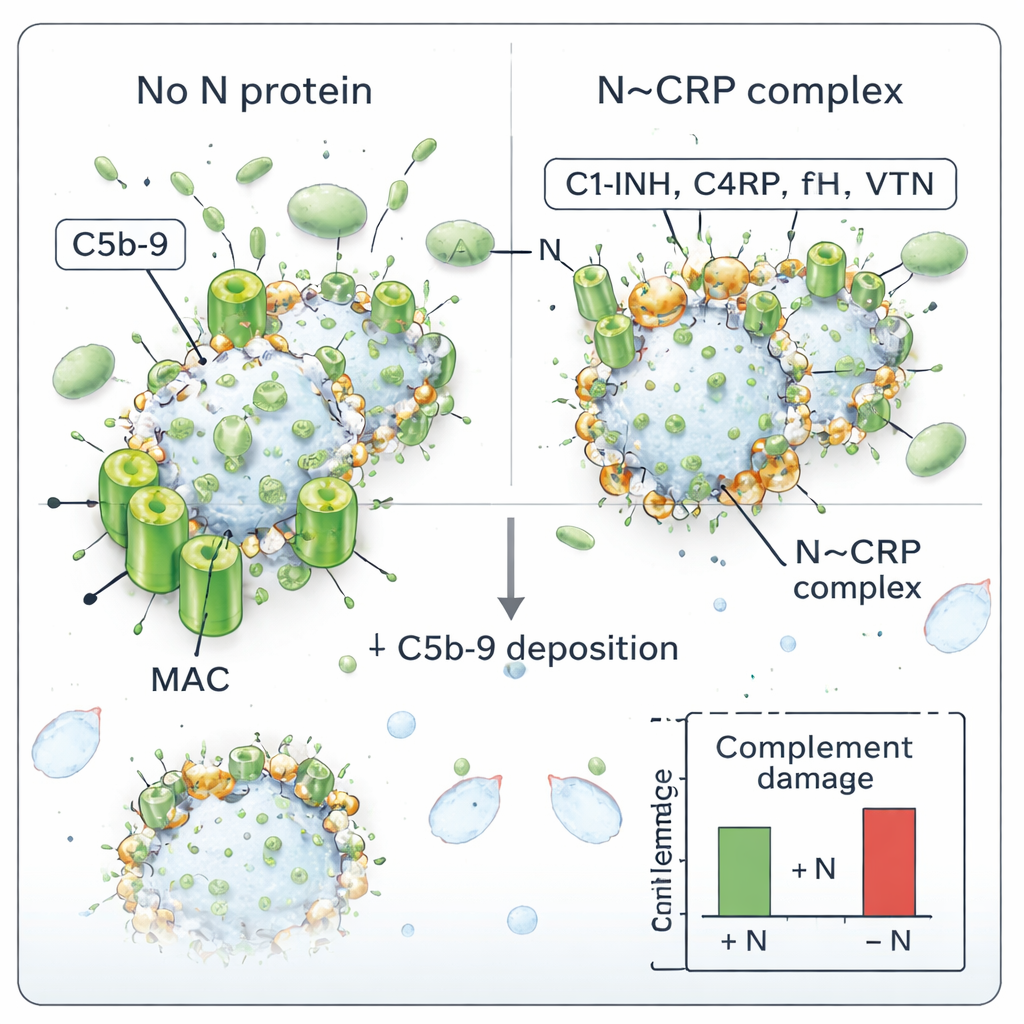
Ostateczną bronią układu dopełniacza jest kompleks atakujący błonę (MAC), pierścieniowa struktura tworząca pory w osłonkach komórek lub wirusów. Autorzy sprawdzili, czy N może zmienić tworzenie MAC na SARS‑CoV‑2. Inkubowali oczyszczony wirus z ludzką surowicą, z dodatkiem lub bez dodatku białka N, a następnie mierzyli, ile kompleksu C5b‑9 MAC kończyło na wirionach. Bez N wirus akumulował C5b‑9, co wskazuje na aktywny atak dopełniacza. Gdy obecne było N, odkładanie MAC spadało w sposób zależny od stężenia: więcej N oznaczało mniej C5b‑9 na wirusie. Zgodne jest to z koncepcją, że N, dekorując wirion regulatorami dopełniacza, chroni go przed tworzeniem się porów.
Co to oznacza dla pacjentów i przyszłych terapii
Dla osoby niebędącej specjalistą zasadniczy wniosek jest taki, że SARS‑CoV‑2 nie polega wyłącznie na słynnym białku kolca, by przechytrzyć układ odpornościowy. Jego wewnętrzne białko N może wydostawać się do krwiobiegu, chwytać własne „hamulce” dopełniacza organizmu i przenosić je z powrotem na powierzchnię wirusa. Tam mogą pomagać wirusowi ukryć się przed potężnym ramieniem odporności wrodzonej i zmniejszać bezpośrednie uszkodzenia wywołane przez dopełniacz. Może to przyczyniać się zarówno do utrzymującej się infekcji, jak i do splątanych zaburzeń dopełniacza obserwowanych w ciężkim COVID‑19. Chociaż eksperymenty wykonano w kontrolowanych warunkach laboratoryjnych, podkreślają one interakcje N–dopełniacz jako potencjalny nowy cel: terapie blokujące wiązanie N z tymi białkami regulatorowymi lub przywracające zrównoważoną aktywność dopełniacza mogłyby pewnego dnia pomóc przechylić szalę walki z powrotem na stronę układu odpornościowego.
Cytowanie: Víglaský, J., Bhide, K., Talpasova, L. et al. SARS-CoV-2 nucleocapsid protein forms complexes with soluble complement regulatory proteins that can bind to the virion. Sci Rep 16, 6599 (2026). https://doi.org/10.1038/s41598-026-37866-4
Słowa kluczowe: nukleokapsyd SARS‑CoV‑2, układ dopełniacza, ucieczka przed układem odpornościowym, regulatory dopełniacza, ciężkość COVID‑19