Clear Sky Science · pl
Strategie obliczeniowe do wydobywania informacji z znanych inhibitorów dla dalszej optymalizacji prowadzącej: studium przypadku analogów celekoksybu
Dlaczego drobne zmiany w tabletkach przeciwbólowych mają znaczenie
Nowoczesne środki przeciwbólowe nie tylko tłumią ból; precyzyjnie modyfikują chemię organizmu. Celekoksyb, popularny lek przeciwzapalny, celuje w enzym zaangażowany w ból i obrzęk, jednocześnie w dużej mierze oszczędzając siostrzany enzym chroniący żołądek. Mimo to dziesiątki bliskich chemicznych krewnych celekoksybu zachowują się w organizmie bardzo różnie. Niniejsze badanie wykorzystuje modelowanie komputerowe, by postawić pozornie proste pytanie o dalekosiężnych konsekwencjach dla bezpieczniejszych leków: ile znaczy pojedyncza, mała zmiana w cząsteczce?
Enzym, który włącza ból
Gdy tkanka zostaje uszkodzona lub zapalona, organizm uwalnia tłuszczową cząsteczkę zwaną kwasem arachidonowym. Enzym o nazwie COX-2 przekształca tę cząsteczkę w prostaglandyny, które wywołują ból, gorączkę i obrzęk. Pokrewny enzym COX-1 pomaga chronić wyściółkę żołądka i płytki krwi. Starsze środki przeciwbólowe, takie jak ibuprofen, trafiają w oba enzymy, łagodząc ból, ale często podrażniając jelita. Celekoksyb zaprojektowano tak, aby wślizgiwał się do nieco większej kieszeni występującej głównie w COX-2, blokując sygnały bólowe przy jednoczesnym zachowaniu ochronnej funkcji COX-1. Zrozumienie szczegółowego kształtu tej kieszeni i sposobu, w jaki cząsteczki leku w niej siedzą, jest kluczowe dla projektowania nowych leków o dużej skuteczności i bezpieczeństwie.
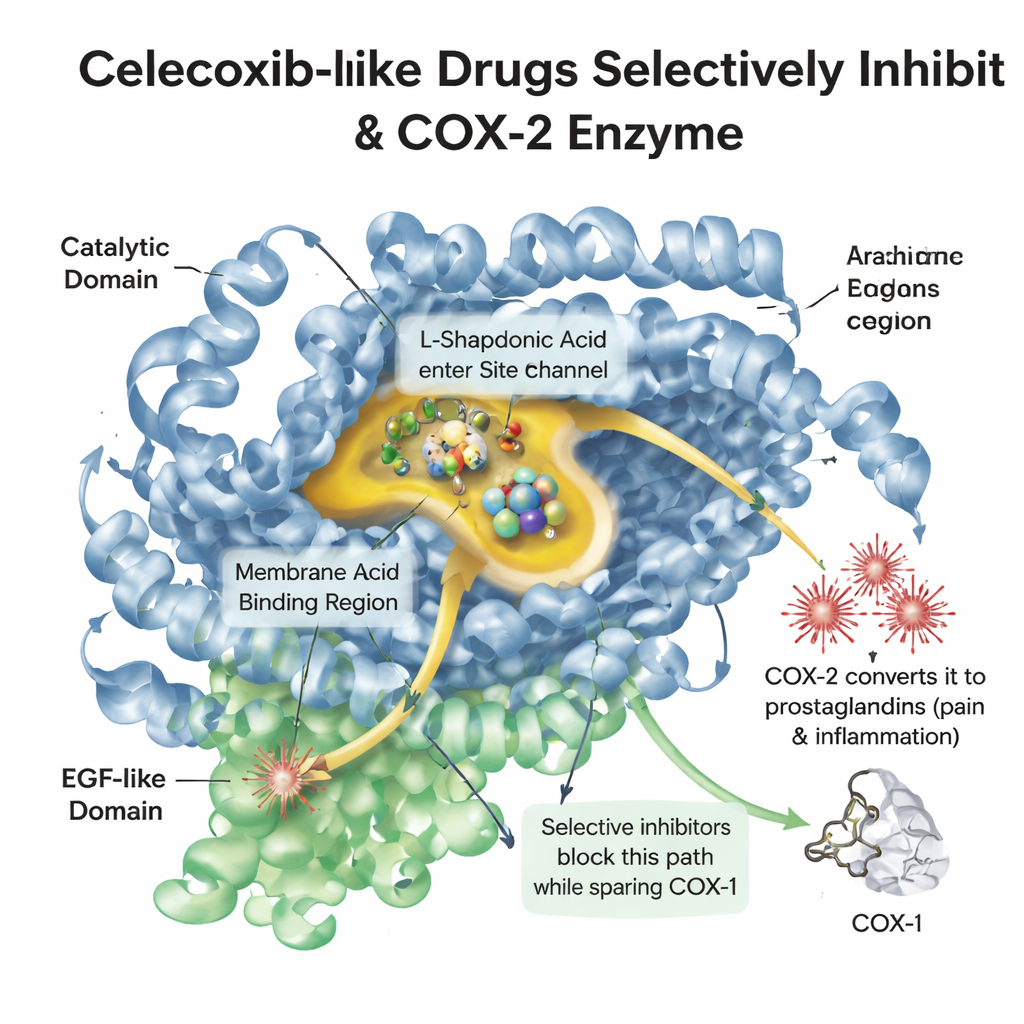
Cyfrowa biblioteka leków podobnych wyglądem
Naukowcy zgromadzili zestaw 375 cząsteczek, które wszystkie dzielą podstawowy trójpierścieniowy szkielet celekoksybu, ale różnią się drobnymi modyfikacjami, takimi jak zamiana pojedynczego atomu lub grupy bocznej. Pobrali te struktury i ich zmierzone zdolności blokowania COX-2 z publicznej bazy danych o lekach. Korzystając z oprogramowania chemicznego, wygenerowali modele 3D każdej cząsteczki, obliczyli niemal 2000 numerycznych deskryptorów ich kształtów i właściwości, a następnie zadokowali je do struktury COX-2 o wysokiej rozdzielczości. W dokowaniu komputer wielokrotnie wkłada cząsteczkę w kieszeń enzymu i ocenia, jak ciasno każda pozycja do siebie pasuje.
Co naprawdę kontroluje siłę i selektywność
Zespół skoncentrował się na trzech kluczowych rejonach celekoksybu. „Miejsce‑1” to pierścień osadzony w tłustej części kieszeni; „Miejsce‑2” to pierścień z ogonem bogatym w fluor; „Miejsce‑3” to pierścień niosący grupę sulfonamidową tworzącą silne wiązania wodorowe. Ich analiza wykazała, że Miejsce‑1 preferuje małe, niepolarne grupy zachowujące kontakty hydrofobowe; uczynienie tego rejonu bardziej hydrofilowym, na przykład przez dodanie grupy –OH lub kwasowej, zwykle osłabiało lek. W Miejscu‑2 małe, elektroujemne grupy, takie jak fluor, często zwiększały moc przez poprawę interakcji w ciasnej kieszeni, podczas gdy większe lub bardziej polarne ogony miały tendencję do osłabiania aktywności. W Miejscu‑3 azot w sulfonamidzie, zdolny do oddawania wiązania wodorowego, był kluczowy; zastąpienie go wersją niezdolną do wiązania znacząco zmniejszało wiązanie.
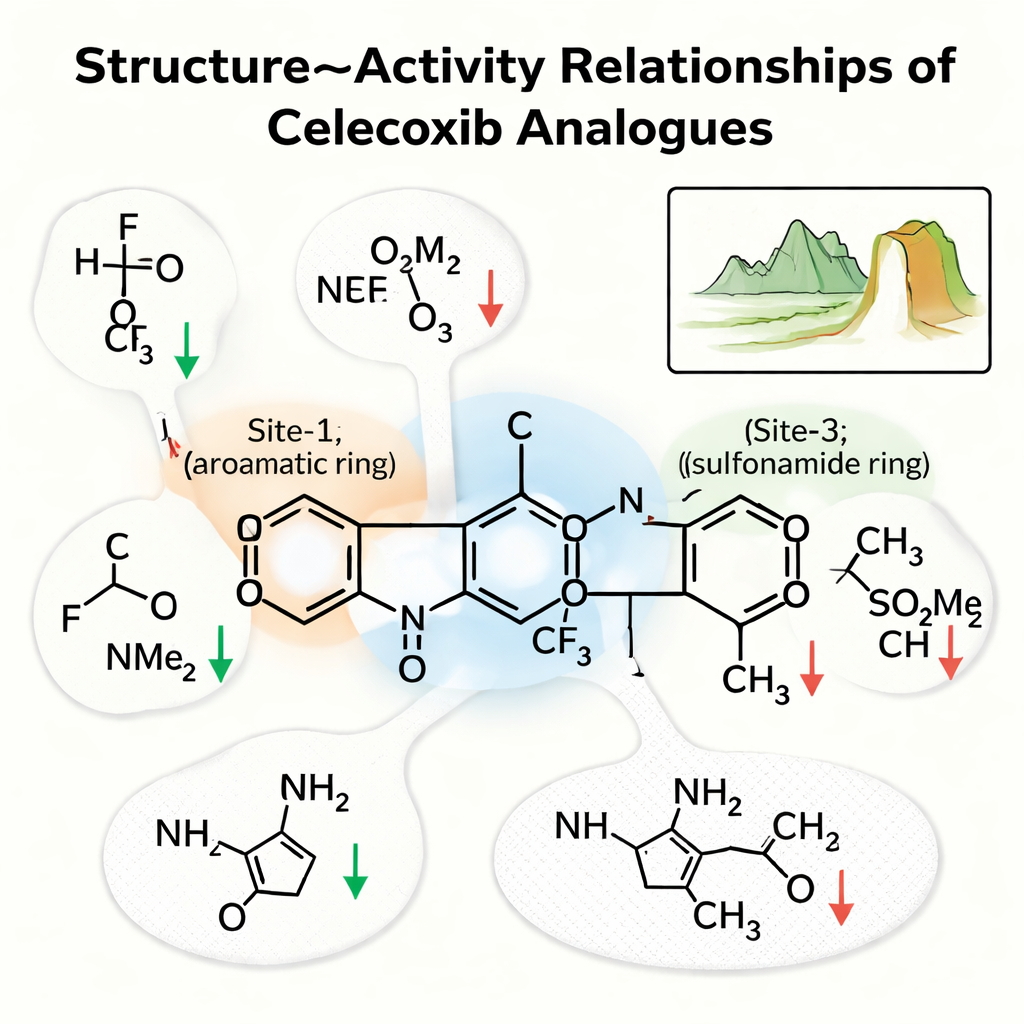
Klify w chemicznym krajobrazie
Aby wyjść poza proste trendy, autorzy zbudowali „krajobraz struktura–aktywność”, pytając, o ile zmienia się siła leku, gdy struktura zmienia się tylko nieznacznie. W tym ujęciu większość związków podobnych do celekoksybu leży na łagodnych wzgórzach: modyfikacje — na przykład przesunięcie halogenu czy dodanie małej elastycznej grupy — przesuwają moc w przewidywalny sposób. Ale kilka par tworzy ostre „klify aktywności”, gdzie drobna zmiana, taka jak zamiana grupy metylowej na trifluorometylową lub dodanie pojedynczego atomu fluoru, powoduje dramatyczny wzrost lub spadek aktywności. Badanie przeprowadziło także pełne symulacje dynamiki molekularnej — wirtualne filmy kompleksów lek‑enzym w ruchu — które potwierdziły, że najlepsze analogi siedzą stabilnie w kieszeni przez setki nanosekund.
Wytyczne dla kolejnej generacji bezpieczniejszych środków przeciwbólowych
Dla czytelnika nie‑specjalisty główny wniosek jest taki, że w projektowaniu leków małe detale mają ogromne znaczenie. Dwa związki wyglądające na prawie identyczne na papierze mogą różnić się tysiąckrotnie pod względem siły blokowania COX-2, po prostu dlatego, że dodatkowy atom poprawia dopasowanie w mikroskopijnej kieszeni lub zaburza kluczowy kontakt. Systematyczne mapowanie, które zmiany pomagają lub szkodzą w każdym z trzech kluczowych miejsc celekoksybu, oraz wskazanie niebezpiecznych „klifów”, gdzie drobne poprawki mają nieproporcjonalne skutki, daje chemikom mapę drogową. Wskazuje kierunki do nowych leków przeciwzapalnych, które zachowują przeciwbólową siłę celekoksybu przy jednoczesnym zwiększeniu bezpieczeństwa i selektywności.
Cytowanie: Grewal, S., Ghosh, B., Narayan, U. et al. Computational strategies for unraveling insights from known inhibitors for further lead optimization: A case study on Celecoxib analogues. Sci Rep 16, 6720 (2026). https://doi.org/10.1038/s41598-026-37798-z
Słowa kluczowe: inhibitory COX-2, analogi celekoksybu, leki przeciwzapalne, obliczeniowe projektowanie leków, zależności struktura‑aktywność