Clear Sky Science · pl
Wstępna ocena biodystrybucji i celowania fluorescencyjnej sondy molekularnej Cy7-SYL3C w mysich modelu raka jelita grubego z dodatnim EpCAM
Dlaczego to ma znaczenie dla wykrywania raka
Rak jelita grubego należy do najgroźniejszych nowotworów na świecie, częściowo dlatego, że wiele guzów wykrywa się późno. Obecne główne narzędzie przesiewowe, kolonoskopia, jest skuteczne, lecz inwazyjne i nieprzyjemne, dlatego wiele osób jej unika. W tym badaniu analizowano nowy rodzaj „inteligentnego znacznika” świecącego w nadziei, że pewnego dnia pomoże lekarzom wcześniej i wyraźniej dostrzegać guzy jelita, używając światła zamiast skalpela czy długiej rurki.
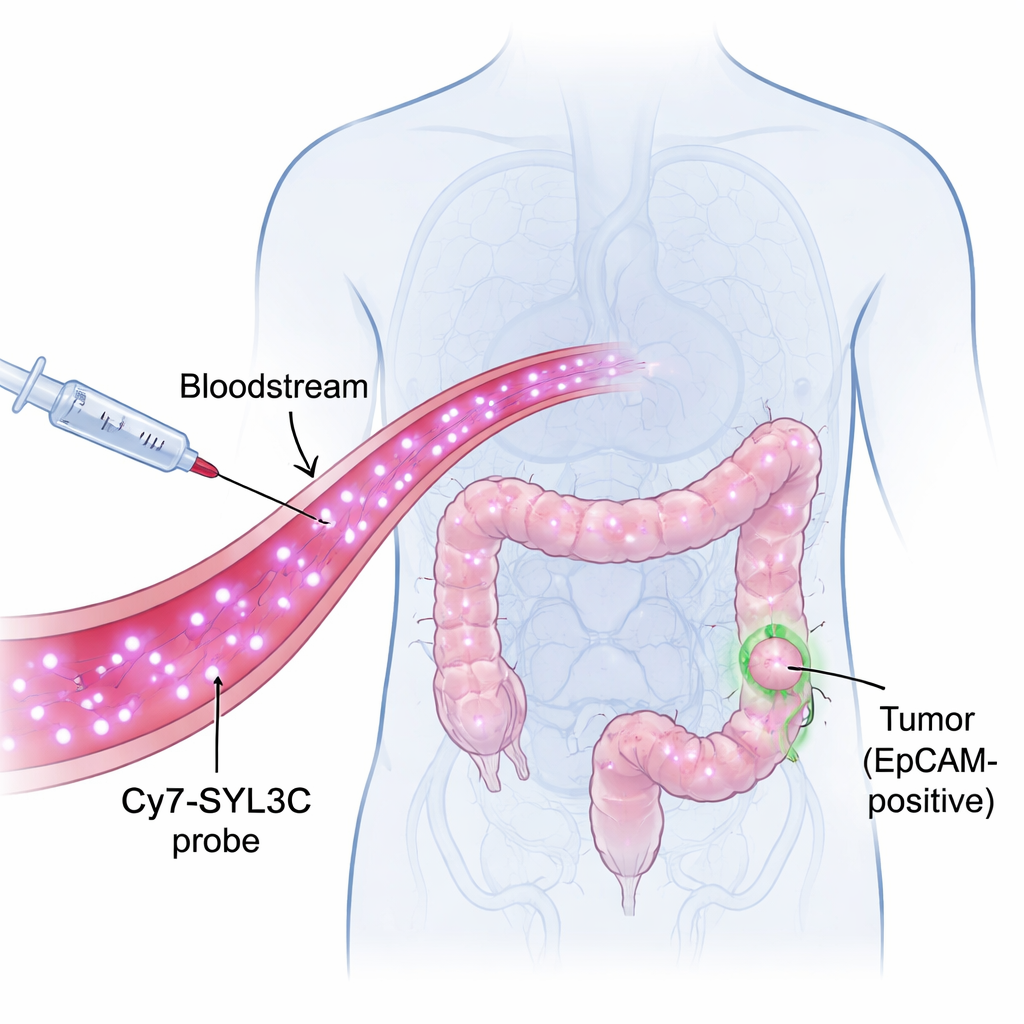
Świecący znacznik rozpoznający komórki nowotworowe
Naukowcy skupili się na cząsteczce zwanej EpCAM, która znajduje się na powierzchni wielu komórek raka jelita grubego, a rzadko na tkankach zdrowych. Zbudowali sondę nazwaną Cy7-SYL3C, łącząc barwnik w bliskiej podczerwieni (Cy7) z krótkim odcinkiem DNA zwanym aptamerem (SYL3C), który rozpoznaje EpCAM jak klucz pasujący do zamka. Światło w bliskiej podczerwieni jest niewidoczne dla oka, ale przenika na kilka milimetrów w tkanki, pozwalając kamerom rejestrować sygnały z wnętrza ciała przy wysokim kontraście. Pomysł jest prosty: wstrzyknąć Cy7-SYL3C do krwiobiegu, pozwolić mu szukać komórek bogatych w EpCAM, a następnie użyć specjalnej kamery, by te komórki rozświetliły się na ciemnym tle.
Badanie bezpieczeństwa i stabilności w laboratorium
Zanim zastosowano sondę u żywych zwierząt, zespół sprawdził jej stabilność i bezpieczeństwo. Mieszano Cy7-SYL3C z surowicą krwi myszy i bydła i stwierdzono, że większość sondy pozostawała nienaruszona przez co najmniej osiem godzin, wystarczająco długo do przeprowadzenia obrazowania podczas zabiegu. Następnie wystawiono ludzkie komórki raka jelita grubego oraz normalne komórki jelita na różne stężenia sondy. Wzrost komórek pozostał w zasadzie niezmieniony, a gdy sondę mieszano z krwinkami czerwonymi, nie powodowała ich pękania. Testy te sugerują, że Cy7-SYL3C jest zarówno chemicznie stabilna, jak i łagodna dla komórek — kluczowe wymagania dla każdego środka obrazującego, który mógłby być używany u pacjentów.
Gdzie sonda podróżuje w organizmie
Następnie naukowcy śledzili tor Cy7-SYL3C u zdrowych myszy za pomocą systemu do obrazowania małych zwierząt. Wkrótce po wstrzyknięciu najsilniejszy sygnał pojawił się w wątrobie i nerkach, narządach filtrujących i usuwających substancje z krwi. Sygnał w wątrobie osiągnął szczyt około godziny po podaniu, a potem słabł, podczas gdy nerki świeciły dłużej, co wskazuje, że główną drogą wydalania sondy jest mocz. Po dwóch dniach pozostała tylko mała część pierwotnego sygnału, a badanie mikroskopowe głównych narządów nie ujawniło widocznych uszkodzeń tkanek. Oznacza to, że sonda jest usuwana w rozsądnym tempie i nie powoduje widocznych szkód w narządach życiowych w tym krótkoterminowym badaniu.
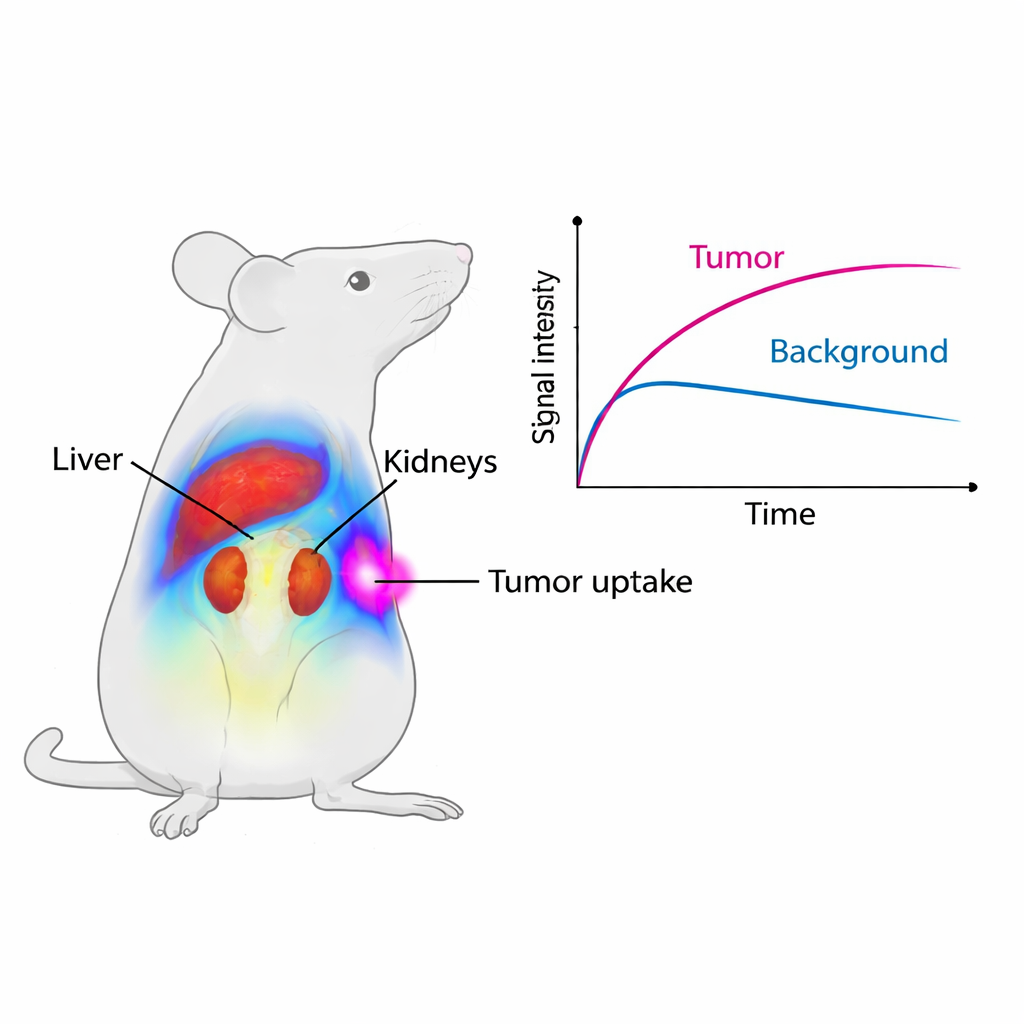
Skupienie się na guzach jelita grubego
Aby sprawdzić, czy Cy7-SYL3C rzeczywiście trafia do nowotworu, zespół użył myszy z wszczepionymi ludzkimi guzami jelita grubego produkującymi EpCAM. Już w ciągu pięciu minut od wstrzyknięcia guzy zaczęły świecić w systemie obrazowania. W pierwszych czterech godzinach średni sygnał w guzach był prawie dwukrotnie silniejszy niż u myszy, u których guzy zostały „zablokowane” nadmiarem nieznakowanego SYL3C, który tymczasowo zajmował miejsca EpCAM i uniemożliwiał przyłączenie świecącej sondy. Stosunek sygnału guza do pobliskiego mięśnia wzrósł ponad jedność i osiągnął szczyt około ósmej godziny, co oznacza, że guzy były zdecydowanie jaśniejsze od otoczenia przez użyteczne okno czasowe obrazowania. Szczegółowe badania mikroskopowe potwierdziły, że fluorescencyjna sonda nakładała się na barwienie EpCAM w komórkach nowotworowych, podczas gdy normalne narządy wykazywały niewielkie lub żadne oznaki EpCAM.
Jak to może pomóc w przyszłej chirurgii i diagnostyce
Dla osoby niebędącej specjalistą główny wniosek jest taki, że Cy7-SYL3C zachowuje się jak inteligentny barwnik, który wyszukuje komórki raka jelita grubego, a następnie w dużej mierze jest wydalany przez nerki. Wydaje się stabilny, łagodny dla komórek i potrafi sprawić, że guzy świecą szybko i przez kilka godzin, co mogłoby pomóc chirurgom w lepszym widzeniu krawędzi guza w czasie rzeczywistym lub radiologom w wykrywaniu podejrzanych obszarów podczas procedur małoinwazyjnych. Chociaż wyniki pochodzą z wstępnych eksperymentów na myszach i przed użyciem u ludzi potrzebne są dalsze badania, praca ta stanowi ważne podstawy pod nową klasę znaczników opartych na świetle, które mogą uczynić wykrywanie i chirurgię raka jelita grubego bardziej precyzyjnymi i mniej inwazyjnymi.
Cytowanie: Li, Y., Li, M., Li, P. et al. Preliminary assessment of biodistribution and targeting of the fluorescent molecular probe Cy7-SYL3C in an EpCAM-positive colorectal cancer mouse model. Sci Rep 16, 6589 (2026). https://doi.org/10.1038/s41598-026-37787-2
Słowa kluczowe: obrazowanie raka jelita grubego, fluorescencja w bliskiej podczerwieni, celowanie w EpCAM, sonda aptamerowa, prowadzenie chirurgii nowotworowej