Clear Sky Science · pl
SIRT3 hamuje postęp raka nerek poprzez regulację acetylacji IDH2
Dlaczego to badanie nad rakiem nerki ma znaczenie
Rak nerki, a zwłaszcza typ zwany rakiem nerkowokomórkowym, występuje coraz częściej i bywa trudny do leczenia po rozsianiu. To badanie zagląda pod maskę komórek nowotworowych, aby zrozumieć, jak drobne zmiany w ich „elektrowniach”, czyli mitochondriach, sprzyjają wzrostowi guza — oraz jak naturalny związek roślinny, honokiol, może ten proces spowalniać. Dla czytelników to wgląd w to, jak zrozumienie komórkowego „porządku” może otworzyć nowe opcje poza dostępnymi lekami.
Ukryty hamulec w komórkach nerek
Nasze komórki nieustannie zarządzają produkcją energii i szkodliwymi produktami ubocznymi. W zdrowych komórkach nerek białko o nazwie SIRT3 działa jak nadzorca utrzymania porządku w mitochondriach, dbając, by inne białka funkcjonowały poprawnie. Autorzy przeanalizowali duże publiczne bazy danych oraz próbki tkankowe od pacjentów i stwierdzili, że poziomy SIRT3 są konsekwentnie niższe w guzach nerkowych niż w sąsiedniej tkance prawidłowej. Guzy z najniższym SIRT3 wykazywały wzory ekspresji genów powiązane z szybszym wzrostem i większą zdolnością do przemieszczania się, co sugeruje, że utrata tego komórkowego hamulca sprawia, że komórki nowotworowe stają się bardziej agresywne.
Jak komórki nowotworowe przekręcają równowagę energetyczną
Aby sprawdzić, czy utrata SIRT3 rzeczywiście napędza złośliwe zachowanie, naukowcy zmniejszyli poziom SIRT3 w liniach komórkowych raka nerki hodowanych w laboratorium. Komórki z mniejszą ilością SIRT3 namnażały się szybciej i tworzyły znacznie więcej kolonii, co świadczy o zwiększonej przeżywalności i wzroście. Gdy takie zmodyfikowane komórki wszczepiono myszom, powstałe guzy były większe i cięższe niż guzy pochodzące od komórek kontrolnych. Razem te eksperymenty pokazują, że SIRT3 nie tylko jest nieobecne w raku nerki — gdy jest obecne, aktywnie hamuje wzrost guza.
Kluczowy enzym i problem „rdzy” w komórkach
Zespół skupił się następnie na innym białku mitochondrialnym, IDH2, które pomaga w produkcji NADPH — cząsteczki zasilającej układy detoksyfikujące reaktywne formy tlenu (ROS) — szkodliwe związki przypominające komórkową „rdzę”. Zachowanie IDH2 może być zmienione przez małą chemiczną grupę zwaną grupą acetylową. Wiadomo, że SIRT3 usuwa takie znaczniki. W komórkach raka nerki SIRT3 fizycznie wiązało się z IDH2 i usuwało grupy acetylowe na określonym miejscu (K413). Gdy SIRT3 było zmniejszone, ten acetylowy znak się kumulował, IDH2 działał mniej wydajnie, poziomy NADPH spadły, a poziom ROS wzrósł. Mitochondria straciły część potencjału błonowego, co świadczy o upośledzeniu funkcji. Używając zaprojektowanych wariantów IDH2 naśladujących stan acetylowany lub zdeacetylowany, autorzy wykazali, że forma acetylowana może zniweczyć efekt spowalniający wzrost wywoływany przez SIRT3, łącząc hamulec guza bezpośrednio z tym pojedynczym przełącznikiem chemicznym.
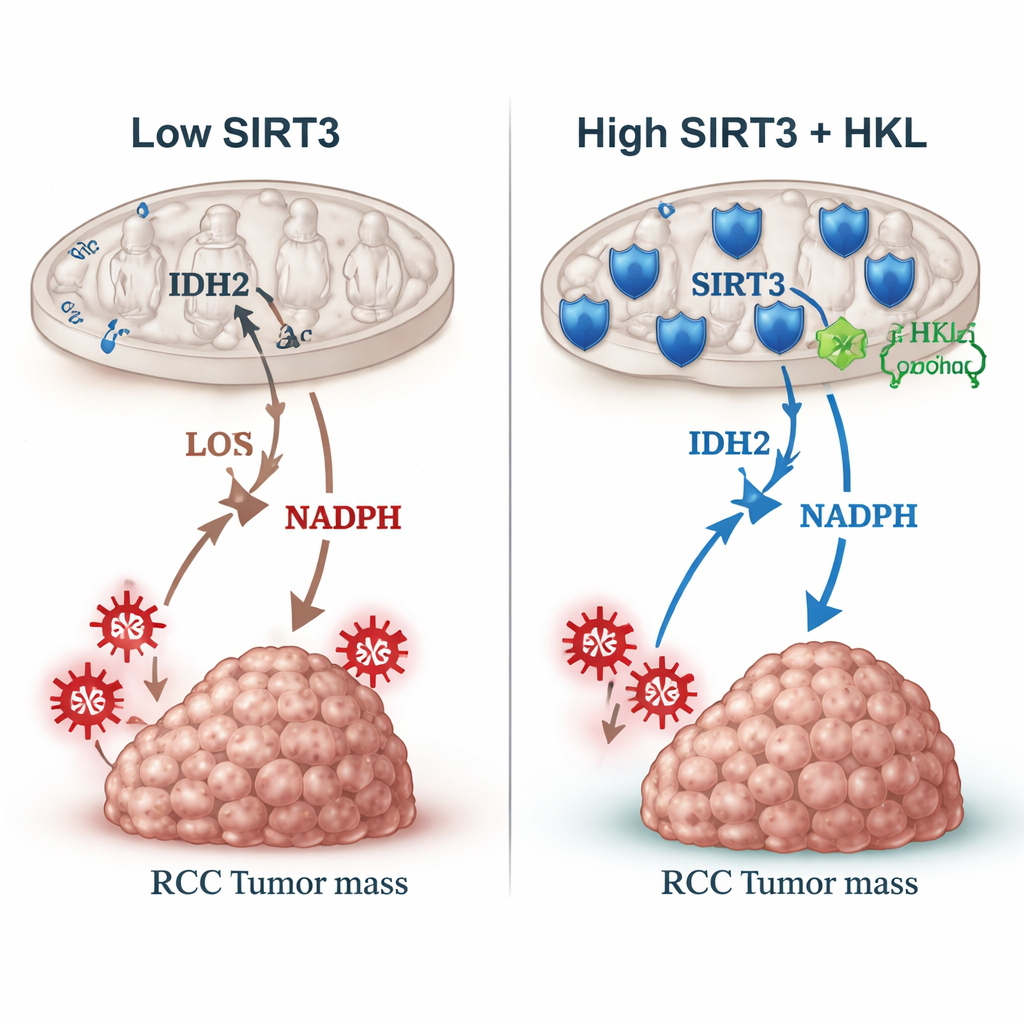
Przywracanie hamulca przy pomocy związku roślinnego
Ponieważ SIRT3 wydaje się ochronne, autorzy zapytali, czy można je zwiększyć za pomocą leku. Testowali honokiol, naturalną cząsteczkę z kory magnolii, już znaną z wpływu na różne szlaki związane z rakiem. W odpowiednio dobranej dawce, która nie zabijała komórek bezpośrednio, honokiol stopniowo zwiększał poziomy SIRT3 w komórkach raka nerki, równocześnie podnosząc związane regulatory (p-AMPK i PGC-1α). Wraz ze wzrostem SIRT3 IDH2 tracił znacznik acetylowy, poziomy ROS spadały, a komórki wolniej rosły i tworzyły mniej kolonii. Gdy honokiol zastosowano razem z sunitynibem, standardowym lekiem na raka nerki, połączenie hamowało wzrost bardziej niż sam sunitynib, częściowo poprzez złagodzenie nadmiaru ROS, które sam sunitynib może wywoływać. Podobne efekty zaobserwowano przy zastosowaniu klasycznego przeciwutleniacza, co wspiera ideę, że kontrola stresu oksydacyjnego może poprawić skuteczność istniejących terapii.
Co to może znaczyć dla przyszłych terapii
Dla osób niebędących specjalistami najważniejszy wniosek jest taki, że badanie identyfikuje SIRT3 jako naturalny hamulec guza w raku nerki, działający przez precyzyjną kontrolę IDH2 oraz równowagi między cząsteczkami ochronnymi a szkodliwymi w mitochondriach. Gdy SIRT3 jest niskie, komórki gromadzą ROS sprzyjające uszkodzeniom i zyskują przewagę wzrostu. Przywrócenie aktywności SIRT3 — potencjalnie przy użyciu honokiolu lub przyszłych, precyzyjniejszych leków — może spowolnić wzrost guza i pomóc obecnym terapiom działać lepiej. Choć sam honokiol nadal stoi przed wyzwaniami, takimi jak biodostępność i wielotorowe działanie, praca wskazuje wyraźną drogę — oś SIRT3–IDH2–redoks — na którą mogą teraz celować projektanci leków, by opracować mądrzejsze terapie oparte na metabolizmie raka nerkowokomórkowego.
Cytowanie: Li, L., Tian, Y., Chen, S. et al. SIRT3 suppresses renal cancer progression by regulating IDH2 acetylation. Sci Rep 16, 7619 (2026). https://doi.org/10.1038/s41598-026-37783-6
Słowa kluczowe: rak nerki, SIRT3, mitochondria, stres oksydacyjny, honokiol