Clear Sky Science · pl
Pobieranie DNA z odchodów w terenie za pomocą magnetycznych nanocząstek do niedestrukcyjnego monitoringu dzikiej przyrody
Dlaczego odchody zwierząt mają znaczenie dla ochrony przyrody
Dzikie zwierzęta bywają trudne do zaobserwowania, zwłaszcza w odległych lasach i tundrze. Zostawiają jednak wiarygodny ślad — odchody. W ich wnętrzu znajduje się DNA, które może ujawnić, jakie gatunki tam przechodziły, a nawet pomóc śledzić stan populacji w czasie. W niniejszym badaniu przedstawiono szybki, niedrogi sposób pozyskiwania użytecznego DNA z odchodów bezpośrednio w terenie, bez konieczności stosowania dużych maszyn laboratoryjnych. To może uczynić monitoring dzikiej przyrody dokładniejszym, tańszym i łatwiejszym do przeprowadzenia w trudno dostępnych miejscach.
Trudność w rozróżnianiu podobnych gatunków
Zespoły zajmujące się ochroną często polegają na odchodach, by monitorować zwierzęta takie jak karibu, jelenie, Łosie czy jelenie wirginijskie. Problem w tym, że wiele z tych gatunków produkuje odchody wyglądające niemal identycznie. W Kanadzie np. odchody karibu mogą być mylone z odchodami jelenia białosternego. Obecnie zwykłym rozwiązaniem jest zbieranie próbek w terenie i wysyłanie ich, często zamrożonych, do odległego laboratorium na testy DNA. Proces ten jest kosztowny, powolny i logistycznie skomplikowany, zwłaszcza gdy próbki przekraczają granice i wymagają pozwoleń. Dodatkowo DNA w odchodach szybko się degraduje, jeśli próbki się ogrzeją podczas transportu, co może zniszczyć cenne materiały.
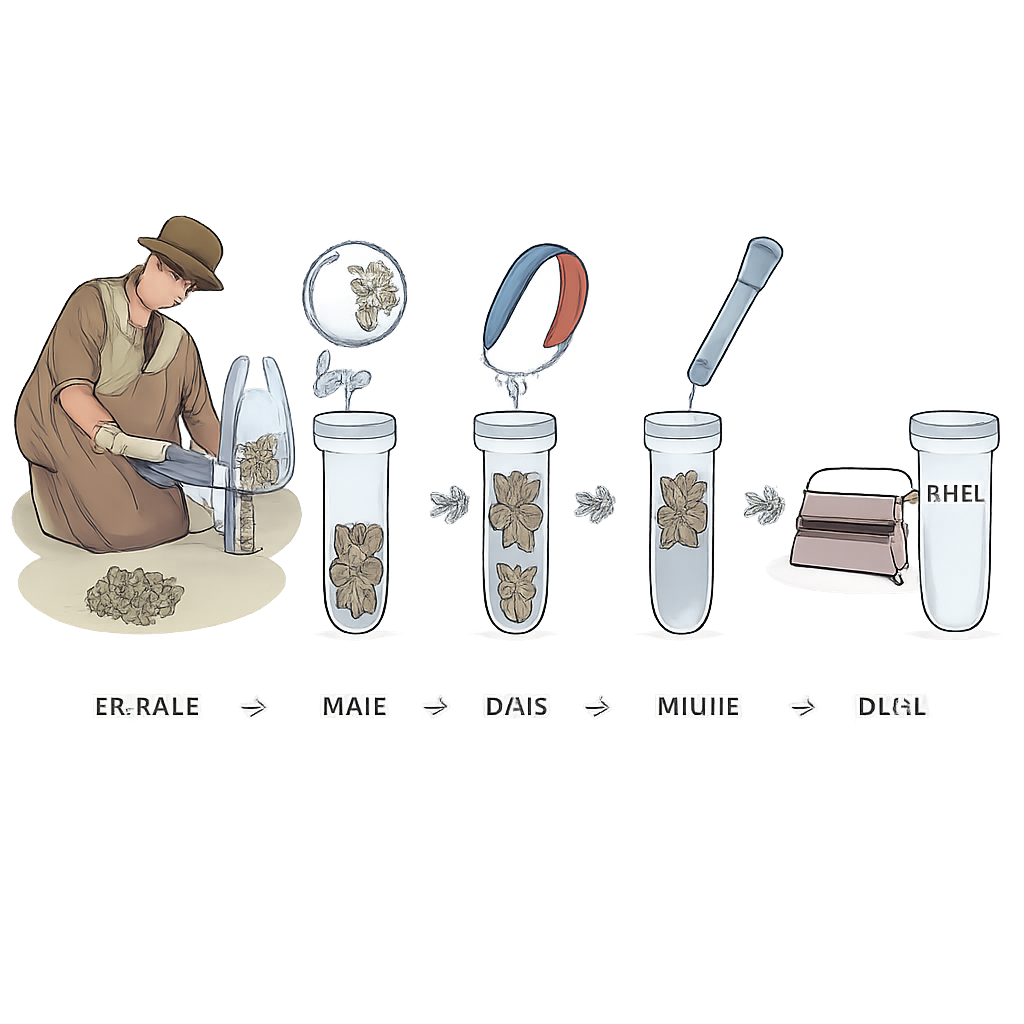
Prosty zestaw z magnetycznymi kulkami do użycia w terenie
Naukowcy opracowali nową metodę ekstrakcji opartą na małych magnetycznych kulkach powlekanych krzemionką — materiałem, który naturalnie przyciąga DNA. Pomysł polega na użyciu tylko podstawowych narzędzi: małych probówek, magnesu i kilku roztworów. W mniej niż 25 minut odchody miesza się z łagodnym roztworem litycznym, który rozbija komórki, łączy z kulkami, tak aby DNA przylegało do nich, myje, by usunąć brud i inhibitory, a następnie uwalnia do czystego płynu gotowego do testów. Co istotne, zespół celowo unikał ostrych, toksycznych chemikaliów stosowanych w komercyjnych zestawach, wybierając środki w rodzaju soli i detergentów dostępnych w gospodarstwie domowym, bezpieczniejszych zarówno dla użytkowników, jak i środowiska.
Równoważne lub lepsze niż laboratoryjny złoty standard
Aby ocenić skuteczność metody, zespół porównał ją z powszechnie stosowanym zestawem komercyjnym do ekstrakcji DNA ze stolca. Przetestowano 50 próbek odchodów karibu, dzieląc każdą pomiędzy obie metody. Średnio podejście z magnetycznymi kulkami faktycznie dało więcej DNA niż zestaw komercyjny, a to DNA działało równie dobrze w czułych testach PCR, które amplifikują materiał genetyczny. Badacze opracowali też nowe pary starterów DNA, które mogą potwierdzić, czy próbka pochodzi konkretnie od karibu, albo od dowolnego przedstawiciela rodziny jeleniowatych. Dzięki tym testom wykazali, że DNA uzyskane ich metodą było wystarczająco czyste, by amplifikować bez dodatkowego rozcieńczenia, co oznacza, że inhibitory pochodzące z odchodów nie przeszkadzały.
Działa w różnych gatunkach i opiera się na czasie
Ponieważ prace ochronne rzadko dotyczą tylko jednego zwierzęcia, zespół przetestował metodę także na odchodach jelenia białosternego, łosia i wapiti. We wszystkich przypadkach udało się wyizolować DNA mitochondrialne, a w większości próbek także DNA jądrowe — kolejny znak, że ekstrakcja jest solidna. Postawili też praktyczne pytanie: co się stanie, jeśli od razu wyekstrahowane DNA trzeba przechować? Gdy pozostawili wyekstrahowane DNA w temperaturze pokojowej lub w lodówce przez tydzień, ilość DNA pozostała stabilna, a próbki nadal nadawały się do PCR. Dla porównania, pozostawienie nietkniętych odchodów w temperaturze pokojowej przez dwa tygodnie, a następnie ekstrakcja, prowadziło do znacznych strat DNA przy obu metodach. Sugeruje to, że szybka ekstrakcja, nawet przy użyciu prostych narzędzi, jest skutecznym sposobem na „zabezpieczenie” informacji genetycznej zanim ulegnie degradacji.
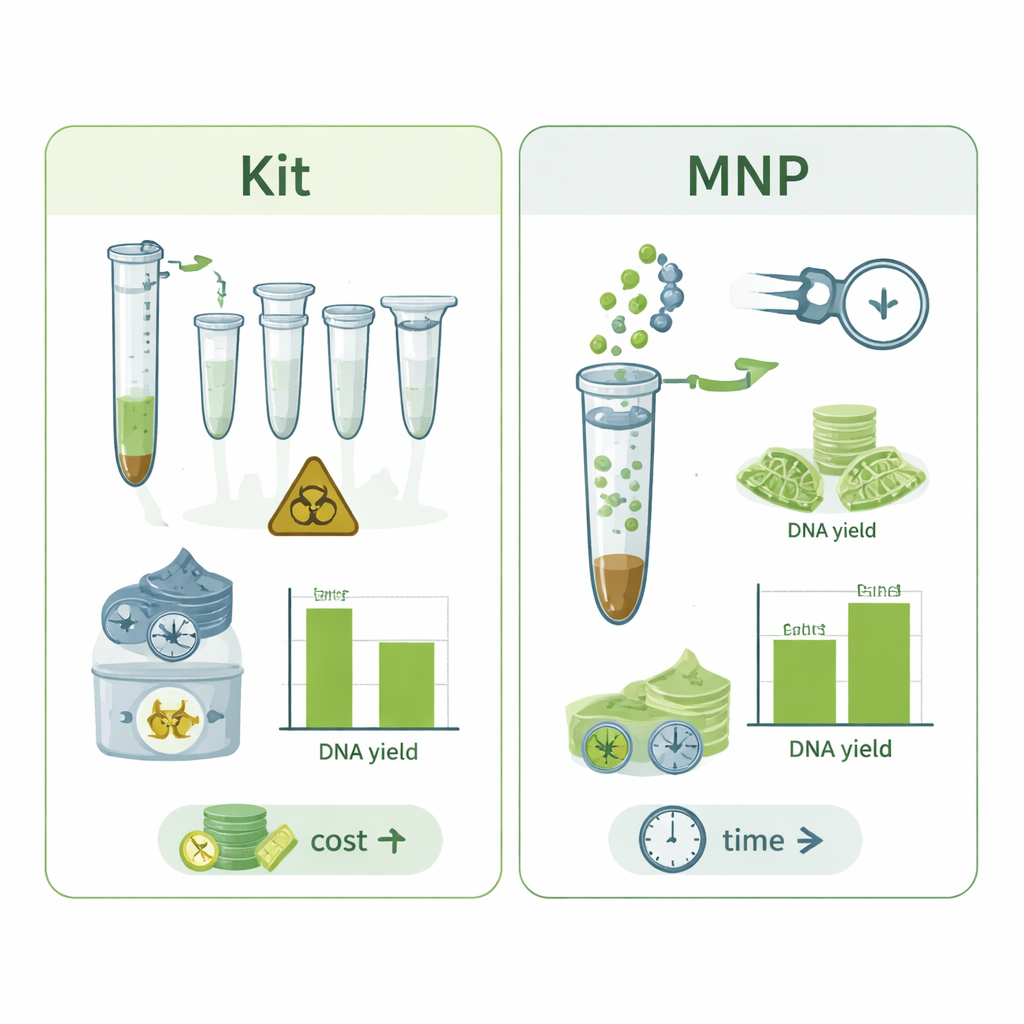
Od techniki laboratoryjnej do zestawu w plecaku
Dla osób śledzących gatunki zagrożone, takie jak karibu, praca ta wskazuje drogę ku przenośnym „laboratoriom w pudełku” mieszczącym się w plecaku. Nowa metoda kosztuje poniżej dolara za próbkę — znacznie taniej niż zestawy komercyjne — i zużywa znacznie mniej plastiku oraz nie wymaga specjalistycznych maszyn. Można ją też skalować w prostych stojakach, by obsłużyć wiele próbek jednocześnie. Mówiąc wprost, autorzy pokazują, że nie potrzeba zaawansowanego laboratorium, by zmieniać odchody zwierząt w wiarygodne wskazówki genetyczne. Z magnesem, kilkoma roztworami i niewielkim urządzeniem PCR zespoły ochrony mogą potwierdzać, które gatunki występują w danym miejscu, szybciej reagować na spadki populacji i podejmować lepsze decyzje dotyczące ochrony dzikiej przyrody i ich siedlisk.
Cytowanie: Dondi, L., Chaudhari, R., Schmitt, N. et al. Field-ready DNA extraction from scat using magnetic nanoparticles for non-invasive wildlife monitoring. Sci Rep 16, 6733 (2026). https://doi.org/10.1038/s41598-026-37759-6
Słowa kluczowe: DNA dzikich zwierząt, analiza odchodów, monitoring karibu, genetyka terenowa, ekstrakcja za pomocą magnetycznych kulek