Clear Sky Science · pl
Klasyfikacja nowotworów przy użyciu radiomiki w kontrolowanych modelach przedklinicznych
Odczytywanie nowotworu ze skanów i krwi
Nowoczesna opieka onkologiczna coraz częściej polega na komputerach przeszukujących obrazy medyczne i wyniki badań laboratoryjnych w poszukiwaniu wzorców, których ludzkie oko łatwo nie wychwyci. W tym badaniu postawiono proste, lecz istotne pytanie: jeśli chcemy określić, jaki rodzaj nowotworu ma pacjent, czy lepiej odczytywać ukrytą informację ze skanów, czy z krwi? Wykorzystując starannie kontrolowane eksperymenty na myszach, naukowcy bezpośrednio porównali te dwa podejścia, aby sprawdzić, które daje bardziej wiarygodne odpowiedzi.
Co oznacza „wirtualna biopsja”
Radiomika to szybko rozwijająca się technika, która traktuje każdy skan medyczny jako bogate źródło danych, a nie tylko obraz. Specjalne oprogramowanie przeszukuje trójwymiarowe obrazy CT guza i przekształca je w setki liczbowych cech opisujących jego kształt, jasność i drobnoziarnistą teksturę. Z założenia te wzorce mogą odzwierciedlać biologię guza podobnie jak biopsja, ale bez igieł czy operacji — tzw. „wirtualna biopsja”. Zwolennicy mają nadzieję, że radiomika pomoże klasyfikować nowotwory, oceniać ich agresywność i wskazywać terapie. Są jednak wątpliwości: wyniki bywają trudne do odtworzenia, łatwe do zaburzenia przez kwestie techniczne i trudne do interpretacji dla lekarzy.
Uczciwy pojedynek na myszach
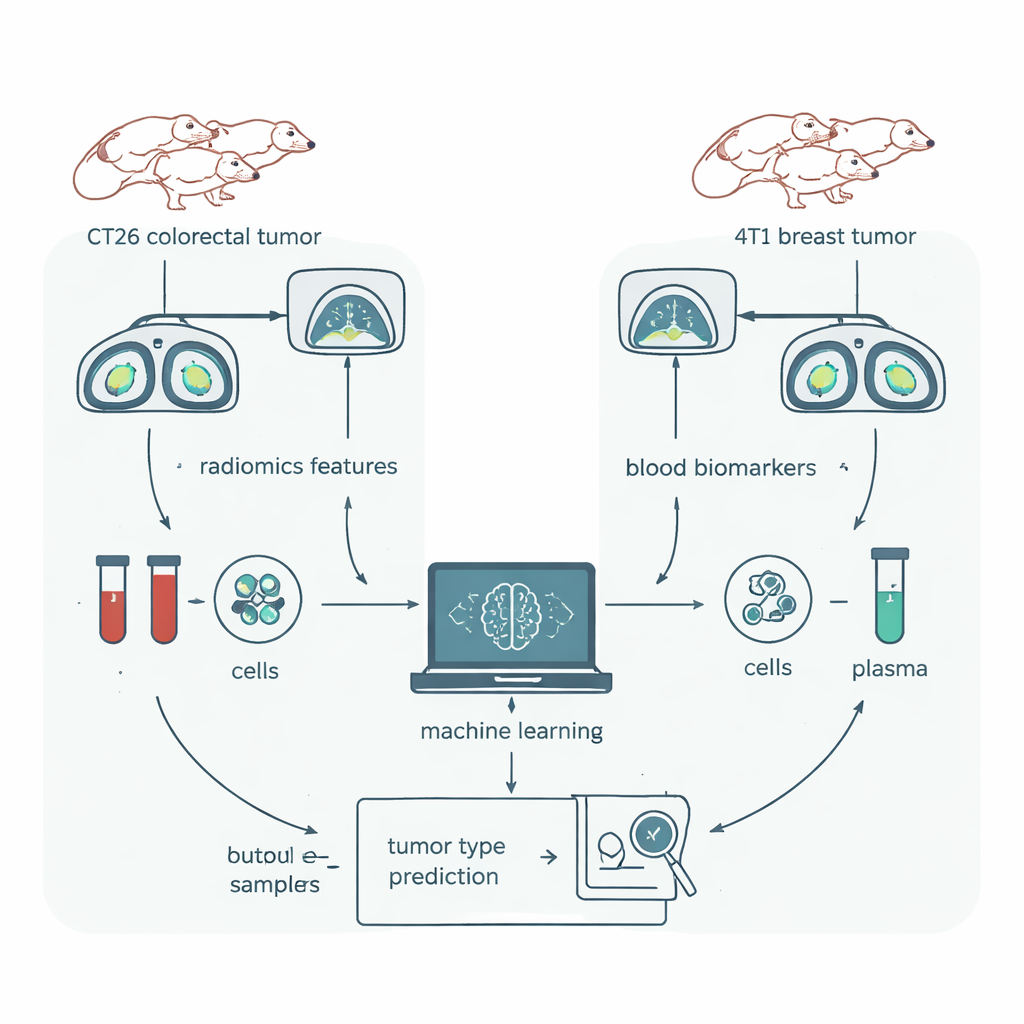
Aby poddać radiomikę rygorystycznej próbie, zespół użył modelu mysiego, w którym niemal wszystko można było kontrolować. Grupom genetycznie identycznych myszy wszczepiono jeden z dwóch typów guza: CT26, model raka jelita grubego, oraz 4T1, model raka piersi. Wszystkie zwierzęta były tej samej linii, tej samej płci i w podobnym wieku, przebywały w tych samych warunkach i były skanowane tym samym aparatem CT. Guzy starannie wyznaczono w oprogramowaniu 3D, a popularny pakiet radiomiki wydobył z każdego skanu 1 409 cech liczbowych. Równolegle badacze pobrali krew od tych samych zwierząt i zmierzyli typy komórek odpornościowych oraz dziesiątki białek — markery, które w ich wcześniejszych pracach niemal perfekcyjnie rozróżniały te modele nowotworów.
Kompresowanie tysięcy szczegółów obrazu do użytecznego sygnału
Większość surowych cech obrazu okazała się nieprzydatna: część prawie się nie zmieniała między myszami, a wiele było niemal duplikatami. Po kilku rundach filtrowania statystycznego pozostało tylko 18 nienadmiarowych cech radiomiki, opisujących głównie subtelne wzory tekstury, a nie proste rozmiary czy kształt. Zespół zastosował następnie standardową metodę uczenia maszynowego, Random Forest, aby sprawdzić, jak dobrze te oczyszczone cechy obrazu rozróżniają dwa typy guzów. Użyto też narzędzi wizualizacyjnych, by zobaczyć, czy dane naturalnie tworzą odrębne klastry dla każdego typu nowotworu bez znajomości etykiet.
Sygnały z krwi przewyższają sygnały z obrazów
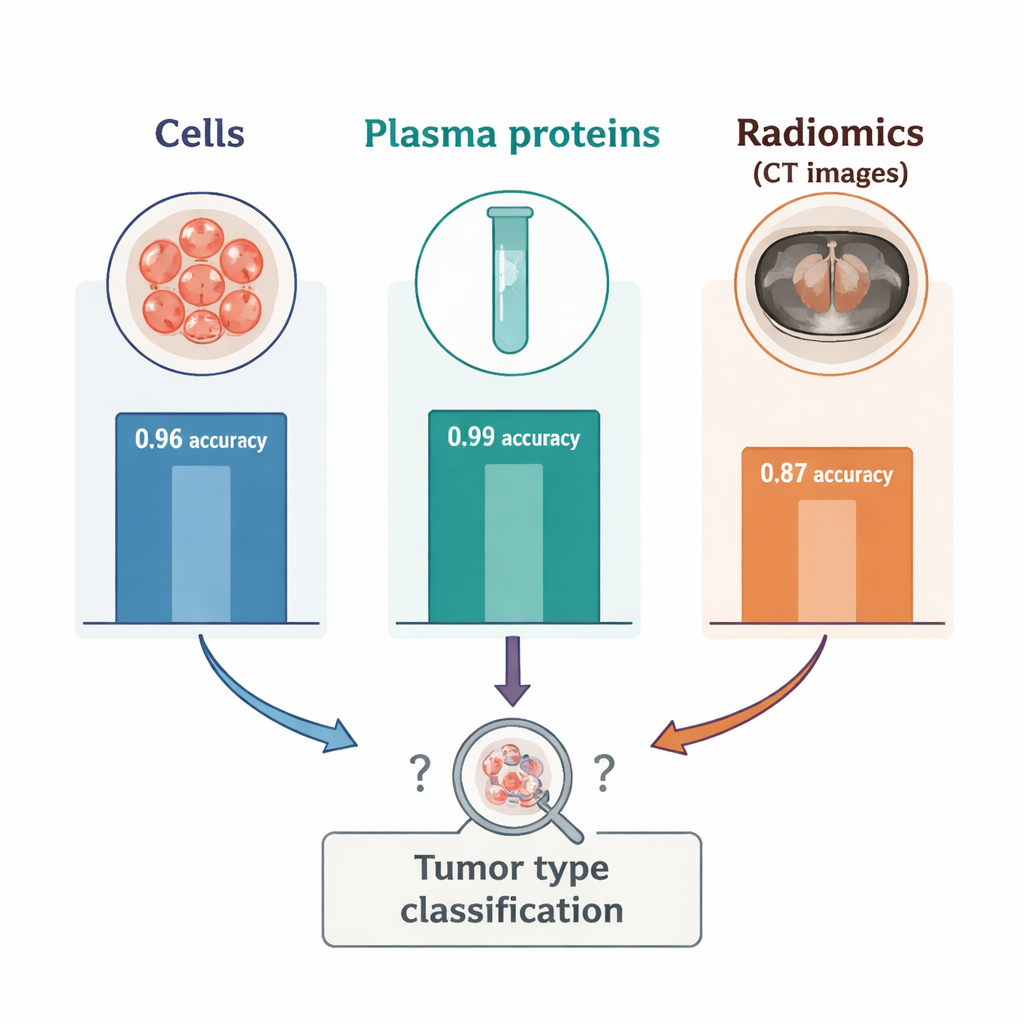
Kontrast między krwią a obrazowaniem był uderzający. Kiedy badacze zredukowali dane o komórkach krwi i białkach osocza do dwóch wymiarów, dwa typy guzów ułożyły się w wyraźnie oddzielone klastry, potwierdzając, że krew uchwyciła silne, specyficzne dla guza sygnały. W danych radiomiki pojawiły się jednak trzy wymieszane klastry, z których każdy zawierał mieszankę obu nowotworów, co sugeruje, że obrazy kształtowały inne, nieznane czynniki. W testach nadzorowanych radiomika sama w sobie klasyfikowała typ guza z dokładnością około 87% — dobrze, ale wyraźnie gorzej niż 96% dokładności uzyskane na podstawie liczby komórek odpornościowych i 99% dokładności na podstawie białek osocza. Dodanie radiomiki do markerów krwi nie poprawiło wyników; w niektórych kombinacjach nieznacznie obniżało dokładność. Dodatkowy eksperyment pokazał, że użycie tylko małego sferycznego obszaru wewnątrz guza, zamiast obrysowania całej masy, jeszcze pogarszało wydajność radiomiki, podkreślając, jak bardzo te cechy zależą od sposobu, w jaki guz jest zaznaczany na skanie.
Co to oznacza dla przyszłych testów nowotworowych
Dla laika wniosek jest jasny: chociaż zaawansowana analiza obrazów może dostarczyć pewnych użytecznych wskazówek, w tym badaniu została prześcignięta przez relatywnie proste testy krwi w zadaniu rozróżniania dwóch typów nowotworów. Nawet w ściśle kontrolowanych warunkach laboratoryjnych, przy identycznych myszach i standaryzowanym obrazowaniu, drobne różnice techniczne i złożoność przetwarzania obrazu wydawały się rozmywać sygnał radiomiki. Autorzy konkludują, że radiomika nie jest jeszcze gotowa, by służyć jako samodzielny, wysoko niezawodny klasyfikator nowotworowy. Zamiast tego wskazują na potrzebę silniejszej standaryzacji obrazowania, lepszych narzędzi do konturowania oraz jaśniejszych powiązań między wzorcami obrazu a biologią guza, zanim wirtualne biopsje będą mogły niezawodnie wspierać decyzje kliniczne obok lub zamiast dobrze ugruntowanych markerów krwi.
Cytowanie: Drover, K., Davis, D.A.S., Gosling, K. et al. Cancer classification with radiomics in controlled preclinical models. Sci Rep 16, 6647 (2026). https://doi.org/10.1038/s41598-026-37757-8
Słowa kluczowe: radiomika, markery nowotworowe, obrazowanie medyczne, uczenie maszynowe w onkologii, badania krwi na nowotwory