Clear Sky Science · pl
Wielowymiarowa strategia umożliwia skalowalną różnorodność metabolomu w mikrobiologicznych fermentacjach
Dlaczego drobne zmiany w „fabryce” mają znaczenie dla nowych leków
Wiele współczesnych leków pochodzi od naturalnych związków wytwarzanych przez bakterie i grzyby. Jednak przekształcenie obiecującego odkrycia w laboratorium w realny kandydat na lek często zawodzi na zaskakująco przyziemnym etapie: hodowli tego samego mikroorganizmu w innym naczyniu lub na większą skalę. W tym badaniu postawiono proste, lecz kluczowe pytanie — jak utrzymać stabilność i różnorodność wydzielanych związków, gdy przenosimy mikroorganizm z małych płytek testowych do większych kolb i bioreaktorów? Odpowiedź może przyspieszyć poszukiwania następnej generacji antybiotyków i innych terapii.
Trzy sposoby hodowli tego samego mikroorganizmu
Naukowcy skupili się na bakterii glebowej, Streptomyces griseochromogenes, znanej z wytwarzania wielu „metabolitów wtórnych” — małych cząsteczek o potencjale terapeutycznym. Porównali trzy powszechne systemy hodowli używane we wczesnym odkrywaniu: kolby z przegródkami (baffled shake flasks), 48-dołkowe płytki mikrodołkowe typu „flower” oraz mieszany bioreaktor z mieszadłem (stirred tank). W każdym systemie mierzyli wzrost, morfologię i strukturę komórek oraz — co kluczowe — wzorzec sygnałów chemicznych wykrywanych spektrometrią mas, używany tutaj jako odcisk palca wydzielanego metabolomu bakterii. Najpierw zastosowali klasyczną zasadę inżynierską: utrzymać taką samą dostępność tlenu we wszystkich systemach i oczekiwać podobnego zachowania. Zamiast tego wykazali, że krzywe wzrostu, formy komórek i chemiczne odciski palców różniły się wyraźnie między naczyniami.
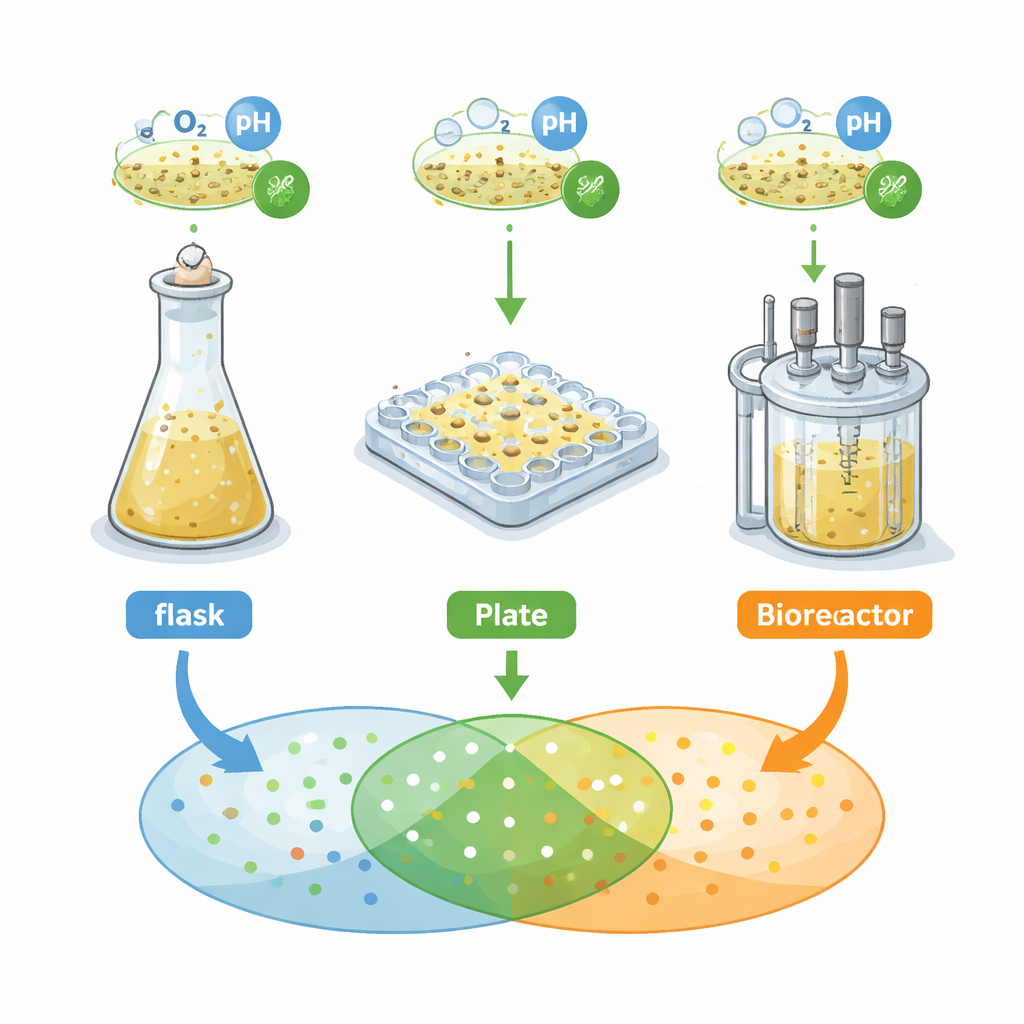
Gdy jedna zasada to za mało
Dopasowanie jedynie dostępności tlenu dało bardzo różne „ślady metaboliczne” — zbiory sygnałów masowych odpowiadających poszczególnym cząsteczkom. Tylko około 18 procent tych sygnałów było wspólnych dla wszystkich trzech systemów. Płytki mikrodołkowe generowały znacznie więcej odrębnych sygnałów niż kolby czy bioreaktor. Zespół wypróbował potem inne podejście jednoczynnikowe, zmieniając albo ilość etanolu w podłożu (mała cząsteczka, która może skłaniać bakterie do produkcji większej liczby metabolitów), albo prędkość mieszania, co wpływa na natlenienie hodowli. Te jednowymiarowe korekty nieco poprawiły nakładanie się chemicznych odcisków, ale tylko o kolejne ~18 procent. Innymi słowy, proste przepisy typu „dodaj więcej tlenu” lub „dodaj etanol” nie gwarantują, że metabolit widoczny w mikrodolekku pojawi się niezawodnie w większym fermentorze.
Jak kształt komórek kieruje różnorodnością chemiczną
Aby rozplątać, co rzeczywiście ma znaczenie, autorzy połączyli dane z 80 różnych hodowli i zastosowali metodę statystyczną poszukującą ukrytych czynników kształtujących wyniki. Analiza wyeksponowała dwa główne motywy: sam system hodowlany oraz morfologię komórek — czy bakterie rosły jako zwarte peletki, luźne maty strzępkowe czy drobno rozproszone włókna. Warunki dające podobne morfologie zwykle skutkowały podobniejszymi śladami metabolicznymi i ułatwiały „skalowanie” związków z małych systemów do mieszanych zbiorników. Poprzez celowy wybór zestawów warunków, które powodowały porównywalne kształty komórek we wszystkich trzech systemach, badacze zwiększyli nakładanie się cech chemicznych o około 50 procent w porównaniu do klasycznego dopasowania tlenu.
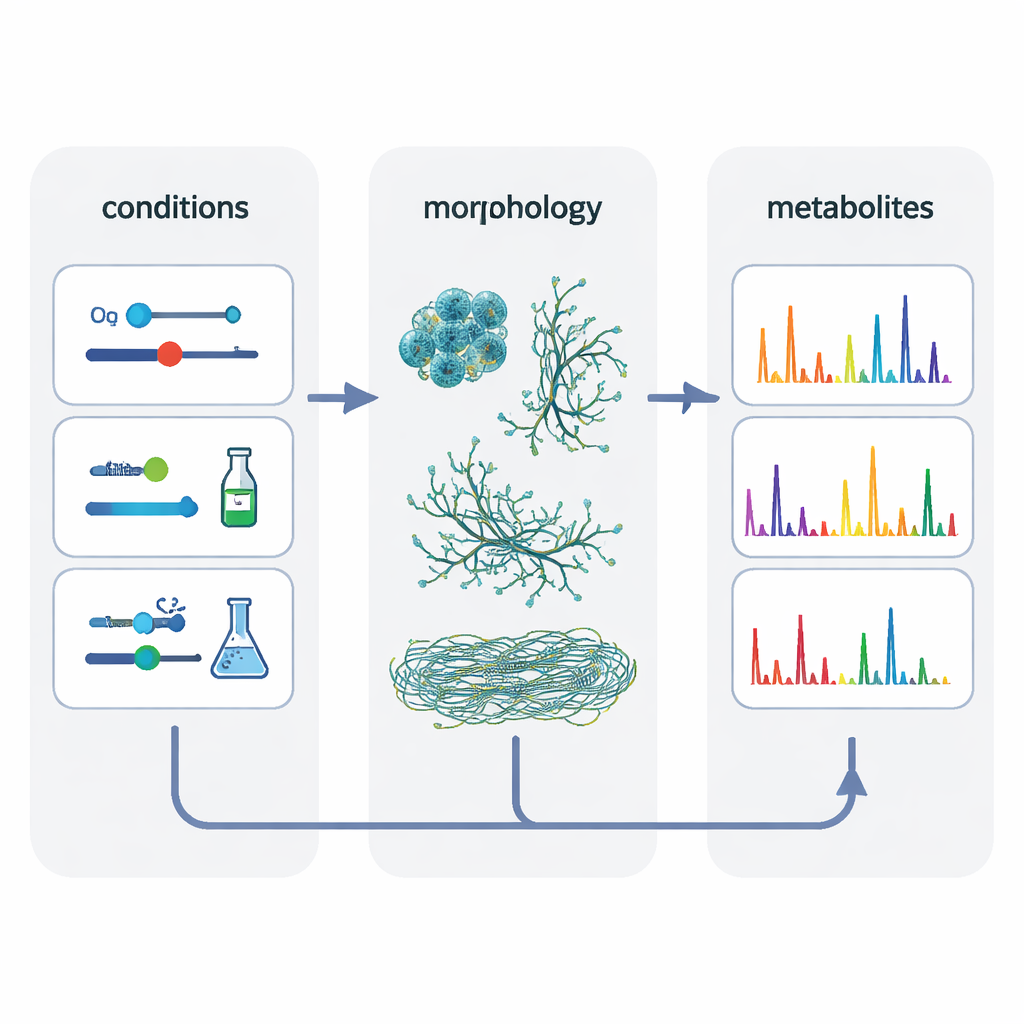
Ukryte rodziny związków i molekuły specyficzne dla systemu
Ponad prostym zliczaniem sygnałów, zespół zbudował sieci molekularne grupujące powiązane cechy masowe w rodziny strukturalnie podobnych metabolitów. Duże rodziny często zawierały przynajmniej jednego członka występującego we wszystkich systemach hodowlanych, co sugeruje pewną rdzeniową chemię odporną na zmiany skali. Jednak wiele mniejszych rodzin — oraz niektóre pojedyncze molekuły — pojawiało się tylko w jednym typie naczynia. Płytki polistyrenowe mikrodołkowe w szczególności generowały najbogatszą różnorodność związków, w tym liczne warianty żelazo‑wiązujących sideroforów zwanych desferriofaminami oraz kilka peptydów nierybosomalnych. Autorzy sugerują, że subtelne stresy w tych płytkach, takie jak wyższe poziomy reaktywnych form tlenu, mogą skłaniać bakterie do zdywersyfikowania swojej chemii, podczas gdy dobrze wymieszany bioreaktor faworyzuje mniejszy zestaw „rdzeniowych” struktur.
Co to znaczy dla poszukiwania nowych związków naturalnych
Dla zespołów zajmujących się odkrywaniem leków przekaz jest jasny: nie można polegać na jednej regule inżynierskiej ani na jednym „optymalnym” warunku, jeśli chce się osiągnąć zarówno bogatą różnorodność chemiczną, jak i wiarygodne skalowanie. Zamiast tego potrzebna jest wielowymiarowa strategia uwzględniająca typ naczynia, transfer tlenu, dodatki takie jak etanol i — co istotne — monitorowanie w czasie rzeczywistym morfologii komórek. Stosowanie płytek mikrodołkowych, które odwzorowują kluczowe cechy bioreaktorów, oraz dostrajanie warunków w celu uzyskania podobnych form wzrostu może znacząco zwiększyć prawdopodobieństwo, że obiecujące molekuły odkryte w mikrolitrach pojawią się ponownie po hodowli w litrach. To podejście pomaga przekształcać kruche wczesne odkrycia w solidne, powtarzalne kandydatury, zwiększając szanse, że nowe związki naturalne przetrwają drogę od ławy laboratoryjnej do apteczki.
Cytowanie: Lindig, A., Fataeri, M., Hubmann, G. et al. Multidimensional strategy enables scalable metabolome diversity in microbial fermentations. Sci Rep 16, 4084 (2026). https://doi.org/10.1038/s41598-026-37748-9
Słowa kluczowe: odkrywanie związków naturalnych, fermentacja Streptomyces, metabolomika, skalowanie w bioreaktorze, metabolity wtórne