Clear Sky Science · pl
Synergistyczne ukierunkowanie osi ARID2–MYC przez pomalidomid i panobinostat pokonuje wrodzoną oporność na IMiD w szpiczaku mnogim
Dlaczego to badanie ma znaczenie dla pacjentów
Szpiczak mnogi to nowotwór komórek produkujących przeciwciała w szpiku kostnym, który stał się bardziej uleczalny, ale rzadko jest w pełni wyleczalny. Wiele osób ostatecznie przestaje reagować na standardowe leki, co ogranicza opcje terapeutyczne. W tym badaniu analizowano, dlaczego połączenie dwóch istniejących klas leków — tzw. IMiD, takich jak pomalidomid, oraz inhibitorów deacetylaz histonowych (HDAC) takich jak panobinostat — może współdziałać w zabijaniu komórek szpiczaka, nawet gdy nowotwór jest już oporny na same IMiD. Zrozumienie tej współpracy na poziomie molekularnym może pomóc w opracowaniu lepszych terapii skojarzonych i umożliwić większej liczbie pacjentów skorzystanie z dostępnych już leków.
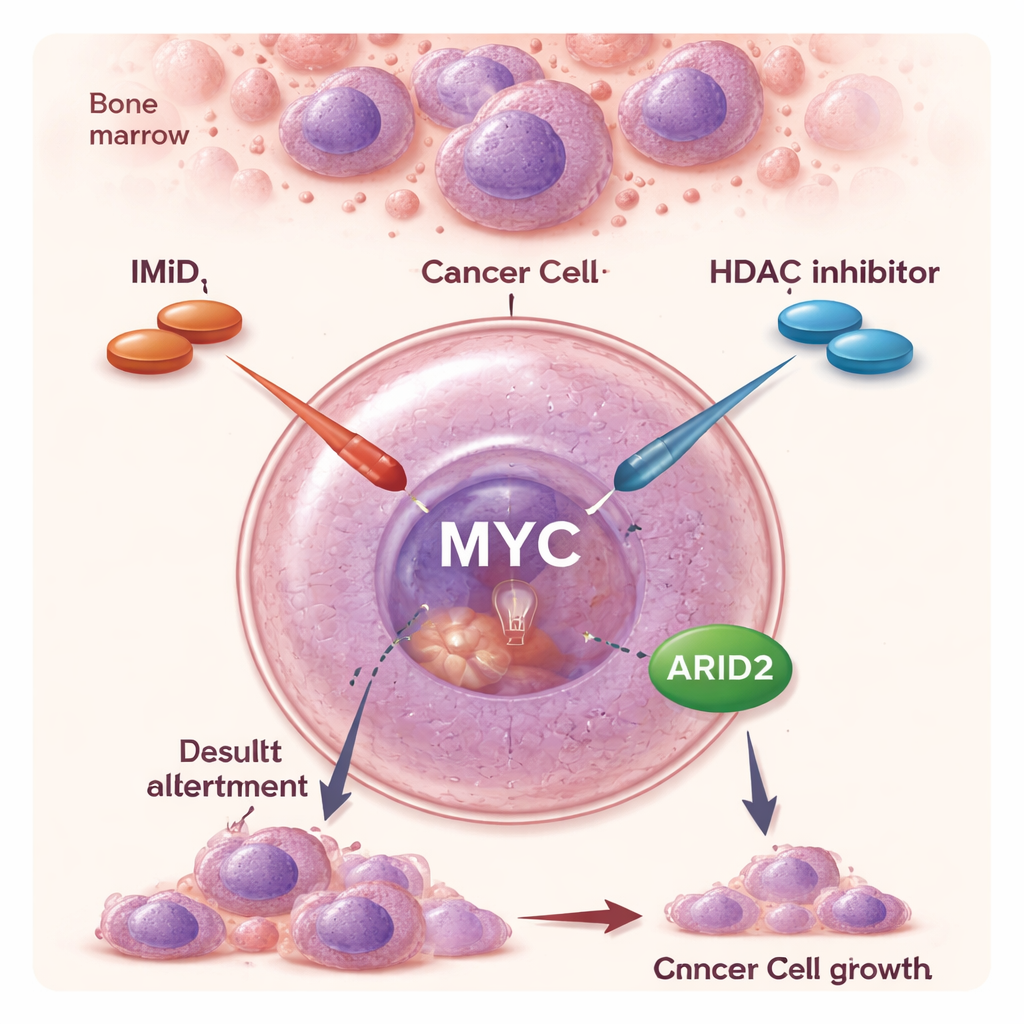
Dwie starsze klasy leków, jedno nowe partnerstwo
W ciągu ostatnich dwóch dekad IMiD i inne leki ukierunkowane znacząco przedłużyły przeżycie chorych na szpiczaka mnogiego. IMiD działają w nietypowy sposób: zamiast jedynie blokować białko, powodują znakowanie niektórych białek do zniszczenia, efektywnie eliminując je z komórki. W ten sposób osłabiają kluczowe sygnały przetrwania, na których polegają komórki szpiczaka. Inhibitory HDAC takie jak panobinostat działają inaczej — rozluźniają ciasne upakowanie DNA, szeroko zmieniając, które geny są aktywne. Jako pojedyncze środki HDAC inhibitory mają umiarkowany efekt i mogą powodować działania niepożądane, ale badania kliniczne sugerowały, że łączenie ich z IMiD daje znacznie silniejszą odpowiedź przeciwnowotworową, także u pacjentów, których choroba przestała reagować na same IMiD. Molekularne podłoże tej synergii pozostawało jednak niejasne.
Wspólny punkt nacisku: przyciszenie MYC
Naukowcy systematycznie testowali kombinacje kilku IMiD z różnymi inhibitorami HDAC na panelu linii komórkowych szpiczaka, stosując ustandaryzowany system punktacji, aby zmierzyć, o ile kombinacje są silniejsze niż pojedyncze leki. Odkryli, że pomalidomid razem z panobinostatem wykazywały szczególnie silną synergię w większości modeli komórkowych, a efekt ten zależał od białka zwanego cereblonem, którego IMiD używają do kierowania „ofiar” białkowych na degradację. Analiza globalnej aktywności genów wykazała, że panobinostat i pokrewny, szeroko działający inhibitor HDAC silnie wyłączają MYC — główny gen wzrostu często określany jako „silnik onkogenowy” w komórkach nowotworowych — a IMiD dokładały dodatkowy nacisk na ten sam węzeł. Gdy naukowcy zmusili komórki szpiczaka do ciągłej ekspresji MYC z opornego na leki źródła, potężny efekt pary leków w dużej mierze zniknął, co pokazuje, że wyciszenie MYC jest kluczowe dla ich współdziałania.
Przełamywanie oporności alternatywną drogą
Niektóre komórki szpiczaka są wrodzenie oporne na IMiD: mimo że oczekiwane wczesne cele są zniszczone, MYC i inne sygnały przetrwania nie zostają poprawnie wyciszone, więc komórki dalej rosną. W jednym z takich modeli standardowa ścieżka IMiD łącząca wczesne cele z MYC była „odłączona”. Zespół sprawdził, czy alternatywna droga może nadal łączyć IMiD z MYC. Skoncentrowali się na ARID2, składniku dużego mechanizmu przebudowy chromatyny zwanego kompleksem SWI/SNF. Wcześniejsze prace wykazały, że pomalidomid może znakować ARID2 do degradacji i że to pomaga obniżyć MYC. W komórkach opornych sam pomalidomid zmniejszał ARID2 tylko w niewielkim stopniu, częściowo dlatego, że komórka zwiększała produkcję ARID2 w odpowiedzi. Dodanie panobinostatu tłumiło sam gen ARID2, przerywając tę pętlę sprzężenia zwrotnego. Razem oba leki silnie obniżały poziom białka ARID2, a następnie MYC, prowadząc do silnego niszczenia komórek nowotworowych nawet w liniach opornych na IMiD.
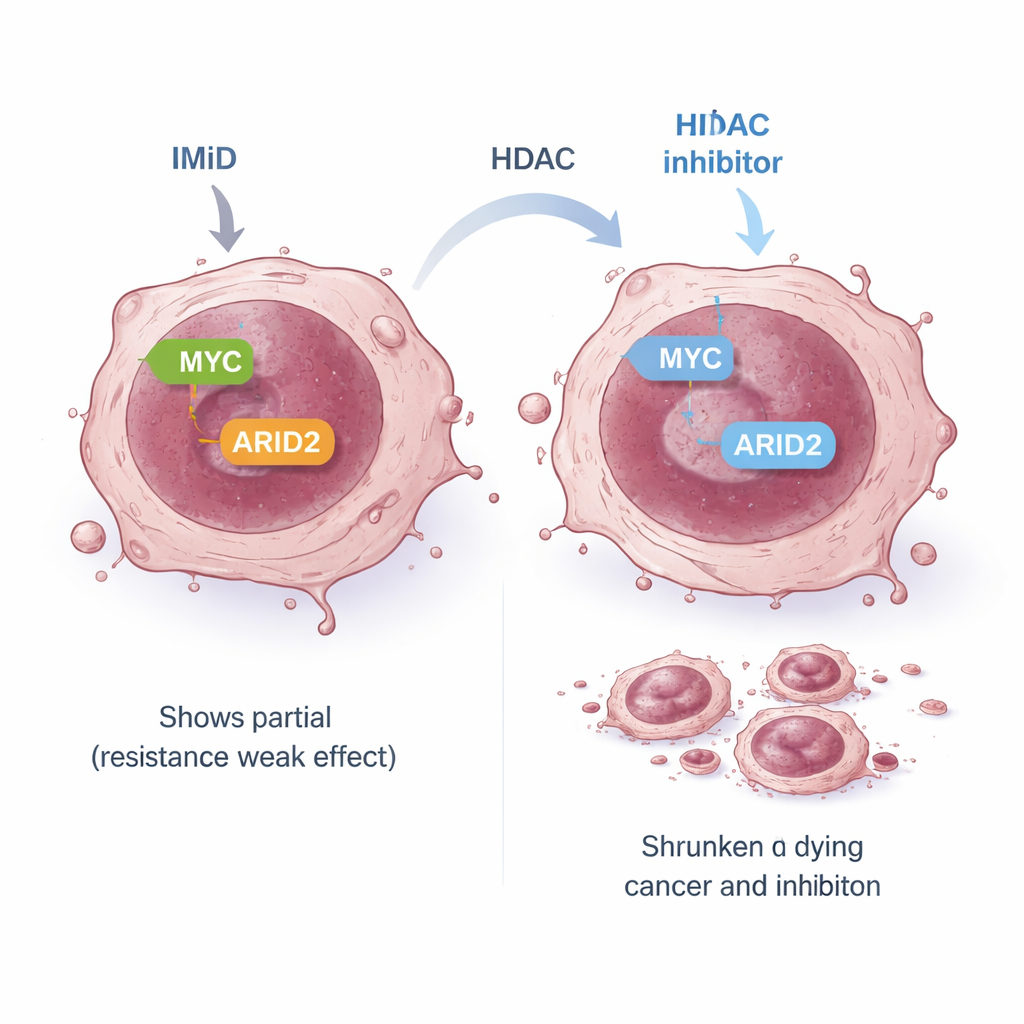
Ujawnienie szerszego punktu wrażliwości w komórkach nowotworowych
Ponieważ ARID2 jest tylko jednym członkiem kompleksu SWI/SNF, autorzy zastanawiali się, czy cały kompleks może stanowić terapeutyczną słabość. Stwierdzili, że inhibitory HDAC obniżają poziomy kilku komponentów SWI/SNF, a odrębna małocząsteczkowa substancja zaprojektowana do blokowania rdzeniowych „silników” kompleksu (BRG1/BRM) sama w sobie hamuje wzrost komórek szpiczaka i redukuje MYC. Co ważne, ten inhibitor SWI/SNF również działał synergistycznie zarówno z pomalidomidem, jak i panobinostatem, a kombinacja trzech leków jeszcze silniej obniżała ARID2 i MYC przy zdecydowanym zahamowaniu proliferacji komórek. Badania nad tym, które konkretne enzymy HDAC są zaangażowane, pozwoliły wyróżnić HDAC1 jako kluczowego gracza wspierającego oś ARID2–MYC, podczas gdy inne HDAC wydają się wpływać na MYC przez równoległe drogi.
Co to oznacza dla przyszłego leczenia szpiczaka
Dla osób niezaznajomionych z tematem istotne przesłanie jest takie, że komórki szpiczaka zdają się polegać na wspólnym „centrum kontroli wzrostu” skupionym wokół MYC, i że prowadzi do niego więcej niż jedna droga. Standardowa terapia IMiD uderza głównie w jedną drogę; w niektórych opornych nowotworach ta droga jest zablokowana, więc MYC pozostaje aktywny. To badanie pokazuje, że alternatywna droga — biegnąca przez ARID2 i kompleks SWI/SNF — pozostaje otwarta, i że zastosowanie panobinostatu razem z pomalidomidem może ją zamknąć. Świadome łączenie leków, które naciskają na MYC z kilku stron, może pozwolić pokonać niektóre formy wrodzonej oporności przy jednoczesnym użyciu niższych dawek każdego leku. Choć potrzebne są dalsze badania przedkliniczne i kliniczne, wyniki dają jaśniejszy plan do projektowania mądrzejszych, opartych na mechanizmach kombinacji dla pacjentów z trudnym do leczenia szpiczakiem mnogim.
Cytowanie: Yamamoto, J., Asatsuma-Okumura, T., Ito, T. et al. Synergistic targeting of the ARID2–MYC axis by pomalidomide and panobinostat overcomes intrinsic IMiD resistance in multiple myeloma. Sci Rep 16, 7375 (2026). https://doi.org/10.1038/s41598-026-37740-3
Słowa kluczowe: szpiczak mnogi, oporność na leki, pomalidomid, panobinostat, MYC