Clear Sky Science · pl
Mechanizm i ewolucyjne rozbieżności nowego utlenionego hydrolazy poliwinylowego alkoholu w Stenotrophomonas rhizophila QL-P4
Dlaczego powszechny „zielony” plastik wciąż zalega w środowisku
Poliwinylowy alkohol, czyli PVA, występuje w wszystkim, od kapsułek do detergentów po powłoki tekstylne i papier. Często jest reklamowany jako przyjazny dla środowiska, ponieważ w zasadzie mikroby mogą go rozkładać. Jednak w rzeczywistych rzekach, glebach i oceanach ten materiał podobny do plastiku rozkłada się wyjątkowo wolno i może utrzymywać się przez dekady jako fragmenty mikro‑ i nanoplastiku. W badaniu przyjrzano się bliżej jednemu z narzędzi przyrody do walki z PVA: niedawno odkrytemu enzymowi z bakterii glebowej, który potrafi rozcinać ten uporczywy polimer na mniejsze, bezpieczniejsze cząstki.
Mały pomocnik z gleby z dużym zadaniem
Naukowcy wcześniej wyizolowali bakterię Stenotrophomonas rhizophila QL-P4 z górskiej gleby w Chinach i stwierdzili, że potrafi ona rosnąć, wykorzystując PVA jako pokarm. W nowej pracy skoncentrowali się na jednym podejrzanym genie o nazwie BAY15_0160, który wyglądał, jakby kodował enzym zdolny do cięcia utlenionego PVA. Poprzez staranne usunięcie tego genu, przywrócenie go oraz wymuszone nadprodukcję wykazali, że BAY15_0160 jest niezbędny do efektywnego rozkładu PVA. Po usunięciu genu drobnoustrój stracił około 40% zdolności do konsumowania PVA; przywrócenie genu przywróciło wydajność, potwierdzając, że jego produkt jest kluczowym ogniwem w ścieżce degradacji.
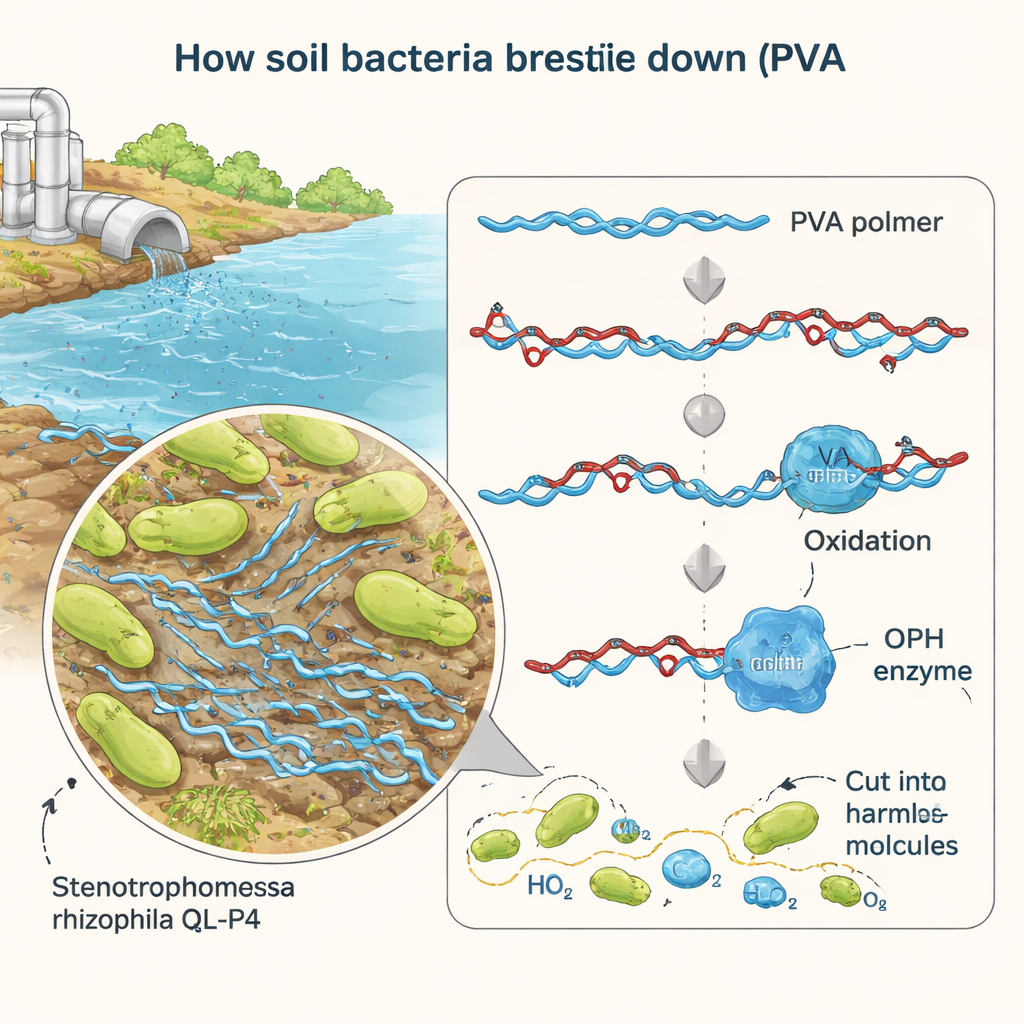
Pomiary, jak enzym wykonuje swoją pracę
Aby szczegółowo zbadać enzym, zespół wyprodukował go w dużych ilościach przy użyciu laboratoryjnych szczepów Escherichia coli. Oczyścili białko, które okazało się mieć około 35 kilodaltonów masy, i testowali jego aktywność w różnych warunkach. Używając prostego substratu, który uwalnia żółty barwnik po przecięciu, śledzili, jak szybko enzym działa przy różnych temperaturach i poziomach kwasowości. Enzym był najbardziej aktywny w warunkach zbliżonych do pokojowych (około 30 °C) i przy neutralnym pH, podobnym do wielu naturalnych wód. W tych łagodnych warunkach wykazał wysoką wydajność katalityczną, co oznacza, że każda cząsteczka enzymu może przetwarzać wiele cząsteczek substratu na sekundę — obiecująca wiadomość dla potencjalnych zastosowań w sprzątaniu środowiska.
Zbliżenie na molekularne nożyczki
Enzymy są miniaturowymi maszynami przyrody, a ich kształt determinuje ich funkcję. Badacze użyli nowoczesnych programów predykcyjnych, RoseTTAFold i AlphaFold, aby zbudować trójwymiarowe modele enzymu tnącego PVA, obecnie rozpoznanego jako nowy utleniony hydrolaza PVA, czyli OPH. Oba narzędzia zgodziły się, że enzym ma klasyczne fałdowanie „alfa/beta hydrolazy” występujące w wielu biologicznych nożyczkach. W jego centrum leży krótki motyw — często zapisywany jako Gly–X–Ser–X–Gly — który pomaga ustawić trio aminokwasów ( seryna, asparaginian i histydyna) do ataku na wiązania chemiczne. Symulacje komputerowe pokazały, że utlenione fragmenty PVA układają się w tym rowku, przy czym kluczowa seryna prawdopodobnie wykonuje pierwszy nacięcie w łańcuchu.
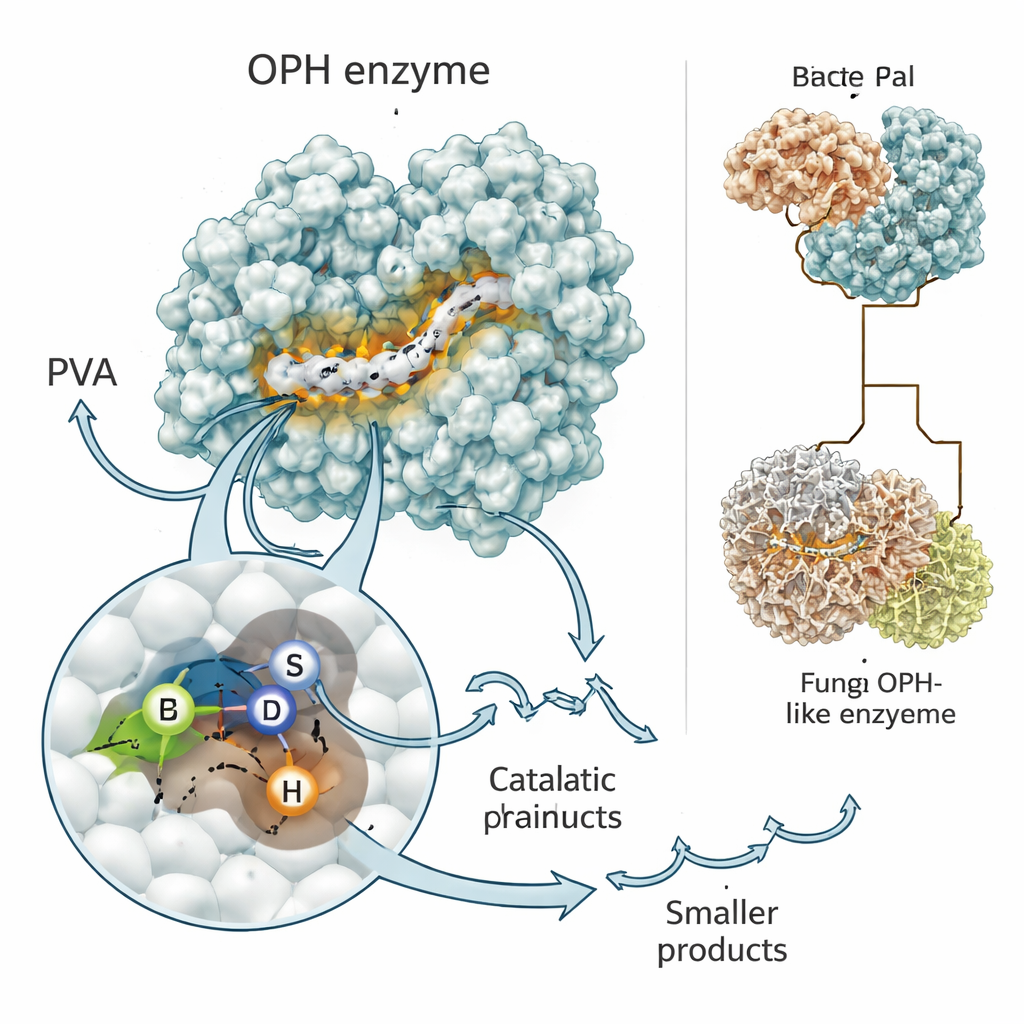
Sygnały, przełączniki i ewolucyjne skręty
Zespół badał również, które części enzymu są absolutnie niezbędne do jego funkcjonowania w bakterii. Jedien region blisko początku białka działa jak kod pocztowy, kierując enzym na zewnątrz komórki, gdzie znajduje się polimer PVA. Inny region zawiera aktywny motyw, który chwyta i przecina wiązania węgiel–węgiel tworzące plastik. Gdy naukowcy skonstruowali wersje genu pozbawione albo segmentu sygnałowego, albo motywu aktywnego miejsca, bakteria nadal wytwarzała RNA z tego genu, lecz nie mogła już efektywnie trawić PVA. Porównując sekwencje wielu bakterii i grzybów, znaleźli krewniaków tego enzymu, którzy dzielą ten sam rdzeń „tnący”, ale różnią się dodatkowymi częściami, w tym uderzającą wersją grzybową, która łączy domenę tnącą z wbudowanym transporterem, co sugeruje jeszcze wydajniejszą strategię importu i trawienia w ekstremalnych środowiskach, takich jak skały Antarktyki.
Co to oznacza dla oczyszczania zanieczyszczeń plastikowych
Dla osób niebędących specjalistami główne przesłanie jest takie, że naukowcy uczą się, jak niektóre mikroby naturalnie rozkładają pozornie biodegradowalny plastik, który inaczej utrzymuje się zbyt długo. Badanie identyfikuje pojedynczy enzym, OPH z S. rhizophila QL-P4, jako potężne molekularne nożyczki działające w łagodnych warunkach i ukierunkowane na kluczowy etap rozkładu PVA. Dzięki zrozumieniu jego struktury, warunków pracy i ewolucyjnych krewnych, badacze mogą zacząć projektować lepsze szczepy mikroorganizmów lub mieszanki enzymów dostosowane do oczyszczalni ścieków, zakładów przemysłowych czy skażonych gleb. W dłuższej perspektywie takie wnioski przybliżają nas do praktycznych, opartych na biologii rozwiązań zarządzania odpadami plastikowymi, zamiast pozostawiać je do akumulacji w środowisku.
Cytowanie: Zhou, Y., Bold, N., Feng, J. et al. Mechanism and evolutionary divergence of a novel oxidized polyvinyl alcohol hydrolase in Stenotrophomonas rhizophila QL-P4. Sci Rep 16, 6411 (2026). https://doi.org/10.1038/s41598-026-37715-4
Słowa kluczowe: polialkohol winylowy, biodegradacja, zanieczyszczenie plastikiem, enzymy mikrobialne, bioremediacja