Clear Sky Science · pl
Klasyfikacja glejaków według metabolizmu lipidów
Dlaczego tłuszcze w nowotworach mózgu mają znaczenie
Nowotwory mózgu zwane glejakami należą do najbardziej niebezpiecznych rodzajów raka, a mimo podobnej rozpoznawczości pacjenci mogą mieć bardzo różne rokowania. To badanie stawia pozornie proste pytanie o dalekosiężnych implikacjach: w jaki sposób sposoby wykorzystania tłuszczów – lipidów organizmu – wpływają na agresywność guza, odpowiedź na leczenie i czy te różnice można dostrzec na standardowych skanach mózgu? Śledząc wykorzystanie lipidów w setkach guzów, autorzy odkrywają ukryte podtypy glejaków, które mogą zmienić sposób prognozowania i projektowania terapii.
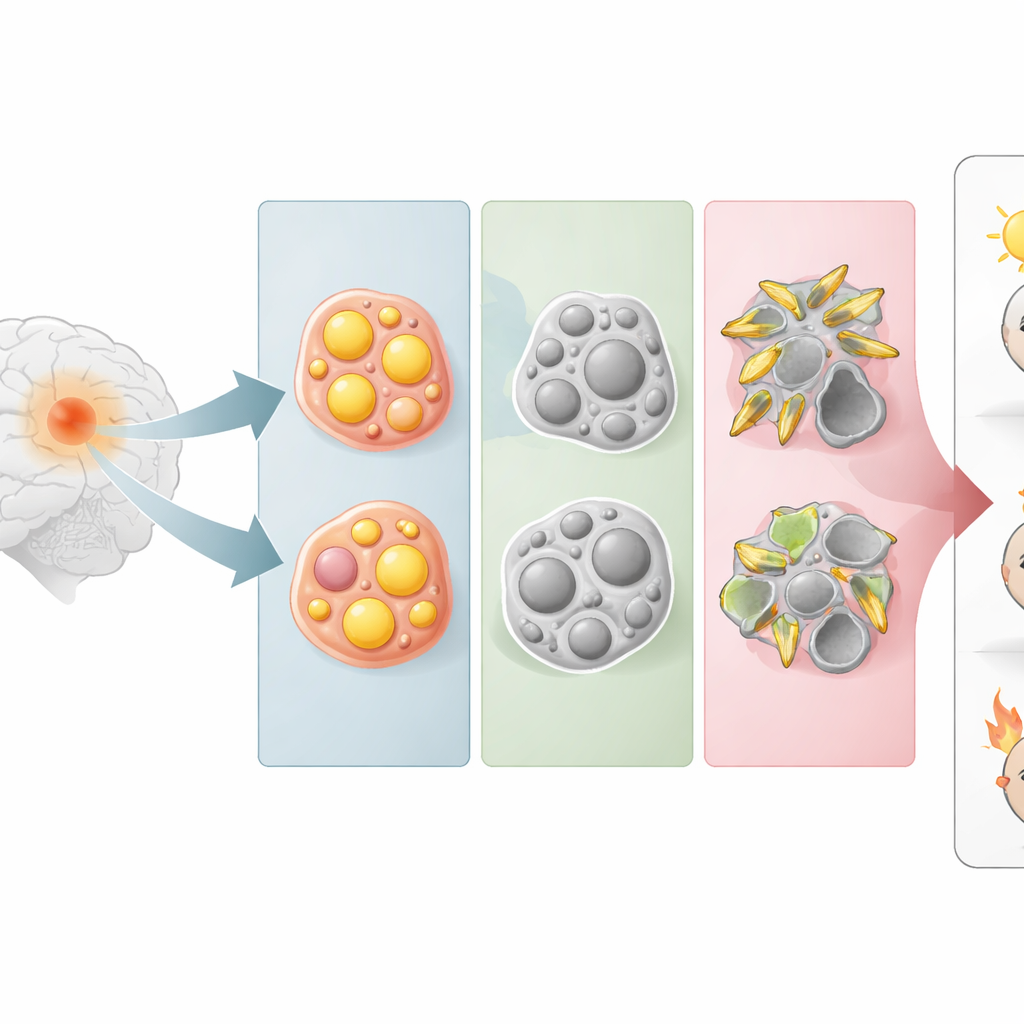
Trzy ukryte oblicza tego samego guza mózgu
Zamiast zaczynać od wyglądu komórek pod mikroskopem, badacze pogrupowali glejaki według siły aktywacji pięciu głównych szlaków lipidowych, w tym tych odpowiadających za lipidy steroidowe, trójglicerydy i sfingolipidy (kluczowe elementy błon komórkowych). Wykorzystując profile aktywności genów z dużych publicznych baz danych guza, odkryli, że glejaki naturalnie dzielą się na trzy grupy. Jedna grupa silnie opierała się na metabolizmie steroidów (typ ST), inna na metabolizmie trójglicerydów (typ TC), a trzecia na metabolizmie sfingolipidów (typ SP). Te metaboliczne podziały przecinają klasyczne kategorie guzów, ujawniając, że komórki o podobnych „zwyczajach” lipidowych mogą występować w morfologicznie różnych glejakach.
Od metabolizmu do prognozy pacjenta
Zespół sprawdził następnie, jak te trzy style używania tłuszczów odnoszą się do rzeczywistych wyników. Pacjenci, których guzy należały do grupy ST, generalnie mieli najdłuższe przeżycia, a ich guzy częściej były niższej klasy i nosiły znane korzystne zmiany genetyczne. Na drugim biegunie, guzy typu SP to zwykle wysokozłośliwe glejaki wielopostaciowe pozbawione protekcyjnych mutacji i występujące częściej u starszych pacjentów. Nawet po statystycznym uwzględnieniu stopnia zaawansowania i kluczowych markerów genetycznych przynależność do typu SP nadal przewidywała znacznie gorsze rokowanie, co sugeruje, że sposób, w jaki guz przetwarza sfingolipidy, oddaje niezależny wymiar zagrożenia, którego standardowe testy nie wychwytują.
Wrogie sąsiedztwo w mózgu
Bardziej szczegółowo autorzy przeanalizowali mikrośrodowisko guza – mieszankę komórek odpornościowych, naczyń krwionośnych i tkanek wspierających wokół nowotworu. Guzy typu SP wykazywały zatłoczone i konfliktowe środowisko immunologiczne, z obecnością zarówno komórek nastawionych na atak, jak i komórek hamujących, oraz silnymi sygnałami tłumiącymi efektywną odpowiedź przeciwnowotworową. Szlaki związane z szybkim wzrostem komórek, inwazją, tworzeniem nowych naczyń, bliznowaceniem i stanem zapalnym były w tym podtypie bardziej aktywne. Miary szacujące wrażliwość guzów na radioterapię sugerowały, że glejaki typu SP są najbardziej oporne na napromienianie, co koresponduje z ich gorszym przeżyciem. Dla porównania, guzy typu ST wyglądały na bardziej „spokojne”, z niższym poziomem tych agresywnych cech.
Odczytywanie metabolizmu guza z MRI
Ponieważ chirurgiczne pobranie tkanki jest inwazyjne i nie zawsze możliwe, badacze sprawdzili, czy standardowe badania rezonansu magnetycznego (MRI) mogą sugerować zachowanie lipidowe guza. Wyodrębnili ponad dwa tysiące subtelnych cech tekstury i kształtu z dwóch powszechnie stosowanych sekwencji MRI i wytrenowali model uczenia maszynowego, by odróżnić typ SP od pozostałych guzów. Model sprawdził się dobrze zarówno w zbiorze treningowym pochodzącym ze szpitala, jak i w niezależnym publicznym zbiorze walidacyjnym, poprawnie rozróżniając guzy typu SP znacznie częściej niż przypadek. Sugeruje to, że metaboliczny odcisk palca szczególnie agresywnego podtypu glejaka zostawia wykrywalny ślad na rutynowych badaniach obrazowych mózgu.
Kluczowy gen w centrum agresywnej sieci
Aby przejść od szerokich szlaków do konkretnych celów, zespół poszukiwał genów centralnych w sieciach związanych z lipidami, silnie nadaktywnych w guzach typu SP, powiązanych z gorszym przeżyciem i precyzyjnie rozróżniających guzy SP od innych. Trzy geny – GLA, GLB1 i HSD3B7 – spełniały wszystkie kryteria. Wszystkie były bardziej aktywne w glejakach typu SP i razem tworzyły silny diagnostyczny sygnaturę. Autorzy skupili się na HSD3B7, którego rola w guzach mózgu była dotąd w dużej mierze niepoznana. Barwienia tkankowe 100 pacjentów z glejakami wykazały, że białko HSD3B7 występowało w wyższym stężeniu w guzach bardziej zaawansowanych i bardziej złośliwych, a pacjenci z wysokim poziomem tego białka mieli istotnie krótsze przeżycie.
Jak jeden gen lipidowy przekształca ekosystem guza
Analizy pojedynczych komórek, które charakteryzują komórki w obrębie guza, wykazały, że HSD3B7 jest aktywny nie tylko w komórkach nowotworowych, lecz także w kilku typach komórek odpornościowych i podporowych. Wysoka aktywność tego genu wiązała się z siecią sygnałów promujących tworzenie naczyń, przewlekły stan zapalny i unikanie odpowiedzi immunologicznej. Komunikacja między pewnymi ochronnymi typami komórek wydawała się osłabiona, podczas gdy samonapędzające pętle w komórkach wspierających guz były wzmocnione. Razem te wzorce sugerują, że zwiększona aktywność HSD3B7 pomaga tworzyć i podtrzymywać wrogie mikrośrodowisko sprzyjające wzrostowi guza i oporności na terapię.
Co to oznacza dla pacjentów i przyszłej opieki
Praktycznie rzecz biorąc, praca ta pokazuje, że glejaki można sensownie podzielić na trzy podtypy oparte na metabolizmie lipidów, przy czym podtyp SP, bogaty w sfingolipidy, wyróżnia się jako szczególnie niebezpieczny i oporny na leczenie. Różnice te nie są jedynie akademickie: można je odczytać z rutynowych skanów MRI za pomocą zaawansowanej analizy obrazów i powiązać z konkretnymi genami, takimi jak HSD3B7, które mogą stać się przyszłymi celami leków. Chociaż konieczne są dalsze prace eksperymentalne, by sprawdzić, czy blokowanie tych szlaków lipidowych może spowolnić guzy lub poprawić skuteczność radioterapii, badanie oferuje nową metaboliczną perspektywę na raka mózgu i przybliża pole do bardziej spersonalizowanych, biologicznie ugruntowanych decyzji terapeutycznych.
Cytowanie: Tu, S., Zhang, P., Chi, X. et al. Lipid metabolism classification of gliomas. Sci Rep 16, 8219 (2026). https://doi.org/10.1038/s41598-026-37697-3
Słowa kluczowe: glejak, metabolizm lipidów, obrazowanie nowotworów mózgu, radiomika, mikrośrodowisko guza