Clear Sky Science · pl
Dietą wysokotłuszczową przebudowano sieci regulacji genów w okolicy przedpokwitaniowej
Dlaczego twój mózg ma znaczenie w cukrzycy
Większość osób kojarzy cukrzycę z problemem trzustki i poziomu cukru we krwi, ale mózg także odgrywa w niej istotną rolę. W tym badaniu analizowano, jak dieta wysokotłuszczowa i silne eksperymentalne leczenie zmieniają aktywność genów w niewielkim, lecz ważnym regionie mózgu zwanym okolicą przedpokwitaniową. Mapując, które komórki mózgowe „resetują się” w trakcie remisji cukrzycy, badacze mają nadzieję wskazać ścieżki do nowych terapii wykorzystujących zdolność mózgu do współregulacji poziomu glukozy.
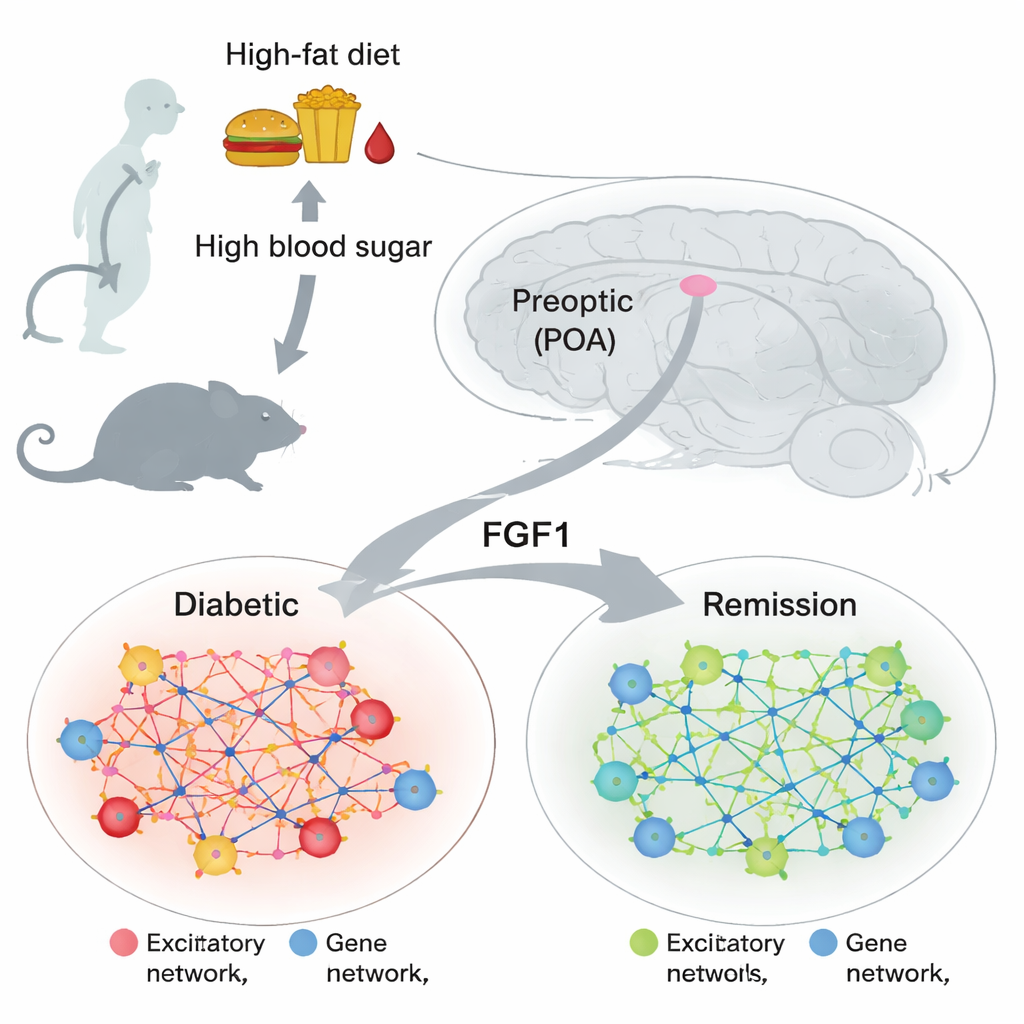
Małe centrum mózgowe o dużym wpływie metabolicznym
Obszar przedpokwitaniowy leży z przodu podwzgórza — części mózgu, która kontroluje temperaturę ciała, sen, apetyt i sygnalizację hormonalną. Wcześniejsze badania wykazały, że komórki w tym rejonie wpływają na gospodarkę glukozową i reakcję na ciepło, ale ich rola w cukrzycy była słabo poznana. Równocześnie inne prace pokazały, że pojedyncza dawka białka fibroblastowego czynnika wzrostu 1 (FGF1), podana do mózgu, może wprowadzić otyłe, cukrzycowe myszy w długotrwałą remisję. Pojawiło się więc kluczowe pytanie: które komórki mózgowe i programy genowe zmieniają się, gdy poziom glukozy ulega normalizacji, i czy podobne zmiany pojawiają się w obrębie okolicy przedpokwitaniowej?
Odczytywanie aktywności genów komórka po komórce
Aby to ustalić, zespół sięgnął po pojedynczo-komórkowe sekwencjonowanie RNA, technikę mierzącą, które geny są włączone w tysiącach pojedynczych komórek jednocześnie. Ponownie przeanalizowali istniejący zestaw danych od myszy, u których po leczeniu FGF1 wystąpiła remisja, koncentrując się na komórkach nerwowych podwzgórza. Przy użyciu narzędzi statystycznych zidentyfikowali grupy genów, które wzrastały lub malały równocześnie w przejściu zwierząt ze stanu cukrzycowego do remisji. Te „moduły remisji” działają jak odciski palców powrotu do zdrowia: zamiast śledzić pojedynczy gen, rejestrują skoordynowane przesunięcia w obrębie wielu genów w konkretnych typach neuronów.
Dieta wysokotłuszczowa, komórki mózgowe i obniżone zużycie energii
Następnie badacze porównali te moduły remisji z aktywnością genów w innym zestawie danych, który obejmował komórki z okolicy przedpokwitaniowej zdrowych myszy. Najpierw podzielili neurony na dwie szerokie klasy: komórki pobudzające, które zwykle zwiększają aktywność w swoich obwodach, oraz komórki hamujące, które ją tłumią. U myszy cukrzycowych leczonych FGF1 oba typy neuronów wykazywały szerokie obniżenie ekspresji genów związanych z produkcją energii — szczególnie tych zaangażowanych w fosforylację oksydacyjną, oddychanie komórkowe i mitochondrialny aparat napędzający aktywne komórki. W neuronach pobudzających duży „turkusowy” moduł genów związanych z wykorzystaniem energii i aktywnością synaptyczną był silnie wyciszony podczas remisji, co sugeruje, że te komórki stają się mniej wymagające metabolicznie, gdy poziom cukru jest kontrolowany.
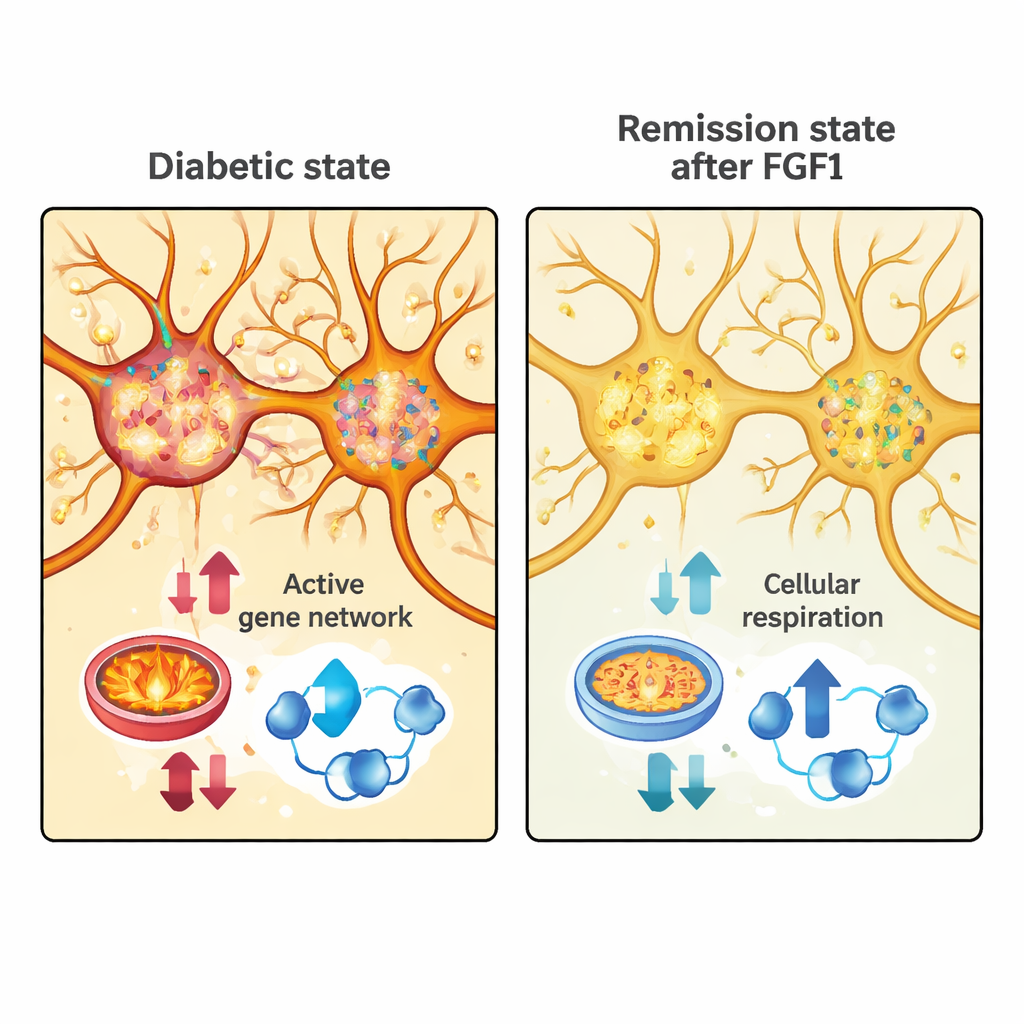
Śledzenie sygnatur remisji do konkretnych grup neuronów
Kolejnym krokiem było sprawdzenie, czy te wzorce genowe związane z remisją pokrywają się z określonymi populacjami komórek w okolicy przedpokwitaniowej. Poprzez obliczeniowe połączenie obu zestawów danych, odkryli, że niektóre klastry neuronów przedpokwitaniowych wykazywały ekspresję wielu tych samych genów, które zmieniały się po leczeniu FGF1. Wyróżnili kilka genów — takich jak Trpc4, Dgkg i Ryr3 — które znalazły się w centrum tych analiz. Za pomocą wysoce czułej metody mikroskopowej RNAscope pokazali, że te geny rzeczywiście są eksprymowane w odrębnych strefach okolicy przedpokwitaniowej myszy, głównie w regionach grzbietowych. Potwierdza to ich status jako rzeczywistych markerów konkretnych grup neuronów, które mogą uczestniczyć w odpowiedzi mózgu na choroby metaboliczne.
Co to oznacza dla przyszłych terapii cukrzycy
Dla osób niebędących specjalistami konkluzja jest taka, że cukrzyca to nie tylko problem poziomu cukru we krwi — to także problem sieci neuronalnych mózgu. Badanie pokazuje, że gdy u myszy występuje remisja cukrzycy, pewne neurony przedpokwitaniowe przechodzą w stan o niższym zapotrzebowaniu na energię i zmieniają swoją aktywność genową w skoordynowany sposób. Definiując te moduły remisji i łącząc je z konkretnymi typami komórek oraz genami markerowymi, praca daje mapę drogową do przyszłych eksperymentów: naukowcy mogą teraz celować w te konkretne neurony, aby przetestować, jak wpływają na kontrolę glukozy, otyłość i powiązane powikłania. W dłuższej perspektywie lepsze zrozumienie tych obwodów mózgowych może pomóc w opracowaniu terapii uzupełniających lub nawet zastępujących zawodne organy poprzez wykorzystanie wrodzonej kontroli metabolizmu przez mózg.
Cytowanie: Lazaro, O., Beimfohr, C., App, B. et al. High fat diet remodels the gene regulatory networks in the preoptic area. Sci Rep 16, 7042 (2026). https://doi.org/10.1038/s41598-026-37692-8
Słowa kluczowe: mózg i cukrzyca, obszar przedpokwitaniowy, dieta wysokotłuszczowa, sieci genowe, remisja po FGF1