Clear Sky Science · pl
Sygnał interferonu typu I definiuje nowy sygnaturę chorobową w keratynocytach ludzkich z xeroderma pigmentosum C
Dlaczego światło słoneczne może być tak groźne dla niektórych osób
Dla większości z nas słońce to ciepło i witamina D. Ale dla osób z rzadkim schorzeniem genetycznym zwanym xeroderma pigmentosum C (XP‑C) nawet umiarkowane światło dzienne może powodować ciężkie uszkodzenia skóry i bardzo duże ryzyko raka skóry. To badanie sięga dalej niż dobrze znany problem z naprawą DNA w XP‑C i odkrywa ukrytą warstwę nadaktywnej, przypominającej odpowiedź immunologiczną sygnalizacji wewnątrz komórek skóry, dając nowe wskazówki, dlaczego ich skóra jest tak wrażliwa i zapalna po ekspozycji na słońce.
Kiedy naprawa DNA zawodzi w skórze
Nasze komórki skóry nieustannie naprawiają uszkodzenia DNA wywołane promieniowaniem UVB ze słońca. Białko zwane XPC jest jednym z pierwszych „czujników”, które wykrywają zmiany spowodowane UV i aktywują szeroki zespół naprawczy. W XP‑C mutacje w genie XPC osłabiają ten wczesny etap alarmowy, więc uszkodzenia spowodowane UV kumulują się zamiast być naprawiane. Pacjenci z XP‑C rozwijają raki skóry tysiące razy częściej niż ogólna populacja i muszą rygorystycznie unikać słońca. Choć defekt naprawy DNA jest dobrze znany, mniej jasne było, jak przebudowuje on wewnętrzne systemy komunikacji komórkowej — zwłaszcza te kontrolujące stany zapalne.
Badanie sygnałów komórkowych w czasie
Aby rozwiązać ten problem, badacze zmodyfikowali ludzkie keratynocyty — główne komórki zewnętrznej warstwy skóry — tak, by całkowicie nie miały XPC, i porównali je z inaczej identycznymi komórkami normalnymi. Oba typy komórek wystawiono na starannie dobrany, rzeczywisty poziom promieniowania UVB zbliżony do dawki umiarkowanego oparzenia słonecznego. Następnie zbadano komórki na dwóch etapach. Godzinę po napromieniowaniu zmierzono aktywność wielu enzymów zwanych kinazami tyrozynowymi, które włączają i wyłączają sygnały przez dodawanie małych znaczników fosforanowych. Dwadzieścia cztery godziny później użyto zaawansowanej spektrometrii mas, aby uzyskać szerokie ujęcie tysięcy białek i zobaczyć, które z nich wzrosły lub zmalały w obfitości. To dwustopniowe podejście pozwoliło śledzić zarówno wczesne „sygnały alarmowe”, jak i późniejsze „odpowiedzi wtórne” wewnątrz komórek.
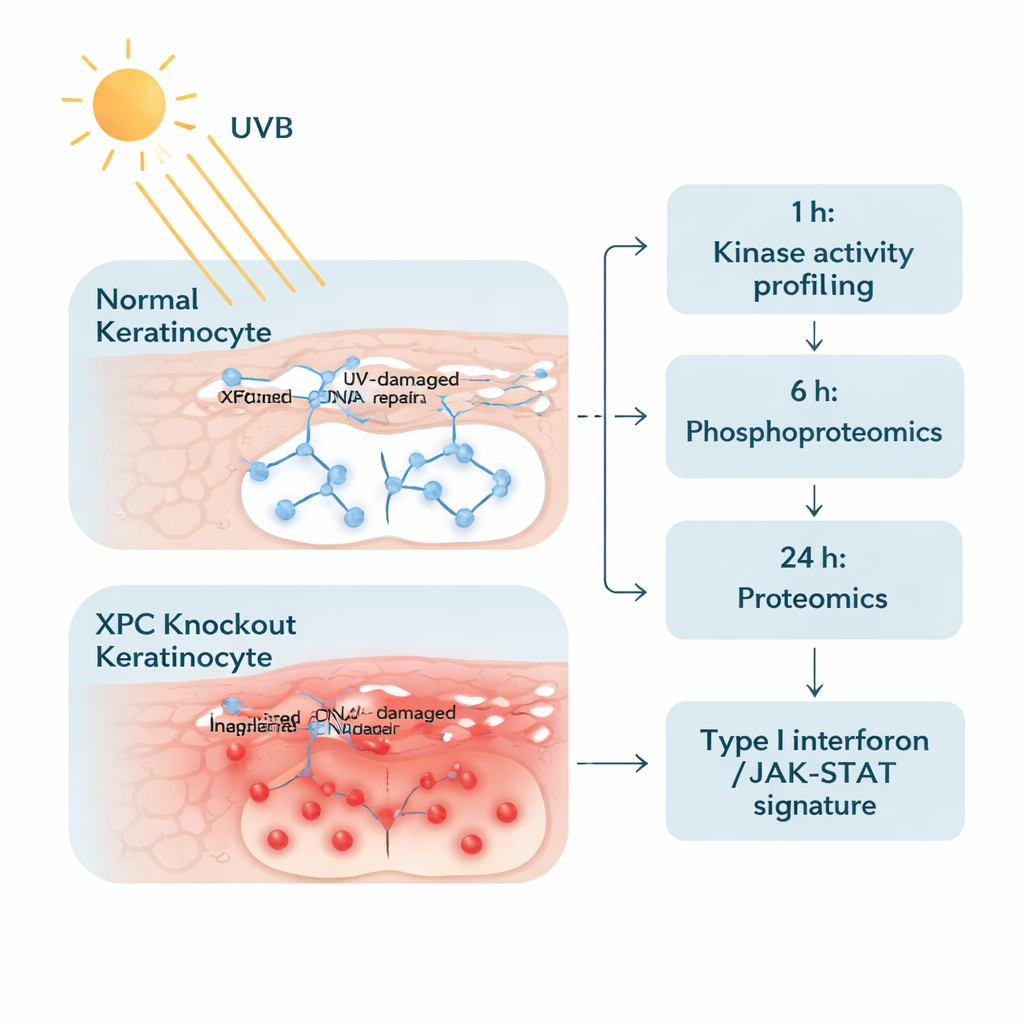
Rozświetla się ścieżka zapalna
Wczesny przegląd kinaz ujawnił, że keratynocyty pozbawione XPC reagują na UVB falą fosforylacji na ponad stu miejscach w porównaniu z komórkami normalnymi. Co ważne, wiele z tych zmian skupiało się w szlaku sygnalizacyjnym JAK/STAT — centralnej trasie komunikacyjnej zwykle wykorzystywanej przez przekaźniki immunologiczne, takie jak interferony. Markery związane z JAK1, JAK2, JAK3, TYK2 i białkami STAT były bardziej aktywne w komórkach XP‑C, nawet przed ekspozycją na UVB, i dodatkowo wzrastały po napromieniowaniu. Sugeruje to, że komórki były „ustawione” w stanie wysokiej gotowości, gotowe wzmacniać sygnały zapalne za każdym razem, gdy napotkały stres spowodowany UV.
Geny alarmowe w stylu interferonu w komórkach skóry
Późniejsze, szersze badanie białek potwierdziło i rozszerzyło ten obraz. W komórkach z wyciszonym XPC, szczególnie po UVB, setki białek uległy zmianom, a duży klaster odpowiadał genom zwykle włączanym przez interferony typu I — tym samym sygnałom przeciwwirusowym, które organizm wykorzystuje do zwalczania zakażeń. Białka takie jak MX1, MX2, IFIT1, IFIT2, IFIT3, ISG15, OAS1 i IRF9, klasyczne „geny stymulowane interferonem”, były silnie podwyższone. Analizy sieci i szlaków powiązały te białka z powrotem ze szlakiem JAK/STAT i sygnalizacją interferonu typu I jako dominującym motywem. Dalsze doświadczenia z użyciem western blot potwierdziły, że kluczowe białka STAT były silniej fosforylowane, a te reakcje na interferony były produkowane na znacznie wyższych poziomach w komórkach XP‑C niż w normalnych keratynocytach, zarówno w stanie spoczynku, jak i szczególnie po ekspozycji na UVB.
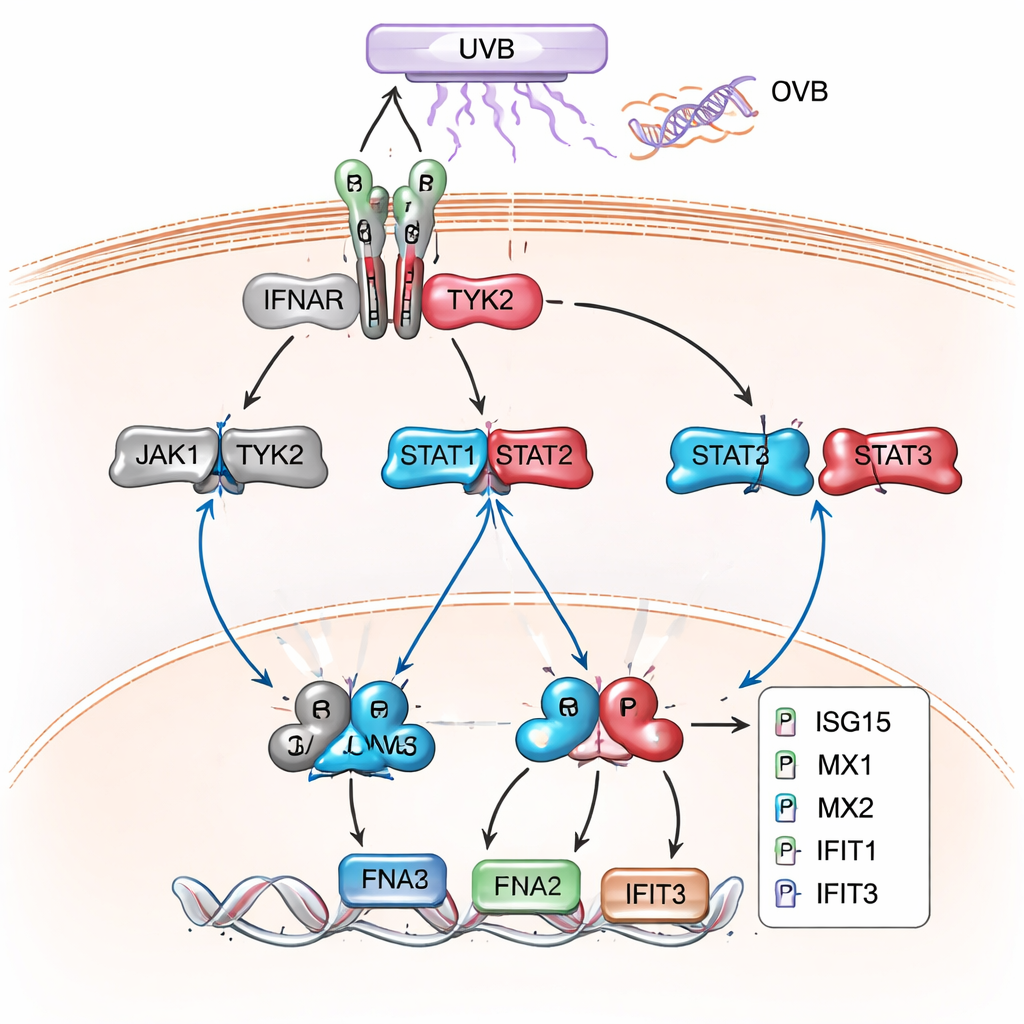
Co to oznacza dla pacjentów i przyszłych terapii
Łącznie wyniki te pokazują, że XP‑C to nie tylko choroba wadliwej naprawy DNA; charakteryzuje się także uporczywym, przypominającym interferon stanem zapalnym wewnątrz komórek skóry, napędzanym przez szlak JAK/STAT i nasilanym przez światło UV. Dla laika oznacza to, że keratynocyty XP‑C zachowują się tak, jakby nieustannie walczyły z niewidzialną infekcją za każdym razem, gdy widzą światło słoneczne, nakładając przewlekłe zapalenie na nieodwrócone uszkodzenia DNA. Choć badanie nie testuje bezpośrednio terapii, sugeruje możliwość, że precyzyjnie dobrane leki celujące w JAK/STAT lub powiązane obwody zapalne mogłyby w przyszłości pomóc zmniejszyć uszkodzenia wywołane przez UV u pacjentów z XP‑C, a być może także w innych zapalnych schorzeniach skóry, które dzielą tę molekularną sygnaturę.
Cytowanie: Nasrallah, A., Rezvani, HR., Belmudes, L. et al. Type I interferon signaling defines a novel disease signature in xeroderma pigmentosum C human keratinocytes. Sci Rep 16, 6559 (2026). https://doi.org/10.1038/s41598-026-37662-0
Słowa kluczowe: xeroderma pigmentosum, rak skóry, naprawa DNA, sygnalizacja interferonowa, szlak JAK STAT