Clear Sky Science · pl
Wnt-3a nasila produkcję TNF-α w mikrogleju stymulowanym LPS niezależnie od kanonicznej ścieżki β-kateniny
Dlaczego zapalenie mózgu ma znaczenie
Wiele zaburzeń mózgu, w tym choroba Parkinsona, wiąże się z przewlekłym zapaleniem. W tym procesie rezydujące w mózgu komórki układu odpornościowego, zwane mikroglejem, mogą przejść ze stanu ochronnego w nadaktywny stan, który uszkadza sąsiednie neurony. Badanie stawia aktualne pytanie: czy cząsteczka sygnałowa Wnt‑3a, długo uważana za działającą uspokajająco i ochronnie, może w pewnych warunkach pogarszać zapalenie? Odpowiedź jest bardziej złożona, niż się spodziewano, i pokazuje, dlaczego ta sama cząsteczka bywa korzystna w jednym kontekście, a szkodliwa w innym.
Posłaniec o dwóch obliczach
Proteiny Wnt to rodzina chemicznych przekaźników, które kierują rozwojem mózgu, utrzymują komórki mózgowe w dorosłości i kształtują ich odpowiedź na uraz. Jednym z najlepiej zbadanych członków jest Wnt‑3a, zwykle kojarzona z „kanoniczną” drogą sygnałową, która stabilizuje wewnątrzkomórkowo białko β‑kateninę. W wielu układach uruchomienie tej drogi wydaje się tłumić zapalenie i wspierać przeżycie neuronów, dlatego niektórzy badacze zastanawiali się, czy wzmocnienie działania Wnt‑3a mogłoby chronić wrażliwe neurony dopaminergiczne w chorobie Parkinsona. Jednak proteiny Wnt mogą też przekazywać sygnały przez alternatywne, „niekanoniczne” szlaki, które mogą napędzać zapalenie, a to, która ścieżka dominuje, zależy od typu komórki i jej stanu.
Kiedy spokojne komórki pozostają spokojne
Aby zbadać te możliwości, naukowcy badali pierwotne mikrogleje hodowane z mózgów myszy. Najpierw przyjrzeli się mikroglejom w stanie spoczynkowym i wystawili je jedynie na działanie Wnt‑3a. W tych spokojnych warunkach Wnt‑3a nie zwiększała uwalniania kluczowych molekuł zapalnych, takich jak TNF‑α czy IL‑1β. Mimo aktywacji niektórych rodzajów sygnalizacji wewnątrzkomórkowej, mikroglej nie przeszedł w silnie zapalny stan. Sugeruje to, że w zdrowym, niezapalnym mózgu podanie samej Wnt‑3a może mieć niewielki bezpośredni wpływ na produkcję czynników zapalnych przez mikroglej.
Gdy zapalone komórki są dodatkowo pobudzane
Obraz zmienił się diametralnie, gdy mikroglej najpierw został wyzwolony do stanu zapalnego przy użyciu lipopolisacharydu bakteryjnego (LPS), standardowego narzędzia laboratoryjnego naśladującego infekcję. Jak oczekiwano, samo LPS spowodowało silny wzrost produkcji TNF‑α. Jednak gdy Wnt‑3a dodano razem z LPS, mikroglej uwalniał istotnie więcej TNF‑α niż przy samym LPS, podczas gdy IL‑1β nie wzrosło dodatkowo. Dokładne pomiary wykazały, że ten wzrost TNF‑α nie wynikał z silniejszej aktywacji zwykłej NFκB-owej drogi zapalnej ani z dodatkowej aktywacji kanonicznej ścieżki β‑kateniny. Zablokowanie drogi β‑kateniny białkiem DKK1 nie zlikwidowało napływu TNF‑α wywołanego przez Wnt‑3a, co wskazuje, że oczekiwana „przeciwzapalna” ścieżka nie była odpowiedzialna.
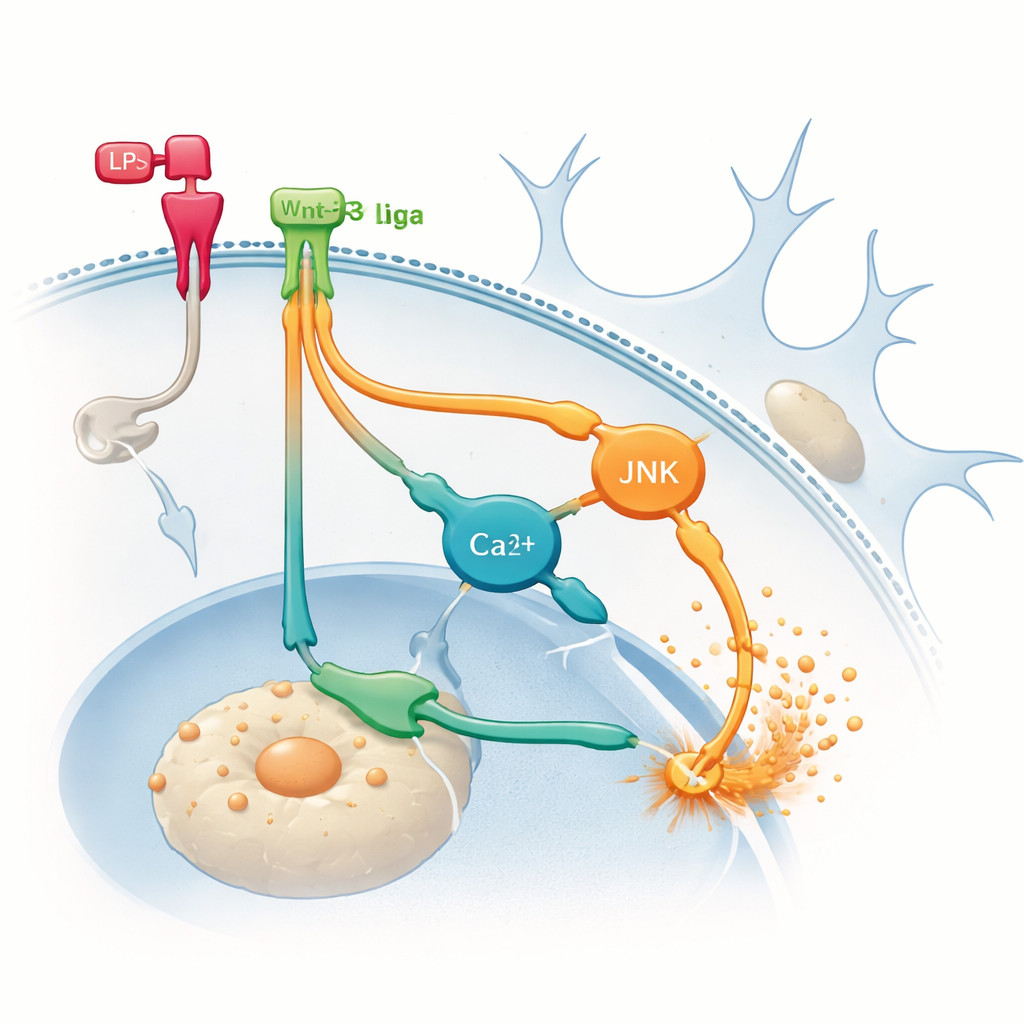
Ukryte szlaki, które dolewają oliwy do ognia
Aby ustalić, skąd pochodzi dodatkowe zapalenie, zespół zwrócił się ku alternatywnym niekanonicznym ścieżkom wykorzystywanym przez proteiny Wnt. Farmakologicznie zablokowali dwa odgałęzienia sygnalizacyjne w mikrogleju: jedno obejmujące białko JNK, a drugie związane ze zmianami poziomu wapnia w komórce. Hamowanie któregokolwiek z tych odgałęzień zmniejszało produkcję TNF‑α indukowaną przez LPS i, co istotne, uniemożliwiało Wnt‑3a dalsze zwiększenie TNF‑α. Wyniki te sugerują, że gdy mikroglej jest już zapalny, Wnt‑3a może przełączać się na przeważne używanie niekanonicznych dróg, które wzmacniają sygnały zapalne zamiast je tłumić. Innymi słowy, ten sam przekaźnik może obrać inną wewnętrzną ścieżkę w zależności od stanu wyjściowego komórki, co prowadzi do bardzo różnych skutków.
Testowanie w modelu Parkinsona
Naukowcy zapytali następnie, czy takie zachowanie Wnt‑3a w mikrogleju przełoży się na większe efekty wobec neuronów w żywym mózgu. Infundowali Wnt‑3a bezpośrednio do komór mózgu myszy, którym podawano toksynę MPTP, szeroko stosowany model uszkodzenia neuronów dopaminergicznych i aktywacji mikrogleju przypominający Parkinsona. Jak przewidywano, MPTP zmniejszył liczbę neuronów dopaminergicznych i zwiększył liczbę mikrogleju w obszarze śródmózgowia kluczowym dla ruchu. Jednak dodatkowa Wnt‑3a nie pogorszyła dodatkowo utraty neuronów ani nie zmieniła istotnie liczby mikrogleju w porównaniu ze zwierzętami otrzymującymi pojazd. W tym złożonym ustawieniu in vivo Wnt‑3a ani nie uratowała, ani wyraźnie nie nasiliła szkodliwych efektów toksyny w badanym okresie.
Co to oznacza dla przyszłych terapii
Podsumowując, badanie pokazuje, że Wnt‑3a nie jest prostym włącznikiem albo wyłącznikiem zapalenia mózgu. W cichym mikrogleju ma niewielki efekt, ale w już zapalonych komórkach może wybiórczo zwiększać uwalnianie TNF‑α poprzez niekanoniczne ścieżki sygnałowe, niezależnie od klasycznej drogi β‑kateniny. Jednocześnie dodanie Wnt‑3a w modelu myszy przypominającym Parkinsona nie wykazało oczywistej ochrony ani krótkoterminowego pogorszenia neuronów dopaminergicznych. Dla osób myślących o przyszłych terapiach kluczowy wniosek jest taki, że modulowanie sygnalizacji Wnt będzie wymagać ostrożnego uwzględnienia kontekstu komórkowego. Terapie oparte na Wnt‑3a lub pokrewnych molekułach mogą być pomocne w niektórych sytuacjach, ale w innych mogą zaszkodzić, jeśli niezamierzenie nasilą szkodliwe zapalenie.
Cytowanie: Federici, G., Stayte, S., Rentsch, P. et al. Wnt-3a exacerbates production of TNF-α in LPS stimulated microglia independent of the β-catenin canonical pathway. Sci Rep 16, 8222 (2026). https://doi.org/10.1038/s41598-026-37653-1
Słowa kluczowe: zapalenie mózgu, mikroglej, sygnalizacja Wnt, choroba Parkinsona, TNF-alfa