Clear Sky Science · pl
Charakterystyka in vitro domeny katalitycznej ludzkiej histonowej deacetylazy 5
Dlaczego drobne przełączniki w pakowaniu DNA mają znaczenie
W każdej komórce nasze DNA jest nawinięte na białka działające jak szpule, co pozwala upakować metry materiału genetycznego w mikroskopijną przestrzeń. To, czy gen jest włączony czy wyłączony, często zależy od małych chemicznych znaczników na tych białkach–szpulach. Niniejsze badanie skupia się na jednym takim „przełączniku” białkowym nazwanym HDAC5, powiązanym z chorobami serca, schorzeniami mózgu, nowotworami i innymi dolegliwościami. Zrozumienie działania HDAC5 na poziomie molekularnym może utorować drogę do precyzyjniejszych leków o mniejszych skutkach ubocznych.
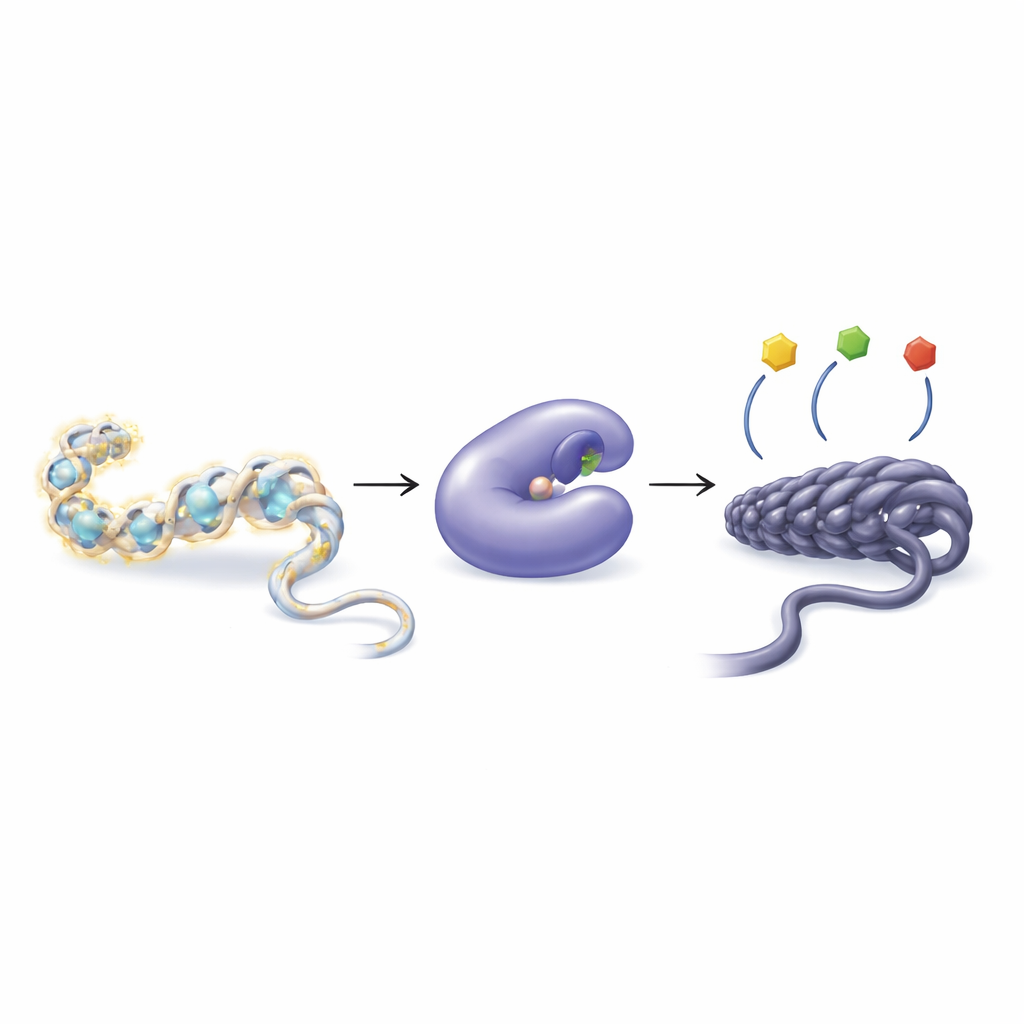
Jak komórki regulują geny za pomocą drobnych chemicznych znaczników
Nasze DNA nie unosi się swobodnie, lecz jest nawinięte na białka nazywane histonami, tworząc strukturę zwaną chromatyną. Komórki mogą przyłączać lub usuwać małe grupy chemiczne, takie jak grupy acetylowe, z ogonków histonowych, aby rozluźnić lub usztywnić chromatynę. Luźniejsze upakowanie zwykle ułatwia odczyt genów; ciaśniejsze skłania do ich wyciszenia. Równowagę tę kontrolują dwie grupy enzymów: histonowe acetylotransferazy dodają grupy acetylowe, a histonowe deacetylazy (HDAC) je usuwają. Zaburzenie tej równowagi może przyczyniać się do wielu chorób, w tym nowotworów, chorób serca, zaników mięśni czy zaburzeń układu odpornościowego.
Dlaczego HDAC5 jest obiecującym, ale trudnym celem terapeutycznym
HDACy tworzą dużą rodzinę spokrewnionych enzymów podzielonych na kilka klas. Wiele stosowanych obecnie leków blokuje jednocześnie wiele typów HDAC, co może hamować ważne funkcje fizjologiczne i prowadzić do silnych działań niepożądanych. HDACy klasy IIa, w tym HDAC5, wyróżniają się tym, że występują obficie w określonych tkankach, takich jak mózg, serce i mięśnie szkieletowe, oraz współdziałają z innymi białkami w regulacji kluczowych sieci genowych. HDAC5 często działa jako most, przyprowadzając bardzo aktywnego partnera enzymatycznego (HDAC3) do wybranych genów, co pozwala zagęszczać chromatynę i wyciszać te geny. Dzięki takim wyspecjalizowanym rolom HDAC5 jest atrakcyjnym celem dla bardziej selektywnych leków, jednak brak szczegółowych danych biochemicznych i brak struktury o wysokiej rozdzielczości jego centrum katalitycznego utrudnia racjonalne projektowanie inhibitorów.
Odtwarzanie HDAC5 w probówce
Aby rozwiązać tę lukę, badacze wyprodukowali jedynie rdzeń katalityczny ludzkiego HDAC5 – część przeprowadzającą reakcję chemiczną – w bakteriach, oczyszczali go i potwierdzili, że w roztworze tworzy stabilne, jednokunitowe białko. Następnie przetestowali jego aktywność w różnych stężeniach soli i przy różnych poziomach kwasowości. Aktywność HDAC5 pozostawała wysoka w szerokim zakresie zasolenia i osiągała maksimum w lekko zasadowych warunkach, podobnych do tych panujących w wielu komórkach. Używając specjalnych fluorescencyjnych związków testowych, stwierdzili, że naturalna forma HDAC5 rozpoznaje tylko jeden specyficzny typ substratu często stosowany do badania enzymów klasy IIa. Korzystając z wcześniejszych prac nad spokrewnionymi HDACami, zastąpili pojedynczy aminokwas (histydynę) tyrozyną w krytycznym miejscu. Co znamienne, ta drobna zmiana pozwoliła mutantowi HDAC5 wydajnie przetwarzać oba typy substratów testowych, ujawniając, jak jeden resztowy aminokwas w centrum aktywnym kieruje chemicznymi preferencjami enzymu.
Testowanie i porównanie dwóch nowych kandydatów na leki
Zespół następnie przebadał dwa eksperymentalne inhibitory HDAC5, znane jako NT160 i FFK24. Związki te wykorzystują nowszą grupę wiążącą cynk, która unika części toksyczności i słabej selektywności obserwowanej przy starszych lekach opartych na hydroxamacie. Mierząc, jak każdy inhibitor spowalniał działanie HDAC5 w kontrolowanych reakcjach, autorzy wyznaczyli bardzo niskie stałe hamowania w zakresie nanomolowym, co oznacza, że oba związki silnie przylegają do enzymu. NT160 wiązał się konsekwentnie około dziesięć razy mocniej niż FFK24. Aby zrozumieć przyczynę, badacze użyli dokowania komputerowego z wykorzystaniem struktury rdzenia HDAC5 przewidzianej przez AlphaFold. Oba inhibitory miały wspólny fragment, który wnikał głęboko w kieszeń aktywną i kontaktował się z jonem metalu, lecz ogon NT160 tworzył dodatkowe stabilizujące kontakty z określonymi aminokwasami w tej kieszeni. Te dodatkowe interakcje prawdopodobnie wyjaśniają jego wyższą moc działania.
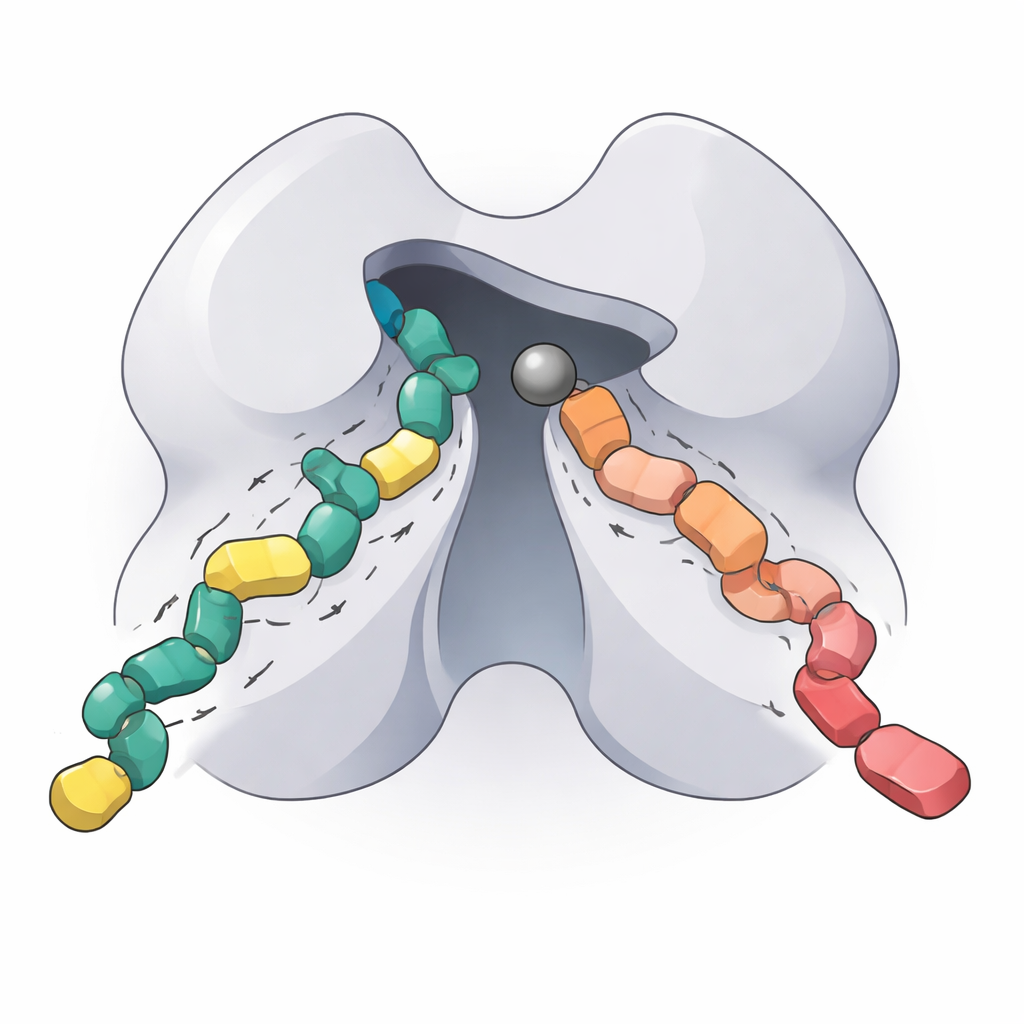
Co to oznacza dla przyszłych terapii celowanych
Odtwarzając funkcjonalny rdzeń HDAC5, określając jego optymalne warunki pracy, analizując, jak pojedyncza zmiana aminokwasu zmienia jego zachowanie, oraz kwantyfikując wiązanie dwóch inhibitorów następnej generacji, badanie dostarcza szczegółowego biochemicznego „odcisku palca” ważnego, dotąd słabo scharakteryzowanego enzymu. Dla osób niebędących specjalistami kluczowe przesłanie jest takie, że HDAC5 pomaga kontrolować, czy niektóre geny są włączone czy wyłączone, i że precyzyjne dostrojenie tego przełącznika może być wartościowe w leczeniu chorób serca, neurodegeneracji, nowotworów oraz zaburzeń układu odpornościowego. Nowe wnioski i narzędzia przedstawione w pracy powinny pomóc badaczom w projektowaniu selektywnych leków przeciwko HDAC5 i klasie IIa, działających tam, gdzie są potrzebne, przy minimalizowaniu niepożądanych efektów w innych częściach organizmu.
Cytowanie: Mammen, C., Hornung, F.M., Anzenhofer, C. et al. In vitro characterization of the catalytic domain of human histone deacetylase 5. Sci Rep 16, 7935 (2026). https://doi.org/10.1038/s41598-026-37633-5
Słowa kluczowe: histonowa deacetylaza 5, regulacja epigenetyczna, inhibitory HDAC, ukierunkowana terapia przeciwnowotworowa, struktura chromatyny