Clear Sky Science · pl
H19 zwiększa proliferację i inwazję raka trzustki poprzez osłabienie hamującego działania miR-29c-5p na ATF2/ECM1
Dlaczego ta ukryta komórkowa wiadomość ma znaczenie
Rak trzustki jest jednym z najgroźniejszych nowotworów, częściowo dlatego, że często wykrywany jest późno i oporny na dostępne terapie. W badaniu tym autorzy wykraczają poza geny kodujące białka i koncentrują się na „cichych” komunikatach genetycznych — długich i krótkich cząsteczkach RNA — które pomagają guzom trzustki rosnąć, rozsiewać się i unikać leczenia. Odkrywając, jak jedna długa cząsteczka RNA o nazwie H19 i jej mały partner miR-29c-5p współdziałają, przekształcając otoczenie guza, autorzy wskazują nowy molekularny schemat, który może prowadzić do wcześniejszej diagnozy i bardziej precyzyjnych terapii.
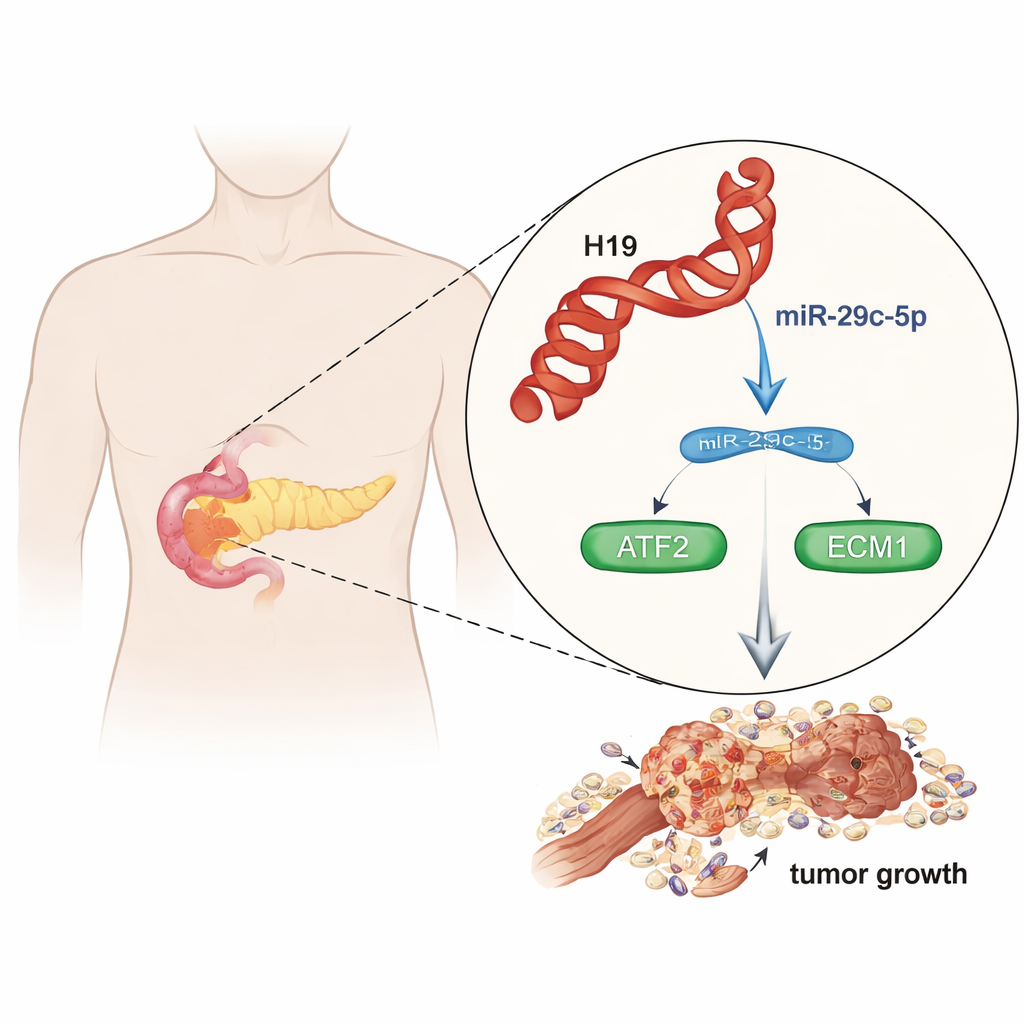
Niebezpieczny nowotwór z niewieloma opcjami
Gruczolakorak przewodowy trzustki (PDAC) ma pięcioletnie przeżycie poniżej 10 procent, głównie dlatego, że wcześnie się rozsiewa i słabo reaguje na chemioterapię. Badacze coraz bardziej doceniają rolę RNA niekodujących — komunikatów genetycznych, które nie kodują białek — jako silnych przełączników kontrolujących zachowanie nowotworu. W tej pracy zespół przeanalizował duże, publiczne zbiory danych i próbki pacjentów, wykazując, że jedno z takich długich RNA niekodujących, H19, jest konsekwentnie podwyższone w guzach trzustki w porównaniu z tkanką normalnej trzustki. Pacjenci, których guzy miały wyższe poziomy H19, umierali wcześniej, co sugeruje, że H19 nie jest jedynie przelotnym zjawiskiem, lecz czynnikiem napędzającym agresywną chorobę.
Jak H19 przechyla równowagę wewnątrz komórek guza
W komórkach H19 lokalizuje się głównie w płynnym cytoplazmie, gdzie może oddziaływać z innymi RNA zamiast bezpośrednio modyfikować DNA. Autorzy odkryli, że H19 działa jak cząsteczkowa gąbka: wiąże i zatrzymuje małe RNA o nazwie miR-29c-5p, które w przeciwnym razie pomagałoby hamować rozwój guza. Gdy poziomy H19 są wysokie, pozostaje mniej wolnego miR-29c-5p do pełnienia jego nadzorującej roli. Eksperymenty laboratoryjne wykazały, że zwiększenie H19 powodowało szybsze mnożenie się komórek raka trzustki i ich większą zdolność do przemieszczania się przez sztuczne membrany, natomiast wyciszenie H19 spowalniało wzrost i inwazję. Przywrócenie miR-29c-5p odwrotnie modyfikowało wiele z tych szkodliwych efektów, co wskazuje na swoisty konflikt między tymi dwiema cząsteczkami.
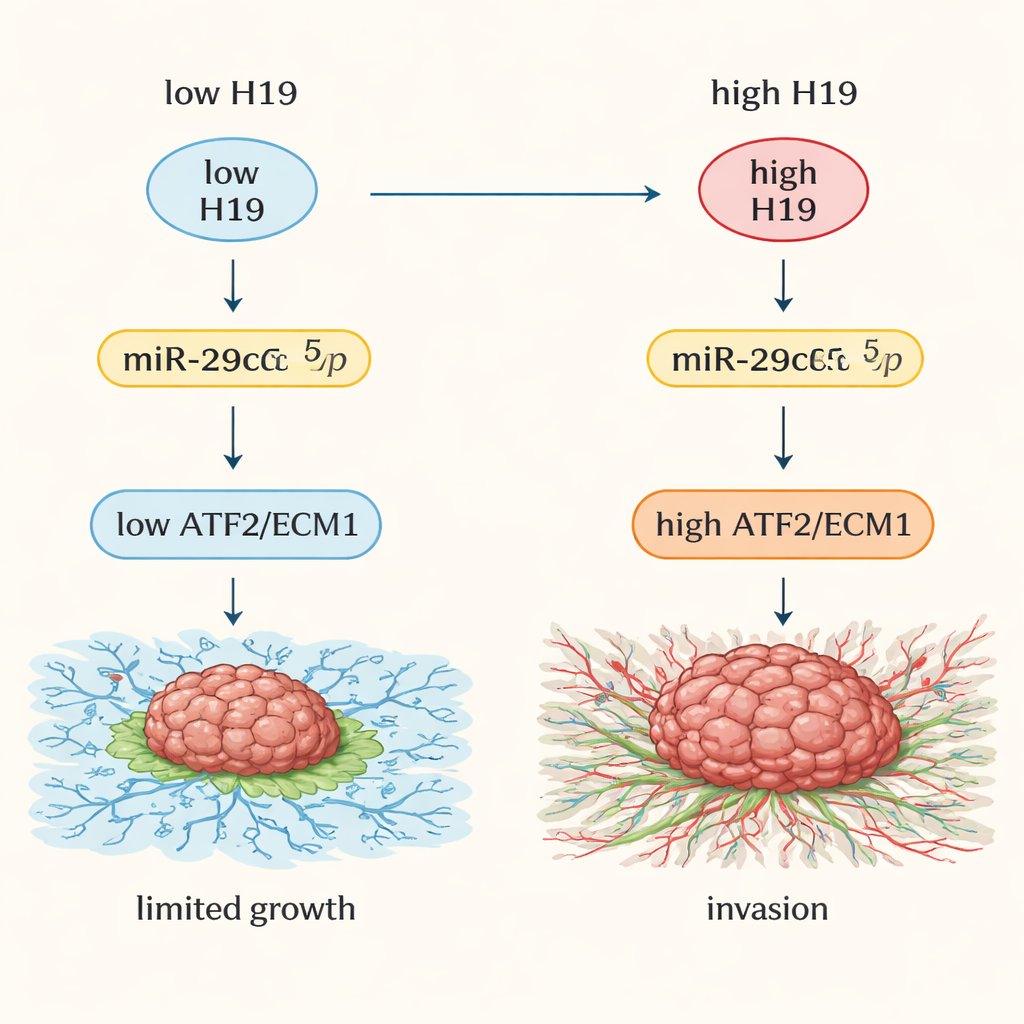
Docelowe efekty: zwalnianie hamulców wzrostu guza
Małe RNA miR-29c-5p zwykle pomaga powstrzymywać dwa istotne białka: ATF2, regulator genowy w jądrze komórkowym, oraz ECM1, białko kształtujące matrycę otaczającą komórki. Gdy miR-29c-5p zostaje pochłonięte przez H19, poziomy ATF2 i ECM1 rosną. W próbkach guzów i publicznych bazach danych dotyczących nowotworów zarówno ATF2, jak i ECM1 były znacznie wyższe w raku trzustki niż w tkance normalnej. Wysokie poziomy tych białek korelowały z bardziej zaawansowaną chorobą i gorszym przeżyciem. W eksperymentach na komórkach i myszach obniżenie H19 lub zwiększenie miR-29c-5p redukowało ATF2 i ECM1, zmniejszało guzy i osłabiało ich inwazyjne zachowanie. Dowody wskazują na reakcję łańcuchową: H19 wiąże miR-29c-5p, uwalniając ATF2, który następnie zwiększa ECM1, sprzyjając powstaniu sztywnego, włóknistego środowiska korzystnego dla rozsiewu guza.
Od mechanizmu do potencjalnych markerów i terapii
Poza odwzorowaniem tego szlaku sygnałowego badacze sprawdzili, czy te molekuły mogą pomóc lekarzom w diagnozie lub klasyfikacji raka trzustki. Analiza danych pacjentów wykazała, że poziomy ECM1 i ATF2 rozróżniały tkankę nowotworową od normalnej trzustki z wysoką dokładnością, w niektórych analizach przewyższając powszechnie stosowany marker krwi CA19-9. Pacjenci, których guzy miały niższe ECM1, mieli tendencję do dłuższego przeżycia, co sugeruje, że może on służyć jako sygnał ostrzegawczy przed agresywną chorobą. Chociaż zestaw próbek klinicznych z tego szpitala był niewielki, spójność wyników w niezależnych bazach danych i eksperymentach na zwierzętach wzmacnia tezę, że ta oś jest kluczowa w biologii PDAC.
Co to oznacza dla pacjentów i przyszłych badań
Mówiąc prościej, badanie pokazuje, że długie „ciche” RNA H19 pomaga guzom trzustki rosnąć i inwadować, neutralizując ochronne małe RNA miR-29c-5p i uwalniając dwa promujące wzrost białka, ATF2 i ECM1. Ten czteroczęściowy łańcuch — H19/miR-29c-5p/ATF2/ECM1 — pomaga guzowi przebudować swoje otoczenie na sprzyjające gniazdo i ściśle wiąże się z gorszymi wynikami. Choć potrzebne są większe badania kliniczne, praca sugeruje, że pomiar składników tej ścieżki mógłby pomóc w identyfikacji pacjentów wysokiego ryzyka, a leki ukierunkowane na blokowanie H19 lub ECM1 albo przywracanie aktywności miR-29c-5p mogą kiedyś zaoferować nowe opcje wobec tego notorycznie trudnego do leczenia nowotworu.
Cytowanie: Rui, M., Xiuping, L., Yu, C. et al. H19 enhances pancreatic cancer proliferation and invasion by reducing miR-29c-5p’s inhibitory effects on ATF2/ECM1. Sci Rep 16, 7623 (2026). https://doi.org/10.1038/s41598-026-37632-6
Słowa kluczowe: rak trzustki, RNA niekodujące, H19, mikrośrodowisko guza, biomarkery