Clear Sky Science · pl
Odpowiedź na wielopokoleniową ekspozycję na tlenek grafenu u szczepów Acheta domesticus wyselekcjonowanych pod kątem długości życia
Dlaczego drobne świerszcze są ważne dla nowych materiałów
Tlenek grafenu to rosnąca gwiazda w przemyśle i medycynie, wykorzystywana od zaawansowanej elektroniki po nośniki leków. Jednak w miarę jak te ultracienkie arkusze węglowe wychodzą z laboratorium do codziennego użytku, prawdopodobnie trafiają do gleby, wód i łańcuchów pokarmowych. W tym badaniu użyto nieoczekiwanego bohatera — pospolitego świerszcza domowego — by postawić proste, lecz istotne pytanie: co się dzieje, gdy organizmy żywe i ich potomstwo żyją przez wiele pokoleń z niskimi stężeniami tlenku grafenu w diecie?
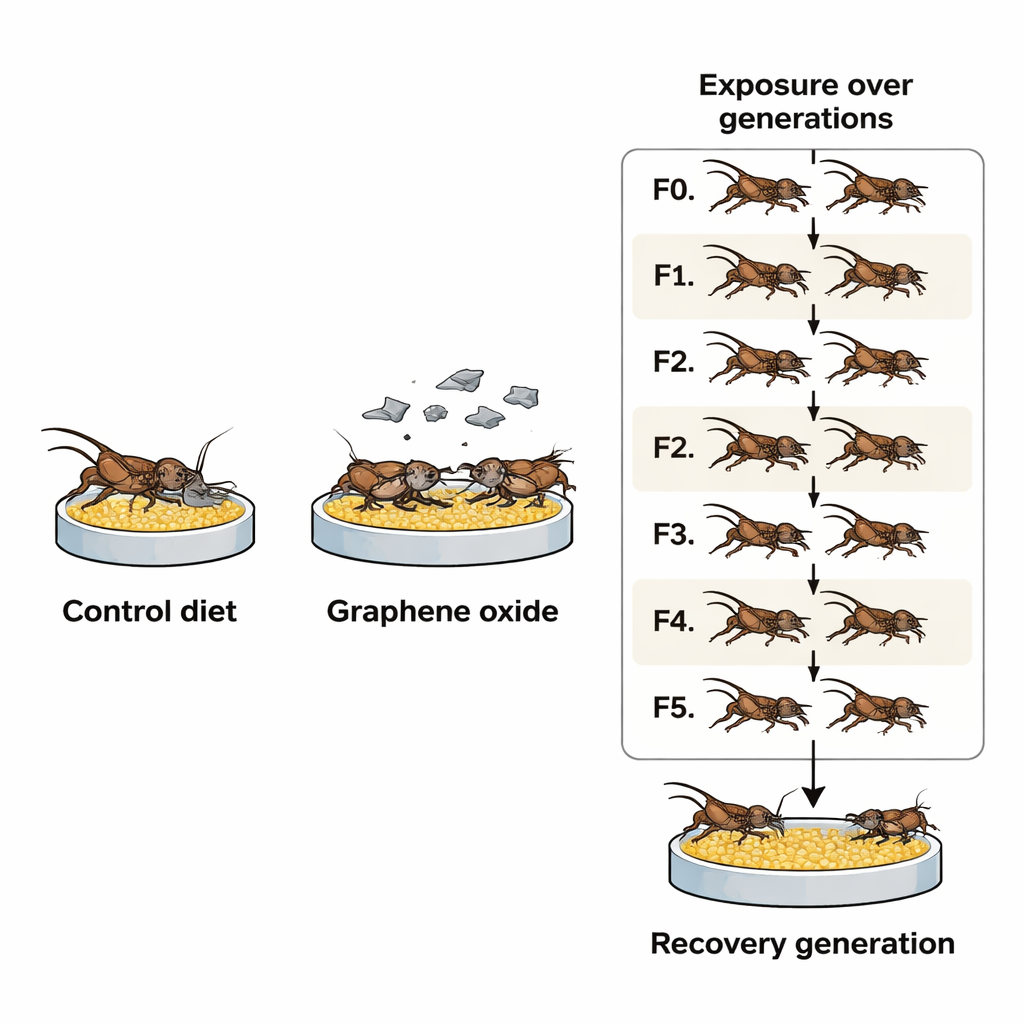
Śledzenie rodzin na przestrzeni sześciu pokoleń
Naukowcy hodowali dwa szczepy świerszcza domowego przez sześć pokoleń: standardowy szczep „dziki” oraz specjalnie wyhodowany, długowieczny szczep. Młode świerszcze w każdym pokoleniu otrzymywały albo normalny pokarm, albo pokarm z niewielką domieszką tlenku grafenu, w dawkach znacznie niższych niż te zwykle stosowane w testach toksyczności w laboratorium. Pierwsze pięć pokoleń (F0–F4) jadło dietę z dodatkiem tlenku grafenu, natomiast szóste „pokolenie rekonwalescencji” (F5) dostało z powrotem czysty pokarm. Porównując grupy w czasie, zespół mógł obserwować, jak komórki zwierząt radzą sobie z trwałą ekspozycją i czy to doświadczenie wydaje się być „zapamiętywane” przez kolejne pokolenia.
Co działo się w jelitach
Ponieważ spożyty tlenek grafenu styka się najpierw z układem pokarmowym, naukowcy skupili się na komórkach jelitowych. Za pomocą cytometrii przepływowej — techniki mierzącej szybko właściwości tysięcy komórek — śledzili kilka wskaźników zdrowia komórek. Obejmowały one uszkodzenia DNA, stabilność mitochondriów (elektrowni komórkowych), odsetek komórek zmierzających do zaprogramowanej śmierci (apoptozy) oraz oznaki recyklingu i sprzątania komórkowego (autofagia). Razem te miary dają wielowarstwowy obraz poziomu stresu komórek i skuteczności ich reakcji.
Trzy odrębne fazy odpowiedzi komórkowej
Komórki świerszczy nie reagowały w prosty, jednokierunkowy sposób. Zamiast tego autorzy wyróżnili trzy szerokie fazy. W pierwszym narażonym pokoleniu (F0) komórki jelitowe wykazywały wyraźne uszkodzenia DNA i zaburzoną aktywność mitochondriów, ale zaskakująco niewielki wzrost śmierci komórek — co sugeruje, że organizmy próbowały naprawiać, a nie poświęcać uszkodzone komórki. W następnej fazie (F1–F3) równowaga ta się przesunęła: uszkodzenia DNA pozostały podwyższone, problemy mitochondrialne utrzymywały się, a udział umierających komórek wzrósł, podczas gdy ogólna żywotność komórek spadła. Intrygująco, niższa dawka tlenku grafenu często wywoływała silniejsze negatywne efekty niż wyższa, co może wynikać z tego, że łagodny stres nie był wystarczająco silny, by w pełni uruchomić ochronne mechanizmy naprawcze.
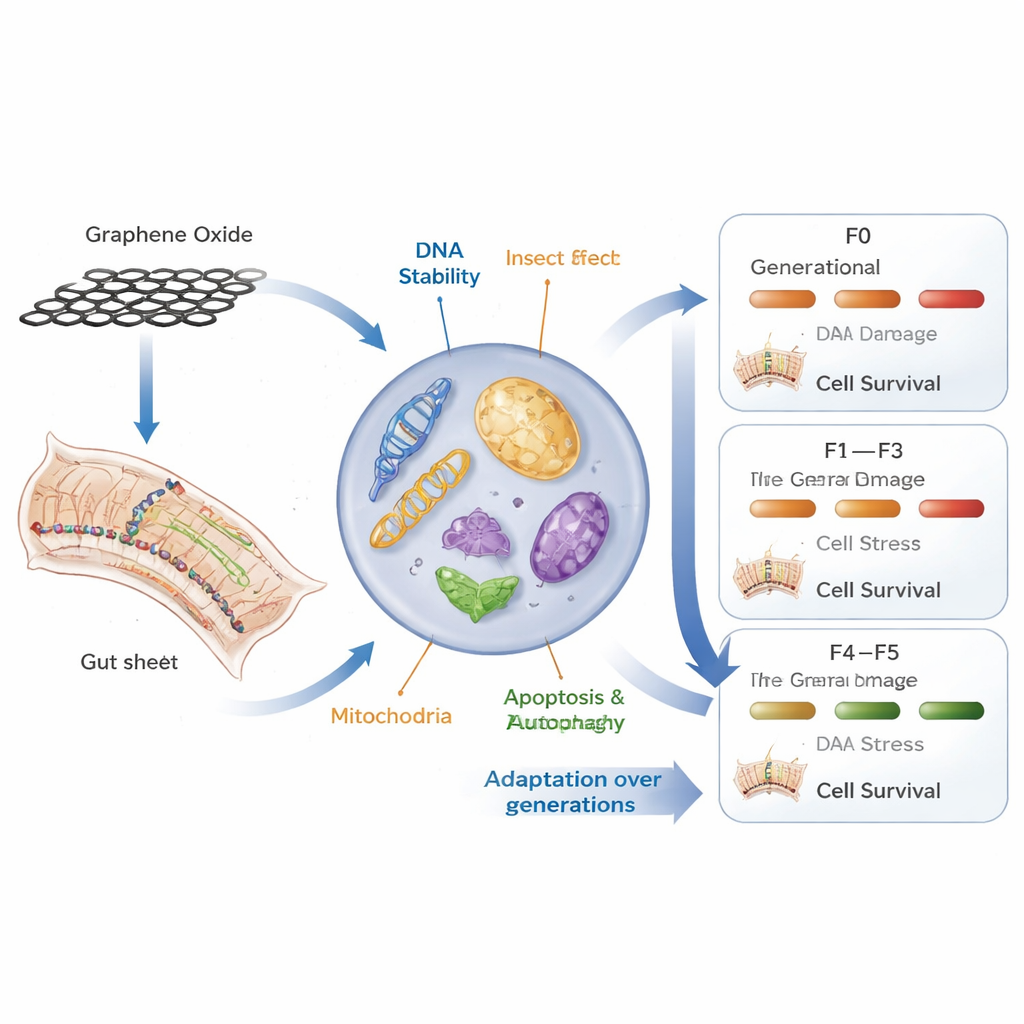
Dostosowanie do nowej normy — a potem jej utrata
Do czwartego pokolenia (F4) obraz znów się zmienił. Wiele z mierzonych wskaźników zdrowia komórek u narażonych świerszczy wróciło w stronę poziomów kontrolnych, a niektóre nawet się poprawiły, co sugeruje, że zwierzęta osiągnęły nowe wewnętrzne równoważenie mimo stałej obecności tlenku grafenu. Analizy statystyczne obejmujące wszystkie markery komórkowe jednocześnie wspierały koncepcję częściowej stabilizacji. Jednak po usunięciu tlenku grafenu z diety w piątym pokoleniu (F5) system został ponownie zaburzony. Zamiast prostego „powrotu” do stanu wyjściowego, pokolenie rekonwalescencji często wykazywało nowe zmiany w uszkodzeniach DNA i stresie komórkowym, jakby nagła utrata długo utrzymującego się czynnika stresowego sama w sobie działała jak wstrząs.
Różne długości życia, różne strategie radzenia sobie
Długowieczny szczep świerszczy nie zachowywał się dokładnie tak jak szczep dziki. W wielu miarach zwierzęta o wydłużonym życiu wydawały się nieco lepiej normalizować uszkodzenia DNA i utrzymywać stabilniejszy ogólny profil komórkowy podczas długotrwałej ekspozycji. Zgodne jest to z ideą, że organizmy selekcjonowane pod kątem większej długości życia często inwestują więcej w naprawę DNA i inne mechanizmy ochronne. Nawet ten szczep wykazywał jednak, że odpowiedzi komórkowe silnie zależały od pokolenia i dawki, podkreślając, że długotrwała ekspozycja na niskim poziomie tlenku grafenu jest daleka od bezpiecznej.
Co to oznacza dla ludzi i środowiska
Dla osoby niebędącej specjalistą kluczowy wniosek jest taki, że tlenek grafenu — nawet na bardzo niskich poziomach — może subtelnie przekształcać sposób funkcjonowania komórek, nie tylko u bezpośrednio narażonych osobników, lecz także przez wiele pokoleń. Badanie sugeruje, że trwałe zmiany mogą być przenoszone przez mechanizmy epigenetyczne: chemiczne przełączniki na DNA i powiązanych białkach, które regulują aktywność genów bez zmiany samego kodu genetycznego. Choć świerszcze nie są ludźmi, stanowią wartościowy substytut dla wielu krótkotrwałych zwierząt w rzeczywistych ekosystemach. Wyniki wskazują, że oceny bezpieczeństwa nanomateriałów powinny wykraczać poza krótkoterminową toksyczność i uwzględniać, jak długotrwała, niskodawkowa ekspozycja może rozchodzić się przez pokolenia, potencjalnie przepisując biologiczną „pamięć” ekspozycji w sposób, który dopiero zaczynamy rozumieć.
Cytowanie: Flasz, B., Babczyńska, A., Tarnawska, M. et al. Response to multigenerational graphene oxide exposure in acheta domesticus strains selected for longevity. Sci Rep 16, 6687 (2026). https://doi.org/10.1038/s41598-026-37623-7
Słowa kluczowe: tlenek grafenu, efekty wielopokoleniowe, dziedziczenie epigenetyczne, nanotoksykologia, model owadzia