Clear Sky Science · pl
Inaktywacja LIMK2 tłumi różnicowanie fibroblastów skóry wywołane mechanicznie oraz oporność na apoptozę
Dlaczego niektóre blizny wymykają się spod kontroli
Większość przecięć i ran pooperacyjnych pozostawia cienką, płaską linię. U niektórych osób proces gojenia przyspiesza jednak nadmiernie, tworząc grube, wypukłe blizny zwane bliznami przerostowymi lub keloidami, które mogą swędzieć, boleć i ograniczać ruch. Badanie to analizuje, dlaczego zwykłe komórki skóry czasem przekształcają się w nadgorliwych producentów blizn i wskazuje na pojedynczy przełącznik molekularny, zwany LIMK2, którego wyciszenie mogłoby zapobiec nadmiernemu rozrostowi blizn.
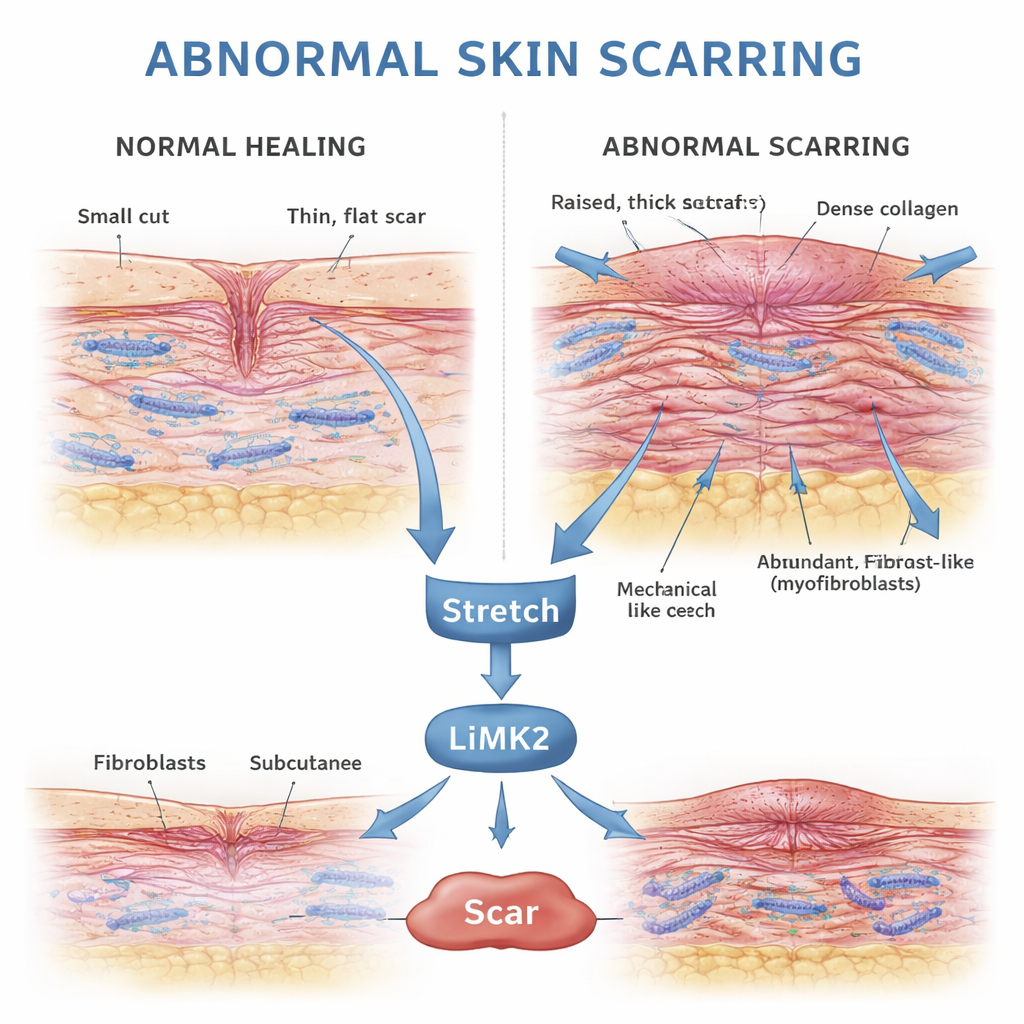
Jak skóra normalnie się goi po urazie
Gdy skóra ulega uszkodzeniu, organizm uruchamia precyzyjnie zorganizowany program naprawczy. Fibroblasty — komórki‑robotnicy z głębszej warstwy skóry — przemieszczają się do rany, mnożą się i odkładają kolagen, białkowy szkielet nowej tkanki. Wiele z tych fibroblastów przechodzi przejściowo w silniejszą, bardziej kurczliwą formę zwaną miofibroblastami, które pomagają zbliżyć brzegi rany. Gdy powierzchnia zostanie zamknięta, a nowa tkanka ustabilizowana, miofibroblasty powinny ulec zaprogramowanej śmierci, apoptozie, pozostawiając skromną, elastyczną bliznę.
Gdy codzienne siły mechaniczne pogarszają blizny
Nieprawidłowe blizny często pojawiają się tam, gdzie skóra jest nieustannie naciągana — na klatce piersiowej, barkach czy dolnej części brzucha. To spostrzeżenie skłoniło badaczy do podejrzenia, że siły mechaniczne, takie jak pociąganie i napięcie działające na gojącą się ranę, mogą skłaniać fibroblasty do zbyt długiej aktywności. Wcześniejsze prace wykazały, że rozciąganie tych komórek w warunkach laboratoryjnych zwiększa poziom białka α‑SMA, markera miofibroblastów, i włącza geny pomagające komórkom opierać się apoptozie. Nowe badanie koncentruje się na LIMK2, kluczowym elemencie łańcucha sygnalizacji mechanicznej wewnątrz komórek, który łączy fizyczne rozciąganie ze zmianami w wewnętrznym szkielecie zbudowanym z filamentów aktynowych.
Kluczowy przełącznik w komórkach tworzących blizny
Aby sprawdzić rolę LIMK2, badacze użyli ludzkich fibroblastów skórnych pochodzących ze skóry zdrowej oraz z tkanek keloidowych. Do części komórek wprowadzili nieaktywną wersję LIMK2, pozostawiając inne niezmienione lub zaopatrując je w ciągle aktywną wersję jako kontrolę. Gdy komórki były mechanicznie rozciągane, normalne fibroblasty reagowały zgodnie z oczekiwaniami: szybki wzrost fosforylowanego kofilinu i wzmocnienie włókien aktynowych, zwiększenie α‑SMA, większa produkcja kolagenu oraz podwyższony poziom Bcl‑2 — białka chroniącego przed śmiercią komórkową — przy jednoczesnym obniżeniu poziomu pro‑apoptotycznego BAX. W uderzającym kontraście fibroblasty z nieczynnym LIMK2 ledwo zmieniały się pod wpływem rozciągania. Nie podnosiły poziomu α‑SMA, nie zwiększały ochronnego Bcl‑2 ani nie zmniejszały BAX, a także wykazywały mniejszą produkcję kolagenu. Komórki te silniej kurczyły żele kolagenowe i poruszały się wolniej w teście przypominającym ranę, co sugeruje słabszą siłę skurczu i ograniczoną zdolność do penetrowania otaczającej tkanki.
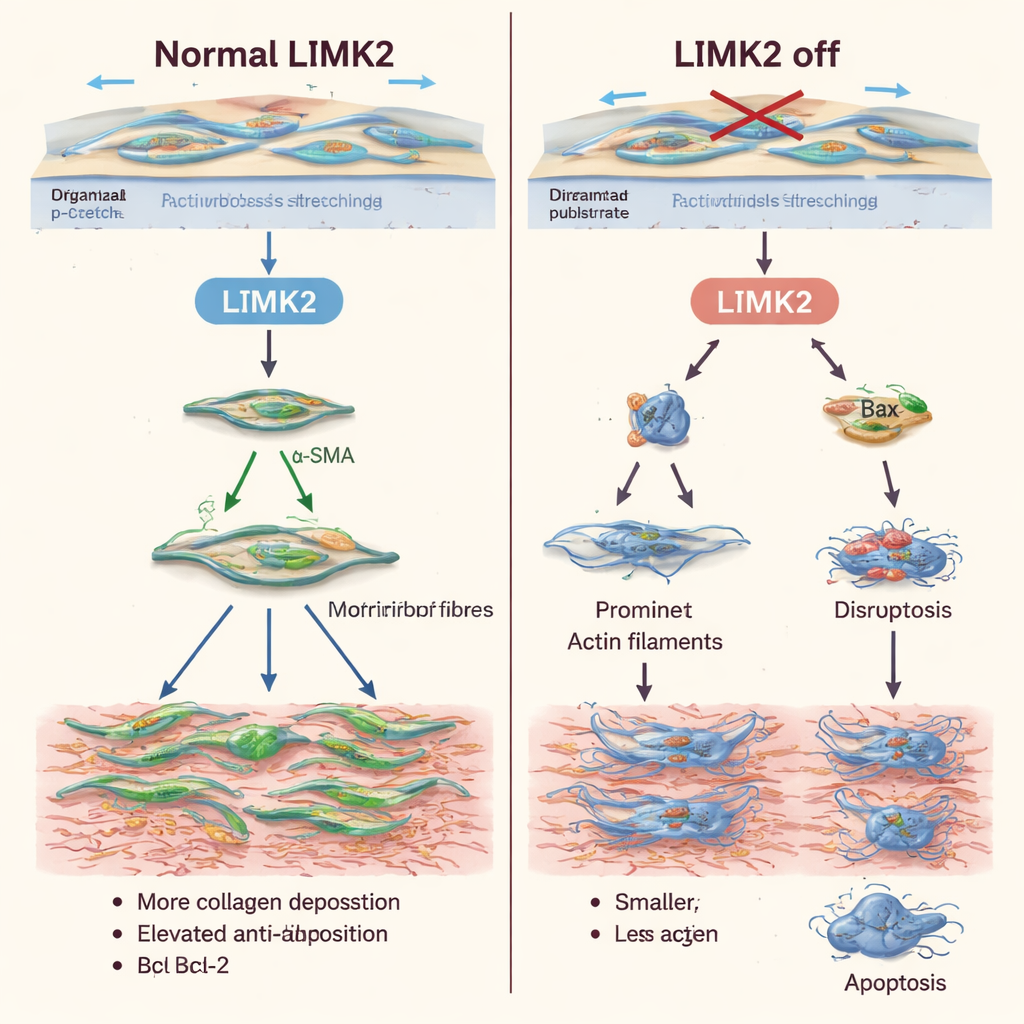
Ułatwianie usuwania uporczywych komórek bliznowatych
Poza zmianą zachowania fibroblastów podczas rozciągania, wyłączenie LIMK2 uczyniło je bardziej podatnymi na śmierć i mniej skłonnymi do proliferacji. Komórki z nieczynnym LIMK2 wykazywały wyższe podstawowe poziomy apoptozy, a rozciąganie mechaniczne — które zwykle działa jako sygnał przeżycia — przestało je chronić. Cytometria przepływowa i barwienia fluorescencyjne potwierdziły, że więcej komórek znajdowało się we wczesnych lub późnych stadiach zaprogramowanej śmierci. Równocześnie pomiary liczby komórek i testy znakowania DNA wykazały, że te komórki dzieliły się znacznie rzadziej niż normalne. Podobne wzorce zaobserwowano po użyciu latrunculiny A, leku zaburzającego filamenty aktynowe, co wspiera hipotezę, że LIMK2 działa głównie poprzez kontrolę wewnętrznego rusztowania komórki.
Co to może znaczyć dla przyszłych terapii blizn
Wyniki sugerują, że LIMK2 znajduje się na skrzyżowaniu, gdzie siły mechaniczne, przeżycie komórek i aktywność budująca blizny się spotykają. Gdy LIMK2 jest aktywny, rozciąganie popycha fibroblasty w stronę odpornego stanu miofibroblastów: kurczą się silnie, opierają się śmierci i produkują nadmiar kolagenu, co sprzyja powstawaniu grubych, wypukłych blizn. Wyłączenie LIMK2 odwraca wiele z tych właściwości — fibroblasty stają się mniej kurczliwe, mniej ruchliwe, mniej płodne i bardziej skłonne do apoptozy. Dla pacjentów może to oznaczać przyszłość, w której kremy, zastrzyki lub opatrunki łagodnie blokujące LIMK2 lub jego pośrednie zmiany w aktynie pomogą ranom o wysokim ryzyku zagoić się z płaskimi, bardziej komfortowymi bliznami.
Cytowanie: Ishii, M., Kuroda, K., Otani, N. et al. LIMK2 inactivation suppresses mechanical stimulation-induced dermal fibroblast differentiation and resistance to apoptosis. Sci Rep 16, 7453 (2026). https://doi.org/10.1038/s41598-026-37610-y
Słowa kluczowe: blizny keloidowe, gojenie ran, fibroblasty, napięcie mechaniczne, apoptoza