Clear Sky Science · pl
Ubikwitynacja SMAD2 przez motyw PY reguluje masę mięśni szkieletowych i zwyrodnienie włókniste
Dlaczego to badanie nad mięśniami ma znaczenie
Wraz z wiekiem wielu z nas zauważa osłabienie i zmniejszenie masy mięśniowej, a w chorobach przewlekłych lub po urazie mięsień może stopniowo zostać zastąpiony twardą tkanką bliznowatą. To badanie zajmuje się podstawowym pytaniem stojącym za tymi zmianami: jak komórki mięśniowe powstrzymują silny sygnał kontrolujący wzrost, zwany TGF‑beta, by nie przesadził i nie doprowadził do utraty mięśni i włóknienia (bliznowacenia)? Odkrywając mały wbudowany „wyłącznik” w kluczowym białku TGF‑beta, autorzy pokazują nowy mechanizm pomagający zachować masę mięśniową i zdrową strukturę tkanki.
Wbudowany hamulec dla silnego sygnału
TGF‑beta to cząsteczka sygnałowa, która mówi komórkom, kiedy spowolnić wzrost, zmienić tożsamość albo wytwarzać tkankę łączną. W mięśniach szkieletowych nadmiar TGF‑beta powoduje kurczenie włókien i sprzyja włóknieniu; jego niedobór może zaburzyć normalną kontrolę wzrostu. Wewnątrz komórek TGF‑beta działa głównie przez białko przekaźnikowe o nazwie SMAD2. Po związaniu TGF‑beta z receptorami na powierzchni komórki SMAD2 zostaje aktywowany i przemieszcza się do jądra, gdzie zmienia aktywność genów. Aby zapobiec trwałemu włączeniu tego sygnału, komórki chemicznie znakują SMAD2 małymi cząsteczkami ubikwityny, oznaczając je do usunięcia. Krótka sekwencja w SMAD2, znana jako motyw PY, jest miejscem dokowania enzymów przyłączających te znaczniki ubikwityny. Badacze zapytali: jeśli to miejsce dokowania zostanie usunięte u żyjącego zwierzęcia, czy hamulec SMAD2 zawiedzie i co stanie się z mięśniami z czasem?
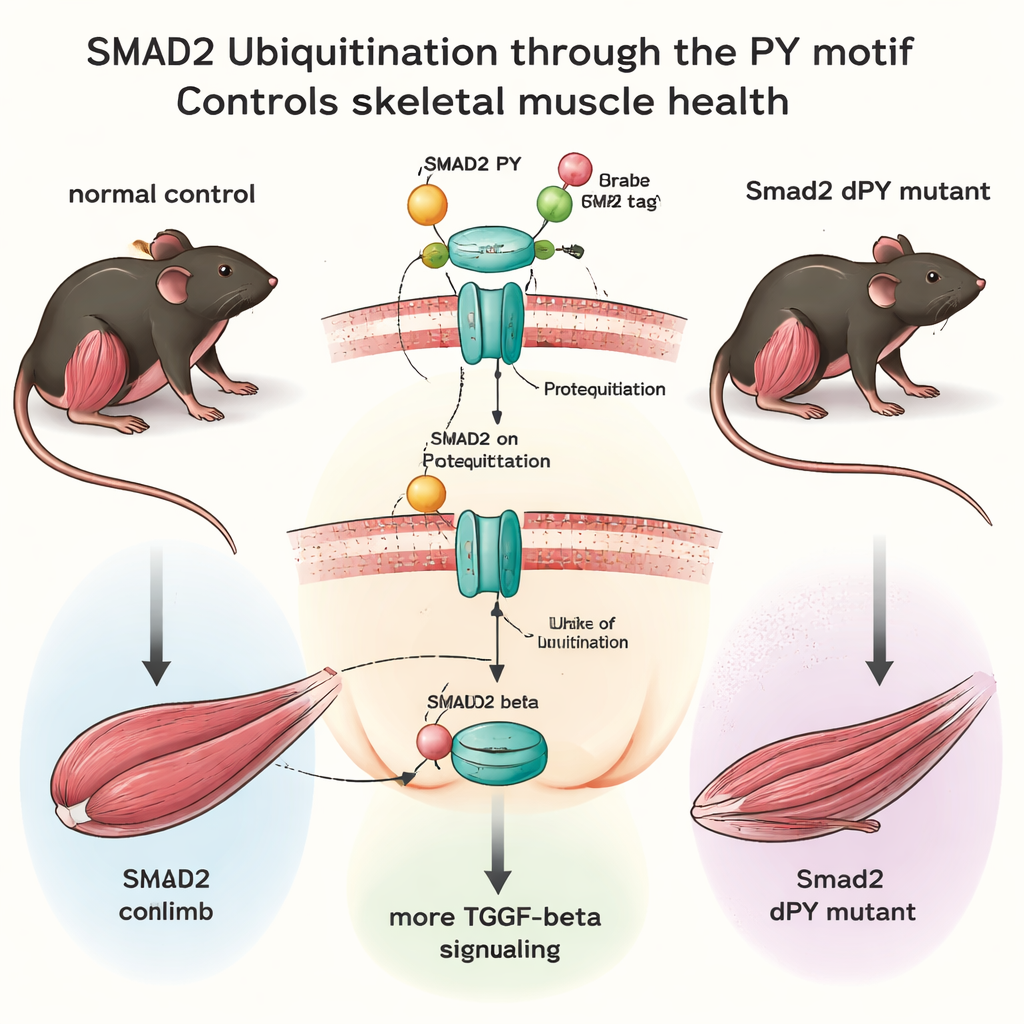
Inżynieria myszy bez znacznika bezpieczeństwa
Używając nowoczesnych narzędzi do edycji genomu, zespół stworzył myszy, którym usunięto z genu Smad2 zaledwie 15 „liter” DNA, precyzyjnie eliminując motyw PY bez zaburzania reszty białka. Te myszy Smad2dPY rodziły się normalnie, dorastały i były płodne, co pokazuje, że ten mechanizm strojenia nie jest niezbędny do podstawowego rozwoju w standardowych warunkach laboratoryjnych. Jednak przy bliższym badaniu mięśni obraz był inny. Młode dorosłe myszy wykazywały tylko subtelne zmiany, ale w wieku około 12 miesięcy — mniej więcej w średnim wieku dla myszy — główne mięśnie kończyn tylnych ważyły mniej, a pojedyncze włókna były mniejsze w porównaniu z normalnymi rodzeństwem. Wewnątrz tych mięśni poziomy białka SMAD2 były wyższe, natomiast jego ubikwitynacja zmniejszona, co potwierdza, że brak motywu PY uczynił SMAD2 bardziej stabilnym i mniej podatnym na degradację.
Nadwrażliwe komórki mięśniowe i zahamowana naprawa
Aby zrozumieć, co to znaczy na poziomie komórkowym, badacze wyizolowali prekursorowe komórki mięśniowe (mioblasty) od myszy mutantów. Po wystawieniu na działanie TGF‑beta in vitro te mioblasty wykazywały silniejszą aktywację SMAD2 i większą indukcję genów reagujących na TGF‑beta niż komórki pochodzące od normalnych myszy. Jednocześnie ich zdolność do łączenia się w długie, wielojądrowe włókna mięśniowe — kluczowy etap wzrostu i regeneracji mięśnia — była upośledzona. Podobne zmiany obserwowano w fibroblastach, komórkach tkanki łącznej znajdujących się między włóknami mięśniowymi: fibroblasty mutantów silniej reagowały na TGF‑beta i chętniej wyrażały geny związane z miofibroblastami formującymi bliznę. Razem te wyniki sugerują, że bez motywu PY zarówno komórki tworzące mięsień, jak i komórki wspierające stają się nadwrażliwe na TGF‑beta, przesuwając równowagę w stronę mniejszych włókien i większej ilości tkanki włóknistej.
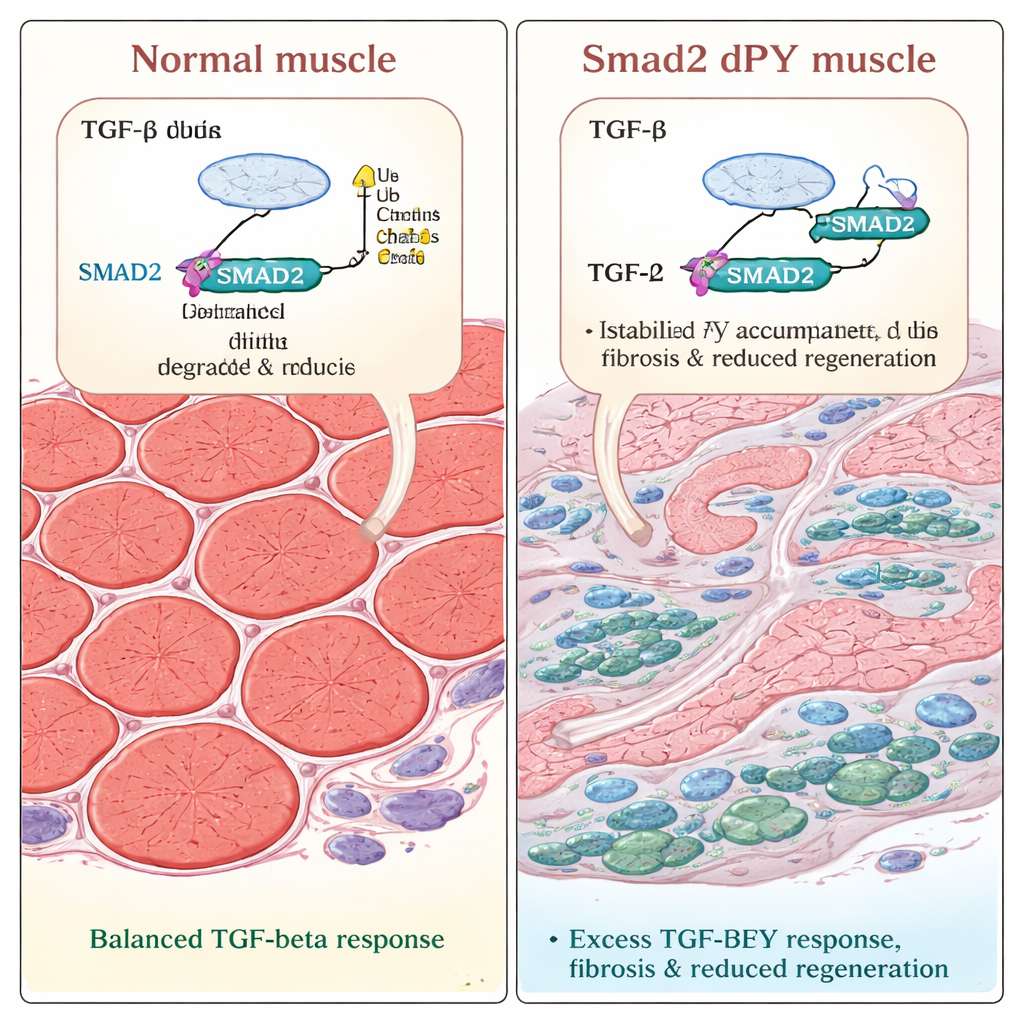
Gdy następuje uraz, wygrywa bliznowacenie
Zespół następnie sprawdził, jak te zmienione mięśnie radzą sobie z uszkodzeniem. Wstrzyknięli toksynę do mięśni nóg, aby wywołać uraz i naprawę — dobrze ugruntowany model regeneracji. Zarówno u normalnych, jak i u mutantów uszkodzone włókna początkowo ulegały rozpadowi, a następnie zaczynały odrastać. Jednak trzy tygodnie po urazie zregenerowane włókna u myszy Smad2dPY były wyraźnie cieńsze. Mikroskopia ujawniła większe obszary wypełnione kolagenem, głównym składnikiem tkanki bliznowatej, oraz zwiększoną liczbę miofibroblastów pozytywnych dla alfa‑gładkokomórkowego aktyny, komórek znanych z napędzania włóknienia. Wyniki te pokazują, że kiedy SMAD2 nie może być prawidłowo znakowany i usuwany, proces naprawy zostaje zaburzony: zamiast w pełni odbudować silny mięsień, tkanka goi się z nadmiarem bliznowacenia i zmniejszoną masą kurczliwą.
Co to oznacza dla zdrowia mięśni
Dla osób niebędących specjalistami główny przekaz jest taki, że bardzo mała cecha molekularna — motyw PY na SMAD2 — działa jako cichy, lecz istotny zabezpieczający mechanizm w mięśniu szkieletowym. Pozwala komórkom osłabić sygnalizację TGF‑beta przez promowanie usuwania SMAD2, pomagając utrzymać prawidłowy rozmiar mięśni i ograniczać włóknienie, szczególnie gdy poziomy TGF‑beta naturalnie rosną z wiekiem lub przy przewlekłych urazach. Gdy to zabezpieczenie jest wyłączone u myszy, mięśnie stopniowo stają się mniejsze i bardziej podatne na bliznowacenie, a po uszkodzeniu nie regenerują się w pełni. Chociaż prace te przeprowadzono na zwierzętach, podkreślają one ubikwitynację SMAD2 jako potencjalną drogę docelową dla przyszłych strategii mających na celu zachowanie masy mięśniowej i zapobieganie zwyrodnieniu włóknistemu w wieku lub chorobie.
Cytowanie: Yamasaki, Y., Sakamoto, K., Yashiro, S. et al. SMAD2 ubiquitination through PY motif regulates skeletal muscle mass and fibrotic degeneration. Sci Rep 16, 6666 (2026). https://doi.org/10.1038/s41598-026-37582-z
Słowa kluczowe: mięsień szkieletowy, sygnalizacja TGF-beta, SMAD2, ubikwitynacja, fibroza