Clear Sky Science · pl
Zmiany aktywności EGFR po edycji domeny wiążącej EGF za pomocą CRISPR/Cas9
Dlaczego przeprogramowanie sygnału nowotworowego ma znaczenie
Rak szyjki macicy często zależy od potężnego przełącznika wzrostu zwanego receptorem naskórkowego czynnika wzrostu (EGFR). Wiele guzów ma ogromne ilości tych receptorów, a mimo to leki mające je wyłączyć pomogły tylko części pacjentów. W badaniu postawiono fundamentalne pytanie o istotnych implikacjach terapeutycznych: co się stanie, jeśli usunąć zdolność EGFR do łapania jego ulubionego sygnału wzrostu, epidermalnego czynnika wzrostu (EGF), nie usuwając samego receptora?
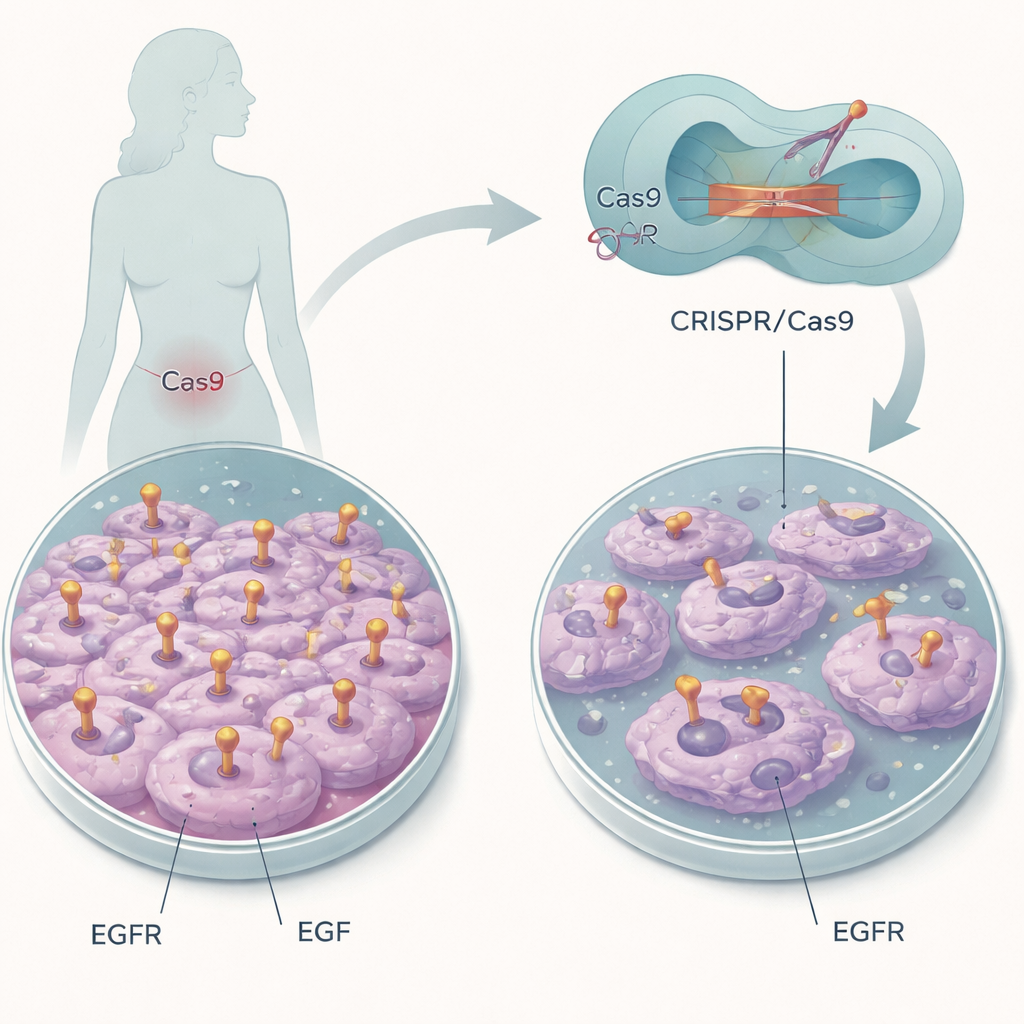
Wyłączanie molekularnego „przełącznika włącz”
Naukowcy skupili się na linii komórkowej raka szyjki macicy, która zawiera duże ilości w przeciwnym razie prawidłowego EGFR. Zamiast niszczyć gen, użyli edycji genomu CRISPR/Cas9 jako molekularnego skalpela, aby zmienić zaledwie kilka aminokwasów w kieszeni wiążącej EGF EGFR. Dwa konkretne miejsca, oznaczone jako L14 i Y45, pomagają EGF zadokować do receptora. Poprzez zastąpienie tych elementów innymi, zespół chciał pozostawić EGFR obecny, lecz ślepym na EGF, co pozwalało wyodrębnić rolę tej pojedynczej interakcji w zachowaniu komórek nowotworowych.
Tworzenie zaprojektowanych linii komórkowych nowotworu
W pierwszym kroku badacze przetestowali te mutacje w komórkach, używając plazmidów, które przejściowo wytwarzały albo normalny, albo zmieniony EGFR. Fluorescencyjnie znakowany EGF wykazał, że wszystkie mutanty wiązały ligand znacznie słabiej niż receptor normalny, szczególnie gdy zmieniono jednocześnie L14 i Y45. Następnie badacze wprowadzili te zmiany bezpośrednio do genomu komórek nowotworowych za pomocą CRISPR/Cas9, generując kilka nowych klonów komórkowych. Niektóre nosiły pojedynczą mutację, inne podwójną mutację na jednej kopii EGFR i inaktywujące zmiany na drugiej. Modelowanie komputerowe powstałych kształtów białka wykazało, że te modyfikacje zniekształcały miejsce wiążące na tyle, by osłabić lub znieść dokowanie EGF, zgodnie z testami wiązania.
Gdy receptor się przemieszcza, ale komórki przeżywają
Szczegółowe obrazowanie ujawniło, że edytowane receptory zachowywały się wewnątrz komórki bardzo inaczej. W nieedytowanych komórkach nowotworowych EGFR siedzi na powierzchni komórki, łapie EGF, a następnie przemieszcza się do wnętrza, ulegając aktywacji chemicznej przez fosforylację. W klonach z podwójną mutacją wiązanie EGF praktycznie zanikło, a EGFR nie był już widoczny na błonie; zamiast tego niewielka ilość pozostałego receptora gromadziła się we wnętrzu komórki. Nawet pojedyncza zmiana Y45 znacząco zmniejszyła wiązanie i obniżyła całkowity poziom EGFR. Mimo tej ingerencji w podręcznikową trasę sygnalizacji EGF–EGFR, komórki nowotworowe pozostały żywotne i nadal rosły w hodowli z tylko skromnymi zmianami w cyklu komórkowym.
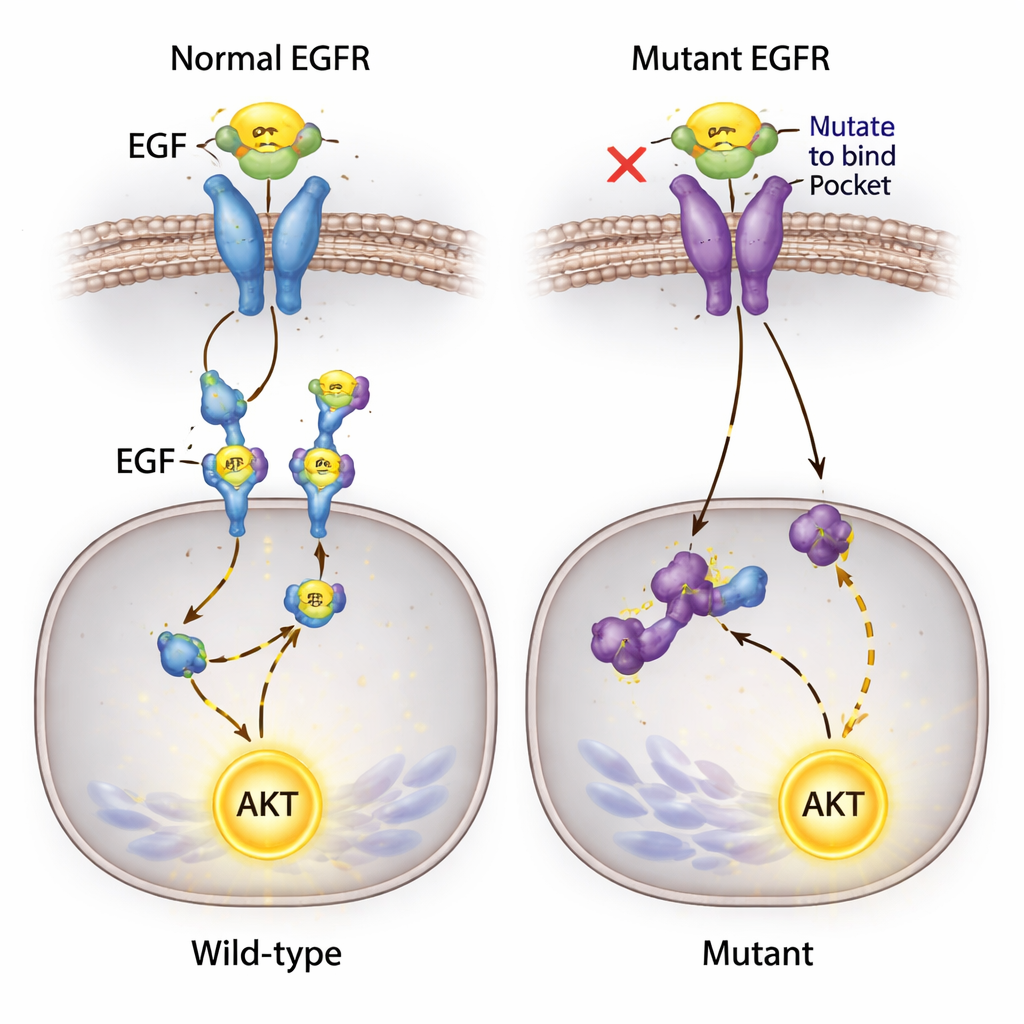
Niespodziewany sygnał, który nie ustępuje
Jednym z najbardziej zaskakujących ustaleń był AKT, kluczowe białko promujące przeżycie komórki, zwykle aktywowane w dółstrumieniowo od EGFR. Badacze spodziewali się, że zablokowanie wiązania EGF z EGFR uciszy ten szlak. Zamiast tego, gdy dodali EGF do podłoża, AKT ulegał silnej aktywacji we wszystkich liniach komórkowych — w tym w tych, gdzie EGF nie mógł już wiązać EGFR i gdzie fosforylacja receptora była niewykrywalna. Ponieważ komórki te noszą znaną mutację w innym genie sygnalizacyjnym, PIK3CA, zespół przypuszcza, że alternatywne drogi mogą umożliwiać przekazywanie sygnału EGF na aktywację AKT, być może przez inne białka powierzchniowe lub tło mutacyjne, omijając zmodyfikowany EGFR.
Ukryte zmiany genetyczne i przyszłe terapie
Aby upewnić się, że CRISPR nie powoduje rozległych niezamierzonych zmian, naukowcy zsekwencjonowali całe genomy nowych linii komórkowych. Potwierdzili obecność pożądanych mutacji EGFR i nie znaleźli dowodów na przecięcia w przewidywanych miejscach poza celem dla przewodników CRISPR. Zidentyfikowali jednak wiele spontanicznych mutacji rozsianych po genomie, z których niektóre mogą wpływać na zachowanie komórek. Podkreśla to, że nawet gdy CRISPR trafia we właściwy adres, niestabilne DNA komórek nowotworowych może komplikować interpretację wyników eksperymentów i projektowanie precyzyjnych terapii genowych.
Co to oznacza dla pacjentów
Dla laików kluczowy wniosek jest taki, że samo zablokowanie uścisku między EGF a EGFR — nawet bardzo precyzyjnie na poziomie atomowym — nie zatrzymuje automatycznie komórek nowotworowych przed otrzymywaniem poleceń „rośnij i przetrwaj”. Badanie pokazuje, że komórki nowotworowe potrafią przekierować kluczowe sygnały, takie jak aktywacja AKT, wokół zablokowanego receptora, a sama edycja CRISPR musi być starannie oceniana w takich niestabilnych genomach. Te zaprojektowane linie komórkowe stanowią teraz potężny model laboratoryjny do poszukiwania zapasowych szlaków podtrzymujących nowotwory zależne od EGFR — informacja, która ostatecznie może doprowadzić do terapii łączonych celujących zarówno w EGFR, jak i jego ukrytych wspólników.
Cytowanie: Popović, J., Hahut, A., Torres, G.E. et al. Changes in EGFR activity following CRISPR/Cas9-editing of the EGF binding domain. Sci Rep 16, 6797 (2026). https://doi.org/10.1038/s41598-026-37579-8
Słowa kluczowe: EGFR, rak szyjki macicy, CRISPR, sygnalizacja EGF, szlak AKT