Clear Sky Science · pl
Amplifikacja liczby kopii powoduje nadekspresję IFI30 i skoordynowaną aktywację odporności, identyfikując nowy cel diagnostyczny i terapeutyczny w gruczolakoraku żołądka
Dlaczego białko w żołądku ma znaczenie
Rak żołądka należy do najgroźniejszych nowotworów na świecie, głównie dlatego, że często wykrywany jest późno i bywa trudny do leczenia. W tym badaniu skupiono się na mało znanym białku o nazwie IFI30, obecnym w komórkach pomagających układowi odpornościowemu rozpoznawać zagrożenia. Śledząc, jak IFI30 jest zmieniane w guzach żołądka i jak wpływa na reakcje obronne organizmu, autorzy sugerują, że może ono stać się silnym narzędziem do wcześniejszej diagnostyki oraz do doboru skuteczniejszych, spersonalizowanych terapii.
Ukryty sygnał w guzach żołądka
Zespół zaczął od podstawowego pytania: czy IFI30 występuje na innych poziomach w zdrowych tkankach żołądka w porównaniu z tkankami nowotworowymi? Korzystając z dużych publicznych zbiorów danych łączących aktywność genów z tysięcy próbek, odkryli, że IFI30 jest konsekwentnie znacznie wyższe w gruczolakoraku żołądka — najczęstszym typie raka żołądka — niż w normalnym nabłonku żołądka. Obserwacja ta potwierdziła się w wielu niezależnych grupach pacjentów oraz zarówno na poziomie RNA, jak i białka. Gdy autorzy oceniali, jak dobrze samo IFI30 rozróżnia tkankę nowotworową od zdrowej, jego skuteczność była uderzająca: dokładność diagnostyczna (AUC) wyniosła 0,92, co dla pojedynczego markera uważa się za doskonały wynik. Obrazy mikroskopowe umiejscowiły IFI30 w wewnętrznym systemie recyklingu komórkowego, gdzie przetwarzane są antygeny do rozpoznania przez układ odpornościowy.
Zmiany w DNA, które zwiększają IFI30
Następnie badacze zastanawiali się, dlaczego IFI30 jest tak podwyższone w tych guzach. Przeszukując genom nowotworów w bazie The Cancer Genome Atlas, stwierdzili, że dodatkowe kopie genu IFI30 — znane jako amplifikacje liczby kopii — były głównym mechanizmem nadekspresji. Guzy z amplifikacją IFI30 wykazywały zwykle większą niestabilność genomową i często niosły znane mutacje nowotworowe, takie jak TP53 i PIK3CA. Wraz ze wzrostem liczby kopii IFI30 rosły też jego poziomy RNA, co sugeruje bezpośredni związek między strukturalnymi zmianami w DNA a zwiększoną produkcją tego białka. To przedstawia IFI30 nie jako biernego obserwatora, lecz jako element szerszego wzorca agresywnej biologii guza.
Komunikacja immunologiczna wokół guza
Ponieważ IFI30 bierze udział w przetwarzaniu materiału, który komórki odpornościowe prezentują jako „listy poszukiwane” limfocytom T, zespół badał, gdzie dokładnie lokuje się ono w mikrośrodowisku guza. Sekwencjonowanie pojedynczych komórek, które odczytuje ekspresję genów w pojedynczych komórkach, wykazało, że IFI30 jest szczególnie wzbogacone w komórkach dendrytycznych, makrofagach i limfocytach CD8 — kluczowych graczach w inicjowaniu i podtrzymywaniu odporności przeciwnowotworowej. Analizy sieciowe ujawniły intensywną komunikację między komórkami odpornościowymi bogatymi w IFI30 a otaczającymi komórkami guza i stromalnymi. Guzy z wysokim IFI30 wykazywały silną aktywację szlaków związanych z prezentacją antygenów, sygnałami zapalnymi i cząsteczkami komunikacyjnymi przyciągającymi i organizującymi komórki odpornościowe. Jednocześnie te guzy pokazywały cechy inwazji i stresu, takie jak przyspieszenie cyklu komórkowego, przebudowa tkanki i adaptacja do niskiego poziomu tlenu, podkreślając rolę IFI30 na styku ataku i obrony w nowotworze.
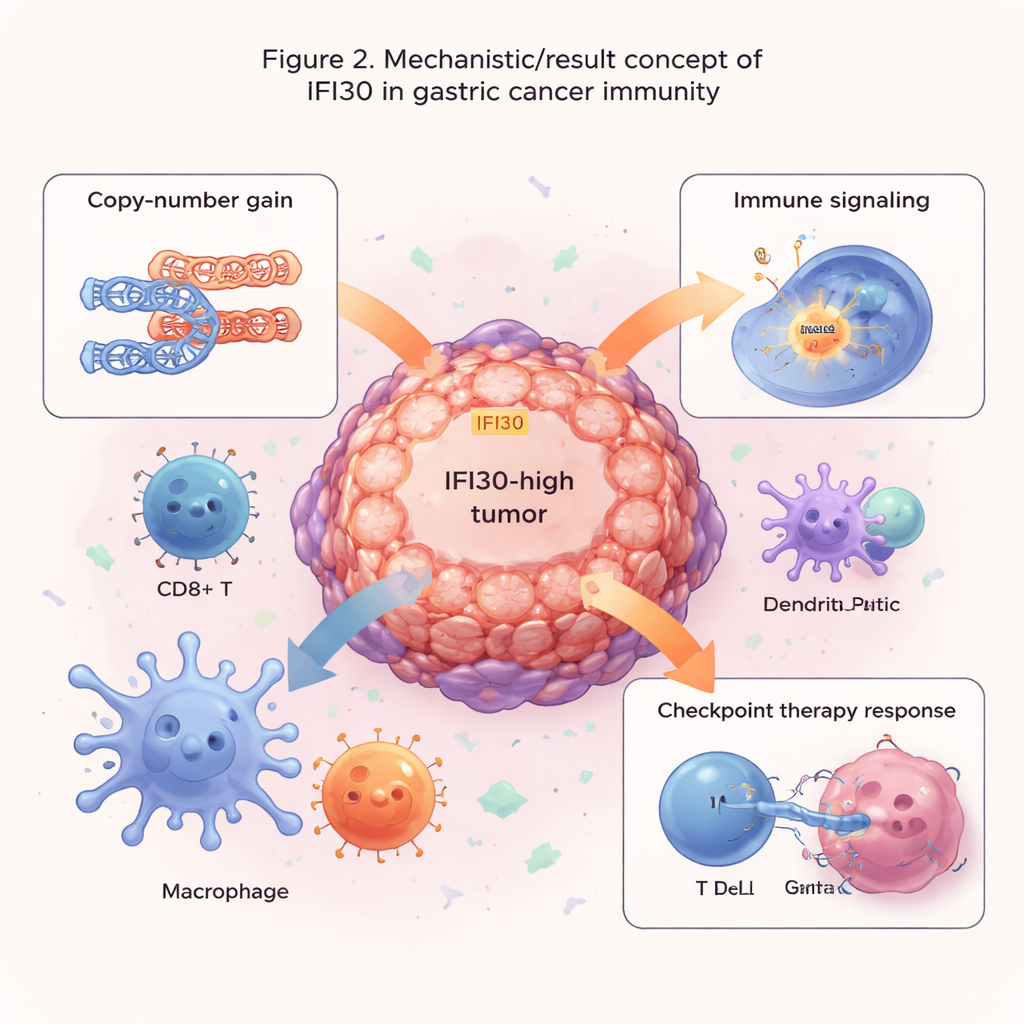
Wskazówki dla doboru leków i immunoterapii
Autorzy sprawdzili następnie, czy IFI30 może pomóc przewidzieć odpowiedź guzów na leczenie. Łącząc poziomy IFI30 z dużymi zbiorami danych dotyczącymi odpowiedzi na leki, stwierdzili, że guzy o wysokim IFI30 mają tendencję do oporności na niektóre leki celujące w podział komórek lub powszechny szlak wzrostu (MAPK), ale wydają się bardziej wrażliwe na leki blokujące sygnalizację EGFR i PI3K/AKT. Co istotne, poziomy IFI30 były silnie skorelowane z PD-L1, głównym hamulcem dla limfocytów T, będącym celem współczesnych inhibitorów punktów kontrolnych. W kilku badaniach immunoterapeutycznych pacjenci z guzami o wyższej ekspresji IFI30 częściej odpowiadali na blokadę punktów kontrolnych niż ci z niskim poziomem. Skala oparta na IFI30 przewyższała ustalone miary, takie jak obciążenie mutacyjne guza i sam PD-L1, i była szczególnie wzbogacona w guzach o wysokiej niestabilności mikrosatelitarnej — podgrupie już znanej z lepszych odpowiedzi na immunoterapię.
Od biurka badawczego do potencjalnego nowego celu
Aby sprawdzić, czy IFI30 jest tylko markerem, czy także wspiera wzrost nowotworu, zespół zmniejszył jego poziomy w liniach komórkowych raka żołądka za pomocą narzędzi genetycznych. Po obniżeniu IFI30 komórki nowotworowe rosły wolniej, co wskazuje na bezpośrednią rolę w podtrzymywaniu proliferacji guza. Podsumowując, dane sugerują, że IFI30 jest zarówno odczytem aktywności immunologicznej, jak i czynnikiem przyczyniającym się do złośliwego zachowania. Dla pacjentów oznacza to, że prosty pomiar IFI30 mógłby pewnego dnia pomóc lekarzom w bardziej wiarygodnym wykrywaniu raka żołądka, przewidywaniu, kto może skorzystać na określonych lekach celowanych lub immunoterapiach, oraz ewentualnie kierowaniu nowych terapii, które bezpośrednio lub pośrednio blokowałyby tumor-promujące działania IFI30.
Cytowanie: Liu, Q., Yuan, W., Zhaowang, R. et al. Copy-number amplification drives IFI30 overexpression and coordinated immune activation, identifying a novel diagnostic and therapeutic target in gastric adenocarcinoma. Sci Rep 16, 6945 (2026). https://doi.org/10.1038/s41598-026-37574-z
Słowa kluczowe: rak żołądka, IFI30, marker, odporność nowotworowa, immunoterapia